名校
解题方法
1 . 某化学课题小组将二氧化硫的制备与多个性质实验进行了一体化设计,实验装置如图所示。已知: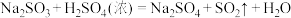 ,下列说法错误的是
,下列说法错误的是
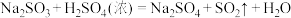 ,下列说法错误的是
,下列说法错误的是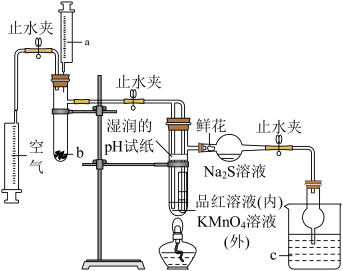
A.a、b、c中盛装物质可以分别为浓硫酸、 固体、 固体、 溶液 溶液 |
B.实验时,湿润的pH试纸、鲜花、品红溶液、酸性 溶液均褪色, 溶液均褪色, 溶液中出现淡黄色沉淀 溶液中出现淡黄色沉淀 |
C.此设计可证明 水溶液呈酸性, 水溶液呈酸性, 具有氧化性、还原性、漂白性 具有氧化性、还原性、漂白性 |
D.点燃酒精灯加热,可证明 使品红溶液褪色具有可逆性,使酸性 使品红溶液褪色具有可逆性,使酸性 溶液褪色不具有可逆性 溶液褪色不具有可逆性 |
您最近一年使用:0次
2024-02-02更新
|
468次组卷
|
3卷引用:浙江金华第一中学2023-2024学年高一下学期4月期中考试化学试题
浙江金华第一中学2023-2024学年高一下学期4月期中考试化学试题河南省南阳市2023-2024学年高一上学期1月期末化学试题(已下线)专题01 硫及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
解题方法
2 . 硫是重要的非金属元素,也是人类较早认识的化学元素之一。人们对硫元素的利用,其本质就是通过各种化学反应,实现含硫元素的物质之间的转化。
(1)硫可以形成分子式为 、
、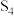 、
、 、
、 的单质,其中
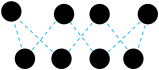
的单质,其中 的分子球棍模型如图所示。下列有关说法正确的是_______。
的分子球棍模型如图所示。下列有关说法正确的是_______。
(2)将 气体通入
气体通入 溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是_______。
溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是_______。
(3)用如图所示实验装置(部分夹持仪器已略去)探究铜丝与过量浓硫酸的反应。
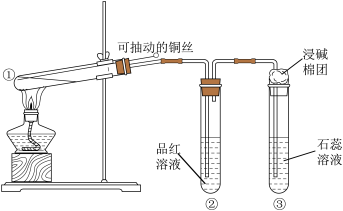
下列实验或说法不合理的是_______。
(4)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是_______ 。不采用铜跟浓硫酸反应来制取硫酸铜的原因是_______ 。
(5)在 溶液中滴加少量
溶液中滴加少量 溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目
溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目_______ 。
_______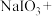 _______
_______ _______
_______ _______
_______ _______
_______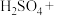 _______
_______
(6)中华人民共和国国家标准(G2762022)规定葡萄酒中 最大使用量为0.25 g⋅L-1,取300.00 mL葡萄酒,通过适当的方法使所含
最大使用量为0.25 g⋅L-1,取300.00 mL葡萄酒,通过适当的方法使所含 全部逸出并用
全部逸出并用 将其全部氧化为
将其全部氧化为 ,消耗浓度为0.0900 mol•L-1NaOH标准溶液25mL,该葡萄酒中
,消耗浓度为0.0900 mol•L-1NaOH标准溶液25mL,该葡萄酒中 含量为
含量为_______ g·L-1。
(7)同学们继续设计实验探究亚硫酸与次氯酸的酸性强弱:甲同学查阅资料得知 为难溶于水的白色沉淀,因此设计了实验方案为:将
为难溶于水的白色沉淀,因此设计了实验方案为:将 通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
 ,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的反应原理是错误的,理由是
,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的反应原理是错误的,理由是_______ 。
(1)硫可以形成分子式为
 、
、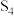 、
、 、
、 的单质,其中
的单质,其中 的分子球棍模型如图所示。下列有关说法正确的是_______。
的分子球棍模型如图所示。下列有关说法正确的是_______。
A.1 mol  单质中含有的S—S键个数为 单质中含有的S—S键个数为 |
B. 、 、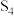 、 、 、 、 互为同位素 互为同位素 |
C.硫的单质在足量的空气中完全燃烧可生成 |
D. 的摩尔质量为32 g/mol 的摩尔质量为32 g/mol |
 气体通入
气体通入 溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是_______。
溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是_______。A. | B. | C. | D. |

下列实验或说法不合理的是_______。
A.上下移动①中铜丝可控制 的量 的量 |
B.②中品红溶液是验证 的生成 的生成 |
| C.③中石蕊溶液先变红后褪色 |
D.为确认 生成,向①中加水,观察颜色 生成,向①中加水,观察颜色 |
(5)在
 溶液中滴加少量
溶液中滴加少量 溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目
溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目_______
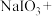 _______
_______ _______
_______ _______
_______ _______
_______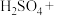 _______
_______
(6)中华人民共和国国家标准(G2762022)规定葡萄酒中
 最大使用量为0.25 g⋅L-1,取300.00 mL葡萄酒,通过适当的方法使所含
最大使用量为0.25 g⋅L-1,取300.00 mL葡萄酒,通过适当的方法使所含 全部逸出并用
全部逸出并用 将其全部氧化为
将其全部氧化为 ,消耗浓度为0.0900 mol•L-1NaOH标准溶液25mL,该葡萄酒中
,消耗浓度为0.0900 mol•L-1NaOH标准溶液25mL,该葡萄酒中 含量为
含量为(7)同学们继续设计实验探究亚硫酸与次氯酸的酸性强弱:甲同学查阅资料得知
 为难溶于水的白色沉淀,因此设计了实验方案为:将
为难溶于水的白色沉淀,因此设计了实验方案为:将 通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
 ,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的反应原理是错误的,理由是
,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的反应原理是错误的,理由是
您最近一年使用:0次
3 . 绿色化学理念影响着整个化学实验改革,微型化学实验就是在这种复背景下诞生的一种创新性的实验教学方法。蔗糖与浓硫酸反应的探究实验改进装置如图所示。下列说法不正确的是


| A.反应中,品红溶液褪色,紫色石蕊试液先变红后褪色 |
| B.该实验体现了浓硫酸的脱水性和强氧化性 |
| C.该装置能证明二氧化硫具有氧化性 |
| D.X可以是NaOH溶液 |
您最近一年使用:0次
2023-04-11更新
|
352次组卷
|
4卷引用:广东省河源市龙川县第一中学2022-2023学年高一下学期4月期中考试化学试题
4 . 绿色化学理念影响着整个化学实验改革,微型化学实验就是在这种复背景下诞生的一种创新性的实验教学方法。蔗糖与浓硫酸反应的探究实验改进装置如图所示。下列说法不正确的是


| A.该实验体现了浓硫酸的脱水性和强氧化性 |
| B.实验中,品红溶液、紫色石蕊试液均褪色 |
| C.该装置能证明二氧化硫具有氧化性 |
| D.X可以是NaOH溶液 |
您最近一年使用:0次
名校
解题方法
5 . 向 溶液中通入过量
溶液中通入过量 ,过程和现象如图。
,过程和现象如图。
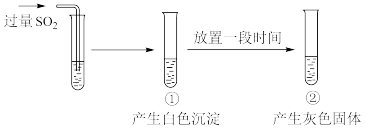
经检验,白色沉淀为 ;灰色固体中含有
;灰色固体中含有
下列说法不正确 的是
 溶液中通入过量
溶液中通入过量 ,过程和现象如图。
,过程和现象如图。
经检验,白色沉淀为
 ;灰色固体中含有
;灰色固体中含有
下列说法
A.①中生成白色沉淀的离子方程式为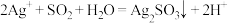 |
B.①中未生成 ,证明溶解度: ,证明溶解度: 小于 小于 |
C.②中的现象体现了 的氧化性 的氧化性 |
D.该实验条件下 与 与 反应生成 反应生成 的速率大于生成 的速率大于生成 的速率 的速率 |
您最近一年使用:0次
2023-04-24更新
|
235次组卷
|
2卷引用:北京市第八中学2022-2023学年高一下学期期中考试(选考班)化学试题
名校
6 . 某小组设计了二氧化硫的制备与性质一体化实验,其装置如图所示。下列说法错误的是

A.a、b、c中依次盛装70%硫酸、 固体,NaOH 溶液 固体,NaOH 溶液 |
B.实验时,湿润的pH试纸、鲜花、品红溶液、 溶液均褪色, 溶液均褪色, 溶液中出现淡黄色沉淀 溶液中出现淡黄色沉淀 |
C.点燃酒精灯加热,品红溶液恢复原色, 溶液不恢复原色 溶液不恢复原色 |
D.此设计可证明 水溶液的酸性、 水溶液的酸性、 的氧化性、还原性、漂白性 的氧化性、还原性、漂白性 |
您最近一年使用:0次
2023-04-21更新
|
294次组卷
|
2卷引用:湖北省武汉市部分重点中学2022-2023学年高一下学期期中联考化学试题
解题方法
7 . SO2是硫元素中一种重要物质。在生产生活中有着重要用途。
(1)某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。

①通入足量SO2时C中观察到的现象为_______ 。
②根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
a.写出SO2与FeCl3溶液反应的离子方程式:_______ 。
b.装置D中倒立漏斗的作用是_______ ,发生反应的离子方程式是_______ ,
c.该小组同学认为C中溶液颜色的改变说明硫元素的价态发生了变化,甲同学认为可以补充一个实验进一步证明硫元素的价态转化,实验方案和现象为:取变色后的溶液于试管中:_______ 。
③为了验证SO2在本实验中体现出的性质,实验中可以代替FeCl3溶液的试剂有_______ (填字母)。
A.浓硫酸 B.酸性KMnO4溶液 C.碘水 D.NaCl溶液
(2)物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价-类”二维图。下列说法错误的是________

(1)某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。

①通入足量SO2时C中观察到的现象为
②根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
a.写出SO2与FeCl3溶液反应的离子方程式:
b.装置D中倒立漏斗的作用是
c.该小组同学认为C中溶液颜色的改变说明硫元素的价态发生了变化,甲同学认为可以补充一个实验进一步证明硫元素的价态转化,实验方案和现象为:取变色后的溶液于试管中:
③为了验证SO2在本实验中体现出的性质,实验中可以代替FeCl3溶液的试剂有
A.浓硫酸 B.酸性KMnO4溶液 C.碘水 D.NaCl溶液
(2)物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价-类”二维图。下列说法错误的是________

| A.c能使紫色石蕊溶液变红 |
| B.b在纯氧气中点燃可生成d |
| C.g既具有氧化性也具有还原性 |
| D.酸雨久置可发生e到f的转化 |
您最近一年使用:0次
解题方法
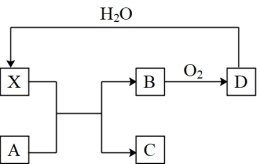
8 . 已知X为一种常见酸的浓溶液,能使蔗糖变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是

| A.X使蔗糖变黑的现象主要体现了X的强氧化性 |
| B.若A为铁,则足量A与X在室温下即可完全反应 |
| C.若A为碳单质,将气体B通入品红溶液褪色,证明B有还原性 |
| D.工业上,B转化为D的反应条件为加热、使用催化剂 |
您最近一年使用:0次
名校
解题方法
9 . 某化学实验小组的同学利用铜与浓硫酸反应制取二氧化硫并研究其性质,所用实验装置如下:
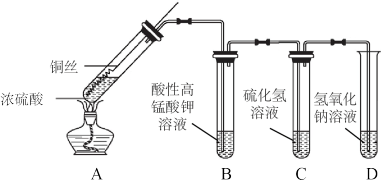
回答下列问题:
(1)将铜丝下端卷成螺旋状的理由是_______ 。
(2)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是_______ 。
(3)用化学方程式表示氢氧化钠溶液的作用是_______ 。
(4)装置A中反应的化学方程式是_______ 。
(5)装置B和装置C分别验证了二氧化硫的_______ 性质。
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是_______(填字母)。已知:Cu2S、CuS不溶于稀硫酸。

回答下列问题:
(1)将铜丝下端卷成螺旋状的理由是
(2)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是
(3)用化学方程式表示氢氧化钠溶液的作用是
(4)装置A中反应的化学方程式是
(5)装置B和装置C分别验证了二氧化硫的
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是_______(填字母)。已知:Cu2S、CuS不溶于稀硫酸。
| 硫酸浓度/(mol· L-1) | 黑色物质出现的温度/°C | 黑色物质消失的温度/°C |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
| A.取黑色物质洗涤、干燥后称量,加入足量稀硫酸充分混合,再取固体洗涤、干燥后称量,固体质量不变,说明黑色物质中不含CuO |
| B.黑色物质消失过程中有SO2、H2S生成 |
| C.相同条件下,硫酸浓度越大,反应速率越快,黑色物质越易出现、越易消失 |
| D.硫酸浓度为16mol/L时,先升温至250°C以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质 |
您最近一年使用:0次
2022-04-27更新
|
230次组卷
|
2卷引用:山西省运城市高中联合体2021-2022学年高一下学期期中联考化学试题
10 . 二氧化硫是中学化学的重要物质。某化学兴趣小组设计如图实验探究SO2的性质。
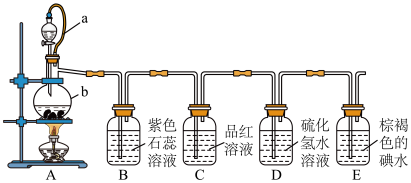
(1)仪器b的名称是_______ ,已知b中放入的是纯铜片,写出装置A中的化学方程式_______ 。
(2)同学甲认为该套装置存在一个明显缺陷,其理由是_______ 。
(3)关于该探究实验,下列说法错误的是_______ 。
①装置A中,橡皮管a的作用是使分液漏斗中的液体能顺利流下
②装置B中,紫色溶液变红,证明二氧化硫是酸性氧化物
③装置C中,品红溶液褪色;证明二氧化硫具有漂白性
④装置D中溶液变浑浊,生成了硫单质,证明SO2具有还原性
(4)装置E中溶液褪色,发生的反应离子方程式是_______ 。
(5)实验过程中,同学乙观察到E中溶液在完全褪色后开始逐渐变浑浊。查阅资料后得知,在催化剂的作用下,SO2在水中会发生歧化反应。于是又设计以下实验进行探究(实验中溶液的体积及溶质的物质的量浓度均相同)。
【实验装置】
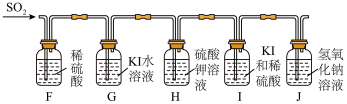
【实验现象】一段时间后,F、H中无明显现象,I中比G中的溶液先变浑浊。
【实验结论】在水中,SO2歧化的离子方程式为_______ 。该反应中的催化剂是_______ (填写序号)。
①H⁺ ②I⁻ ③H⁺、I⁻ ④K⁺、H⁺ ⑤K⁺、I⁻

(1)仪器b的名称是
(2)同学甲认为该套装置存在一个明显缺陷,其理由是
(3)关于该探究实验,下列说法错误的是
①装置A中,橡皮管a的作用是使分液漏斗中的液体能顺利流下
②装置B中,紫色溶液变红,证明二氧化硫是酸性氧化物
③装置C中,品红溶液褪色;证明二氧化硫具有漂白性
④装置D中溶液变浑浊,生成了硫单质,证明SO2具有还原性
(4)装置E中溶液褪色,发生的反应离子方程式是
(5)实验过程中,同学乙观察到E中溶液在完全褪色后开始逐渐变浑浊。查阅资料后得知,在催化剂的作用下,SO2在水中会发生歧化反应。于是又设计以下实验进行探究(实验中溶液的体积及溶质的物质的量浓度均相同)。
【实验装置】

【实验现象】一段时间后,F、H中无明显现象,I中比G中的溶液先变浑浊。
【实验结论】在水中,SO2歧化的离子方程式为
①H⁺ ②I⁻ ③H⁺、I⁻ ④K⁺、H⁺ ⑤K⁺、I⁻
您最近一年使用:0次
2022-11-15更新
|
325次组卷
|
2卷引用:湖北省黄冈市2022-2023学年高三上学期期中质量抽测化学试题



