解题方法
1 . 2022年6月5日是第51个世界环境日,主题是共建清洁美丽世界。下列行为不符合该主题的是
| A.推广电动汽车,践行绿色交通 |
| B.使用绿色化学工艺,开发绿包产品 |
| C.大量使用农药和化肥,确保粮食产量 |
| D.工业废气净化达标后排放,减少雾霾的形成 |
您最近一年使用:0次
2 . 下列说法错误的是
| A.开发燃料电池汽车,有利于减少机动车尾气污染 |
| B.开发利用太阳能、风能等新能源代替化石能源,利于实现低碳经济 |
| C.天然气是推广使用的清洁燃料 |
| D.在燃煤中加入生石灰,可减少CO2的排放 |
您最近一年使用:0次
名校
3 . SO2、CO、NO、NO2及其他氮氧化物都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题。
(1)上述四种气体中直接排入空气时会引起酸雨的有____ (填化学式)。
(2)回收大气污染物SO2的方法如下:
方法一:在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和液态H2O。已知:
CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(1) △H=-295.9kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-297.2kJ·mol-1
则CH4的燃烧热的热化学方程式为:___ 。
方法二:在恒容密闭容器中,用H2还原SO2生成S的反应分两步完成(如图1所示),该过程中部分物质的物质的量浓度随时间的变化关系如图2所示:

①由分析可知X为____ (填化学式)。
②0~t1时间段的温度为____ 。
方法三:利用反应:NO2(g)+SO2(g) SO3(g)+NO(g)。
SO3(g)+NO(g)。
③一定条件下,将NO2与SO2以体积比1∶1置于恒温恒容的密闭容器中发生反应:NO2(g)+SO2(g) SO3(g)+NO(g),能说明反应达到平衡状态的是
SO3(g)+NO(g),能说明反应达到平衡状态的是____ (填字母)。
a.混合气体的密度保持不变
b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变
d.每生成1molSO3的同时消耗1molNO
e.容器内的混合气体平均相对分子质量保持不变
④已知该反应的平衡常数为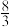 ,向某恒温恒容密闭容器中通入NO2、SO2、SO3、NO各1mol,此时v(正)
,向某恒温恒容密闭容器中通入NO2、SO2、SO3、NO各1mol,此时v(正)____ v(逆)(填“>”、“<”或“=”)。
(3)在发动机的高温下,空气中的N2和CO2可能发生:N2(g)+CO2(g) C(s)+2NO(g)。现向2L体积恒定的密闭容器中充入一定量N2和CO2来模拟此过程,其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
C(s)+2NO(g)。现向2L体积恒定的密闭容器中充入一定量N2和CO2来模拟此过程,其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。

①图中A点v正____ v逆(填“>”“<”或“=”)。
②第10min时,外界改变的条件可能是____ (填字母)。
A.加催化剂
B.增大C的物质的量
C.减小CO2的物质的量
D.升温
E.降温
(1)上述四种气体中直接排入空气时会引起酸雨的有
(2)回收大气污染物SO2的方法如下:
方法一:在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和液态H2O。已知:
CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(1) △H=-295.9kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-297.2kJ·mol-1
则CH4的燃烧热的热化学方程式为:
方法二:在恒容密闭容器中,用H2还原SO2生成S的反应分两步完成(如图1所示),该过程中部分物质的物质的量浓度随时间的变化关系如图2所示:

①由分析可知X为
②0~t1时间段的温度为
方法三:利用反应:NO2(g)+SO2(g)
 SO3(g)+NO(g)。
SO3(g)+NO(g)。③一定条件下,将NO2与SO2以体积比1∶1置于恒温恒容的密闭容器中发生反应:NO2(g)+SO2(g)
 SO3(g)+NO(g),能说明反应达到平衡状态的是
SO3(g)+NO(g),能说明反应达到平衡状态的是a.混合气体的密度保持不变
b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变
d.每生成1molSO3的同时消耗1molNO
e.容器内的混合气体平均相对分子质量保持不变
④已知该反应的平衡常数为
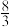 ,向某恒温恒容密闭容器中通入NO2、SO2、SO3、NO各1mol,此时v(正)
,向某恒温恒容密闭容器中通入NO2、SO2、SO3、NO各1mol,此时v(正)(3)在发动机的高温下,空气中的N2和CO2可能发生:N2(g)+CO2(g)
 C(s)+2NO(g)。现向2L体积恒定的密闭容器中充入一定量N2和CO2来模拟此过程,其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
C(s)+2NO(g)。现向2L体积恒定的密闭容器中充入一定量N2和CO2来模拟此过程,其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
①图中A点v正
②第10min时,外界改变的条件可能是
A.加催化剂
B.增大C的物质的量
C.减小CO2的物质的量
D.升温
E.降温
您最近一年使用:0次
2022-05-26更新
|
241次组卷
|
3卷引用:重庆市重庆实验外国语学校2021-2022学年高二上学期10月月考化学试题
4 . 化石燃料燃烧、硝酸工业废气处理不当及机动车辆尾气排放中的 、
、 进入大气后,在日光照射下分解成
进入大气后,在日光照射下分解成 和O时,即开始光化学烟雾的循环,不断地产生
和O时,即开始光化学烟雾的循环,不断地产生 ,光化学烟雾通常呈现淡蓝色其主要成分及简单形成机理如图所示。
,光化学烟雾通常呈现淡蓝色其主要成分及简单形成机理如图所示。

为预防和控制氮氧化物的污染,人们采取许多措施。可用氢氧化钠溶液对含氮氧化物的废气进行处理,氨气也可以用来处理氮氧化物。下列说法错误的是
 、
、 进入大气后,在日光照射下分解成
进入大气后,在日光照射下分解成 和O时,即开始光化学烟雾的循环,不断地产生
和O时,即开始光化学烟雾的循环,不断地产生 ,光化学烟雾通常呈现淡蓝色其主要成分及简单形成机理如图所示。
,光化学烟雾通常呈现淡蓝色其主要成分及简单形成机理如图所示。
为预防和控制氮氧化物的污染,人们采取许多措施。可用氢氧化钠溶液对含氮氧化物的废气进行处理,氨气也可以用来处理氮氧化物。下列说法错误的是
| A.光化学烟雾有强氧化性 | B.氮氧化物还可引发酸雨等污染问题 |
| C.光化学烟雾成分中含有烃和烃的衍生物 | D.光化学烟雾呈现淡蓝色是因为含有 |
您最近一年使用:0次
名校
5 . 环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中常含有的NOx、SO2、H2S等污染物,容易形成酸雨,破坏环境。其综合治理是当前重要的研究课题。
Ⅰ.以下是对酸雨的若干项评价,其中不正确的是__________
a.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.导致臭氧层空洞
d.二氧化碳的过量排放,是形成酸雨的主要原因之一
Ⅱ.电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。
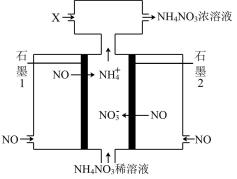
(1)电解NO制备NH4NO3原理如上方左图所示:
①阳极为石墨_____ (填1或2),该电极的反应式为_____________ 。
②为使电解的副产物也完全转化为NH4NO3,需要补充的物质X的化学式为___________ 。
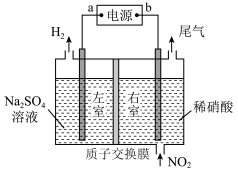
(2)用上方右图装置进行模拟电解NO2气体实验,可回收硝酸。
①外接电源a极为______ 极,左室发生的电极反应式为_____________ 。
②若有标准状况下2.24L NO2被吸收,通过质子交换膜(只允许质子通过)的H+为______ mol。
③用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中增加了1 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28L H2。原气体中NO和NO2的体积比为____________ 。
Ⅰ.以下是对酸雨的若干项评价,其中不正确的是
a.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.导致臭氧层空洞
d.二氧化碳的过量排放,是形成酸雨的主要原因之一
Ⅱ.电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。


(1)电解NO制备NH4NO3原理如上方左图所示:
①阳极为石墨
②为使电解的副产物也完全转化为NH4NO3,需要补充的物质X的化学式为
(2)用上方右图装置进行模拟电解NO2气体实验,可回收硝酸。
①外接电源a极为
②若有标准状况下2.24L NO2被吸收,通过质子交换膜(只允许质子通过)的H+为
③用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中增加了1 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28L H2。原气体中NO和NO2的体积比为
您最近一年使用:0次
11-12高二上·重庆·期中
6 . 为了降低硫氧化物造成的空气污染,可以在含硫的燃料中加入生石灰,这种方法称为“钙基固硫”,则燃料燃烧过程中的“固硫”反应为:
| A.CaO+2S = 2CaS + O2 | B.S + O2 = SO2 |
| C.CaO + SO2= CaSO3 | D.2CaO + 2SO2+ O2= 2CaSO4 |
您最近一年使用:0次



