1 . 下列反应的离子方程式正确的是
A.碘化亚铁溶液与等物质的量的氯气: |
B.向次氯酸钙溶液通入足量二氧化碳: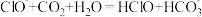 |
C.铜与稀硝酸: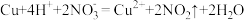 |
D.向硫化钠溶液通入足量二氧化硫: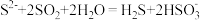 |
您最近一年使用:0次
2023-06-21更新
|
12166次组卷
|
21卷引用:安徽省淮南第二中学2024届高三上学期第四次段考化学试题
安徽省淮南第二中学2024届高三上学期第四次段考化学试题山东省烟台市莱州市第一中学2023-2024学年高一上学期1月月考化学试题江西省宜春市百树学校2023-2024学年高三上学期暑期阶段测试化学试卷四川省眉山市仁寿第一中学校(北校区)2023-2024学年高一下学期3月月考化学试题2023年高考浙江卷化学真题(6月)(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题6-10)(已下线)专题04 离子反应(已下线)专题04 离子反应(已下线)第2讲 离子反应和离子方程式(已下线)考点04 离子反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题04 离子方程式与离子共存-2023年高考化学真题题源解密(新高考专用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)吉林省长春外国语学校2023-2024学年高三上学期开学考试化学试题河南省南阳市第一中学校2023-2024学年高三上学期开学考试化学试题(已下线)选择题1-5福建省福州第四中学2023-2024学年高三上学期期中考试化学试题北京市中国人民大学附属中学2023-2024学年高三下学期开学考试化学试题(已下线)5.2.3硝酸和酸雨的防治课后作业提高篇天津市耀华中学2023-2024学年高三下学期开学验收考化学试卷四川省内江市第六中学2023-2024学年高三下学期入学考试理综试题-高中化学北京市第二中学2023-2024学年高三下学期三模化学试题
名校
解题方法
2 . 宏观辨识与微观探析是化学学科核心素养之一。下列物质的性质实验对应的反应方程式书写正确的是
A.硫酸亚铁溶液滴入酸性高锰酸钾溶液中: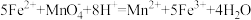 |
B.足量 通入氯化铝溶液中: 通入氯化铝溶液中: |
C.足量氯气通入碳酸钠溶液中: |
D. 通入 通入 溶液中: 溶液中: |
您最近一年使用:0次
2022-03-20更新
|
2508次组卷
|
11卷引用:湖南省常德市第一中学2022-2023学年高三下学期第六次月考化学试题
湖南省常德市第一中学2022-2023学年高三下学期第六次月考化学试题黑龙江省哈尔滨市第三中学校2023-2024学年高三上学期第二次验收考试化学试题广东省湛江市2022届高三下学期一模化学试题广东省肇庆市2022届高中毕业班下学期第三次教学质量检测化学试题河北省张家口市2022届高三第一次模拟考试化学试题(已下线)必刷卷01-2022年高考化学考前信息必刷卷(广东专用)(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2023年高考化学一轮复习考点微专题(已下线)化学(辽宁A卷)-学易金卷:2023年高考第一次模拟考试卷辽宁省葫芦岛市第一高级中学2022-2023学年高三上学期期末线上教学阶段检测化学试题(已下线)专题05 离子方程式正误判断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)辽宁省本溪市高级中学2023届高三下学期第一次摸底考试化学试题
名校
解题方法
3 . 探究硫及其化合物的性质,下列方案设计、现象和结论中有不正确的是
实验方案 | 现象 | 结论 | |
A | 在过硫化钠(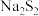 )中加入稀盐酸 )中加入稀盐酸 | 产生淡黄色沉淀和臭鸡蛋气味的气体。 | 发生歧化反应: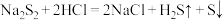 |
B | 已知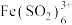 呈红棕色,将 呈红棕色,将 气体通入 气体通入 溶液中 溶液中 | 溶液先变为红棕色,过一段时间又变成浅绿色。 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大。 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大。 |
C | 燃着的镁条插入盛有 的集气瓶中。冷却后,往集气瓶中加入适量稀盐酸,静置,取少量上层清液于试管中,滴加少量 的集气瓶中。冷却后,往集气瓶中加入适量稀盐酸,静置,取少量上层清液于试管中,滴加少量 溶液。 溶液。 | 剧烈燃烧,集气瓶口有淡黄色固体附着,集气瓶底有白色固体生成。试管中没有产生黑色沉淀 | 镁能在 中燃烧: 中燃烧: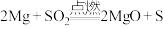 |
D | 探究电石与水的反应 | 将电石与饱和食盐水反应产生的气体通入酸性高锰酸钾溶液,观察现象 | 若酸性高锰酸钾溶液褪色,说明电石与水反应生成了乙炔 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-22更新
|
1899次组卷
|
6卷引用:浙江省天域全国名校协作体2022-2023学年高三下学期4月阶段性联考化学试题
浙江省天域全国名校协作体2022-2023学年高三下学期4月阶段性联考化学试题重庆市万州第二高级中学2023-2024学年高三上学期7月月考化学试题湖南省长沙市第一中学2023-2024学年高三上学期月考卷(三)化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)江西省抚州市乐安县第二中学2023-2024学年高三上学期11月期中化学试题2024年山东省潍坊市高三下学期高考模拟训练调研试题(二)
名校
4 . 实验室中为验证SO2的性质,将SO2分别通入溴水、品红溶液、硫化氢溶液、滴有酚酞的氢氧化钠溶液。下列说法错误的是
| A.溴水褪色,体现SO2的还原性 |
| B.品红溶液褪色,体现SO2的漂白性 |
| C.硫化氢溶液变浑浊,体现SO2的氧化性 |
| D.滴有酚酞的氢氧化钠溶液褪色,体现SO2的漂白性 |
您最近一年使用:0次
2024-02-25更新
|
1024次组卷
|
5卷引用:四川省德阳市什邡中学2023-2024学年高一下学期3月月考化学试题
四川省德阳市什邡中学2023-2024学年高一下学期3月月考化学试题辽宁省沈阳铁路实验中学2023-2024学年高一下学期4月月考化学试题河北省唐山市2023-2024学年高一上学期1月期末考试化学试题河北省石家庄市第四十二中学2023-2024年高一上学期期末考试化学试题(已下线)专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
5 . 下列实验操作、现象和结论(或解释)均正确的是
| 选项 | 操作 | 现象 | 结论(或解释) |
| A | 将水蒸气通过炽热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| B | 向Na2SiO3溶液中加入稀盐酸 | 产生白色沉淀 | 非金属性:Cl>Si |
| C | 向氢硫酸中通入SO2气体 | 产生淡黄色沉淀 | SO2具有氧化性 |
| D | 向盛有某溶液的试管中加入稀NaOH溶液,再将红色石蕊试纸靠近试管口 | 试纸不变蓝 | 该溶液中不含NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-02-26更新
|
1200次组卷
|
6卷引用:辽宁省锦州市黑山县第四高级中学2021-2022学年高三3月月考化学试题
辽宁省锦州市黑山县第四高级中学2021-2022学年高三3月月考化学试题广东省中山市第一中学2022-2023学年高一下学期6月月考化学试题广东省深圳市普通高中2022届高三下学期第一次调研考试化学试题(已下线)卷08 元素周期律-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)专项06 元素及其化合物-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)广东省汕尾市华大实验学校2021-2022学年高三下学期第二次周考化学试题
名校
6 . 探究 的性质,进行如下实验。
的性质,进行如下实验。
由上述实验所得 的性质及对应的解释
的性质及对应的解释不正确 的是
 的性质,进行如下实验。
的性质,进行如下实验。| 编号 | 实验装置 | 试剂a | 实验现象 |
| ① |
| 品红溶液 | 溶液褪色 |
| ② |  溶液 溶液 | 溶液变浑浊 | |
| ③ |  溶液 溶液 | 白色沉淀 | |
| ④ |  溶液 溶液 | 有气泡 |
 的性质及对应的解释
的性质及对应的解释A.实验①表明 具有漂白性 具有漂白性 |
B.实验②表明 具有氧化性 具有氧化性 |
| C.实验③产生的白色沉淀难溶于盐酸 |
D.实验④通入足量 发生反应的离子方程式为: 发生反应的离子方程式为: |
您最近一年使用:0次
2023-02-16更新
|
937次组卷
|
5卷引用:山西省大同市第一中学2022-2023学年高一下学期3月考试化学试题
名校
解题方法
7 . 下列有关实验的操作、现象和结论有错误的是
| 操作 | 现象 | 实验结论 | |
| A | 将SO2通入酸性KMnO4溶液 | 溶液褪色 | SO2具有还原性 |
| B | 将SO2通入H2S溶液 | 产生淡黄色沉淀 | SO2具有氧化性 |
| C | 向蔗糖中加入浓硫酸,将产生的气体通入溴水 | 蔗糖膨胀变黑,溴水褪色 | 浓硫酸具有脱水性和氧化性 |
| D | 将淀粉与稀硫酸混合加热后,加入少量新制Cu(OH)2,再加热 | 无砖红色沉淀生成 | 淀粉没有水解,或水解后没有葡萄糖生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-31更新
|
981次组卷
|
6卷引用:天津市宝坻区第一中学2022-2023学年高一下学期阶段练习四化学试题
名校
8 . 硫代硫酸钠(Na2S2O3)俗称海波,广泛应用于照相定影及纺织业等领域。某实验小组制备硫代硫酸钠并探究其性质。
Ⅰ:硫代硫酸钠的制备
实验小组设计如下装置制备硫代硫酸钠
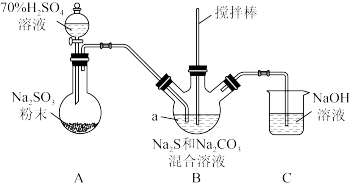
已知:①Na2CO3+2Na2S+4SO2=3Na2S2O3+CO2
②Na2S2O3中S元素的化合价分别为-2和+6
(1)仪器a的名称是___________ 。A中发生的化学反应方程式为___________ 。
(2)为了保证Na2S2O3的产量,实验中通入的SO2不能过量,需控制A中SO2的生成速率,采取的措施是___________ 。
Ⅱ:产品纯度的测定
①溶液配制:准确取该硫代硫酸钠样品2.0000g,配制成250mL溶液。
②滴定:向锥形瓶中加入20.00mL0.01mol·L-1KIO3溶液,加入过量KI溶液和H2SO4溶液,发生反应: +5I-+6H+=3I2+3H2O,然后加入淀粉作指示剂,用硫代硫酸钠样品溶液滴定,发生反应:I2+2
+5I-+6H+=3I2+3H2O,然后加入淀粉作指示剂,用硫代硫酸钠样品溶液滴定,发生反应:I2+2 =
= +2I-。
+2I-。
(3)滴定终点现象为________ ,消耗样品溶液的用量为25.00mL,则样品纯度为________ %(保留1位小数)
Ⅲ:硫代硫酸钠性质的探究
①取Na2S2O3晶体,溶解,配成0.2mol/L溶液。
②取4mL溶液,向其中加入1mL饱和氯水(pH=2.4),溶液立即出现浑浊,经检验浑浊物为S。
实验小组研究S产生的原因,提出了以下假设:
假设1:氧化剂氧化:Cl2、HClO等含氯的氧化性微粒氧化了-2价硫元素。
假设2:___________(不考虑空气中氧气氧化)。
设计实验方案:

(4)假设2是___________ 。
(5)第②组实验中胶头滴管加入的试剂是___________ 。
(6)依据现象,S产生的主要原因是___________ 。
Ⅰ:硫代硫酸钠的制备
实验小组设计如下装置制备硫代硫酸钠

已知:①Na2CO3+2Na2S+4SO2=3Na2S2O3+CO2
②Na2S2O3中S元素的化合价分别为-2和+6
(1)仪器a的名称是
(2)为了保证Na2S2O3的产量,实验中通入的SO2不能过量,需控制A中SO2的生成速率,采取的措施是
Ⅱ:产品纯度的测定
①溶液配制:准确取该硫代硫酸钠样品2.0000g,配制成250mL溶液。
②滴定:向锥形瓶中加入20.00mL0.01mol·L-1KIO3溶液,加入过量KI溶液和H2SO4溶液,发生反应:
 +5I-+6H+=3I2+3H2O,然后加入淀粉作指示剂,用硫代硫酸钠样品溶液滴定,发生反应:I2+2
+5I-+6H+=3I2+3H2O,然后加入淀粉作指示剂,用硫代硫酸钠样品溶液滴定,发生反应:I2+2 =
= +2I-。
+2I-。(3)滴定终点现象为
Ⅲ:硫代硫酸钠性质的探究
①取Na2S2O3晶体,溶解,配成0.2mol/L溶液。
②取4mL溶液,向其中加入1mL饱和氯水(pH=2.4),溶液立即出现浑浊,经检验浑浊物为S。
实验小组研究S产生的原因,提出了以下假设:
假设1:氧化剂氧化:Cl2、HClO等含氯的氧化性微粒氧化了-2价硫元素。
假设2:___________(不考虑空气中氧气氧化)。
设计实验方案:

| 胶头滴管 | 现象 | |
| 第①组 | 1mL饱和氯水 | 立即出现浑浊 |
| 第②组 | ___________ | 一段时间后出现浑浊,且浑浊度比①组小 |
(5)第②组实验中胶头滴管加入的试剂是
(6)依据现象,S产生的主要原因是
您最近一年使用:0次
2022-03-27更新
|
947次组卷
|
4卷引用:上海市复旦大学附属中学2023届高三阶段性练习化学试题
上海市复旦大学附属中学2023届高三阶段性练习化学试题四川省南充市2022届高三 适应性考试(二模)理综化学试题(已下线)化学-2022年高考考前押题密卷(广东卷)上海市复旦大学附属中学2023届高三下学期开学阶段性集中练习化学试题
名校
9 . 部分含硫物质中硫元素的价态与相应物质的类别的关系如图所示,下列有关说法不正确 的是


A.S在过量 中燃烧生成X 中燃烧生成X | B.V不可以用Z的浓溶液干燥。 |
| C.将V通入Y的溶液中可产生浑浊 | D.可实现W→Y→Z→W的循环转化 |
您最近一年使用:0次
2023-04-03更新
|
957次组卷
|
5卷引用:广东省江门市第二中学2022-2023学年高一下学期3月月考化学试题
广东省江门市第二中学2022-2023学年高一下学期3月月考化学试题(已下线)期中模拟题(二)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册) 江苏省无锡市梅村高级中学2022-2023学年高一下学期期中考试化学试题(已下线)第14讲 硫和二氧化硫-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)贵州省江口中学2022-2023学年高一下学期期中考试化学试卷
10 . 在实验室进行少量铁粉和硫粉混合加热的实验,将其产物又进行了系列实验,流程如下。下列说法正确的是
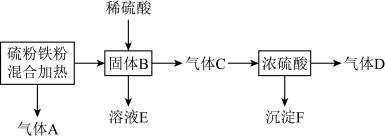

A.气体A和D含有 ,且均为氧化产物 ,且均为氧化产物 |
| B.上述过程中,硫元素共参加了2个氧化还原反应 |
| C.气体A、C混合也能生成固体F |
D.气体C与浓硫酸反应的化学方程式为: |
您最近一年使用:0次
2023-02-12更新
|
1302次组卷
|
4卷引用:江西省南昌市进贤县第一中学2022-2023学年高一下学期第一次月考化学试题




