名校
解题方法
1 . 衣食住行皆化学。下列物质在生活中的用途与其性质具有对应关系的是
| 选项 | 用途 | 性质 |
| A | 明矾净水 | 铝离子能够杀菌消毒 |
| B | 石英光纤用于通信 | 石英光纤传输光信号损耗低,带宽大,重量轻 |
| C | 氧化铝用于电解制取铝 | 氧化铝熔点高 |
| D | 茶叶常用于饼干类保鲜 | 茶叶酚具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-25更新
|
154次组卷
|
4卷引用:湖南省张家界市2023-2024学年高三上学期期末联考化学试题
解题方法
2 . 下列物质的用途与性质对应关系正确的是
| A.用SiO2制作光导纤维,是由于其硬度大、熔点高 |
| B.用FeCl3溶液刻蚀铜印刷线路板,是由于其有氧化性 |
| C.用铝质容器储运浓硫酸,是由于其常温下与浓硫酸不反应 |
| D.用NaHCO3作焙制糕点的膨松剂,是由于其能与碱反应 |
您最近一年使用:0次
3 . O3可将CN-转化为N2、CO2。单质Se是半导体材料,Se可通过SO2还原H2SeO3获得。下列物质性质与用途均正确且具有对应关系的是
| A.O3具有强氧化性,用于除去废水中CN- |
| B.SO2具有还原性,用于砂糖的脱色增白 |
| C.Se单质不溶于水,用于制作Se光电池 |
| D.浓硫酸具有吸水性,用于H2S气体的干燥剂 |
您最近一年使用:0次
4 . 性质决定用途,用途反映性质。下列物质的性质与用途不具有对应关系的是
| 选项 | 物质性质 | 用途 |
| A | 钠的熔点低,导热性好 | 液态钠用作核反应堆的传热介质 |
| B | 过氧化氢具有强氧化性 | 用于杀菌清毒 |
| C | 氢氟酸为弱酸 | 用于刻蚀玻璃 |
| D | 二氧化硅折射率,机械强度高 | 用作光导纤维 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-06更新
|
59次组卷
|
2卷引用:陕西省商洛市2022-2023学年高二下学期7月期末考试化学试题
5 . 物质的性质决定用途,下列对应关系不正确 的是
| A.二氧化硅的导电性介于导体和绝缘体之间,故常用于制造光导纤维 |
B.Ti-Fe合金能够大量吸收 ,并与 ,并与 结合成金属氢化物,故可用于做储氢合金 结合成金属氢化物,故可用于做储氢合金 |
| C.碳纳米管具有优良的电学性能,故可用于生产电池和传感器 |
| D.铝和氧化铝均能与酸、碱反应,故铝制餐具不宜用来长时间盛放酸性或碱性食物 |
您最近一年使用:0次
名校
解题方法
6 . 性质决定用途,下列物质的性质与用途正确且具有对应关系的是
| A.二氧化硫具有漂白性,可用于红酒杀菌消毒 |
| B.铁和浓硫酸常温下不反应,可以用铁罐盛装浓硫酸 |
| C.过氧化钠是淡黄色固体,在呼吸面具中用作供氧剂 |
| D.二氧化硅导光能力强,并且有硬度和柔韧度,可作光导纤维 |
您最近一年使用:0次
7 . 我国拟定于2022年底发射“爱因斯坦”探针卫星,首次填补时域天文观测和高能天体物理研究的国际空白。X射线主探器单体结构如图,下列有关物质的性质与用途不具有对应关系的是
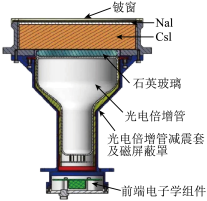

| A.金属铍有延展性,可作主探器的射线窗 |
| B.石英对光线全反射,可作光导材料 |
| C.SiO2属于原子晶体,可作耐高温材料 |
| D.NaI、CsI遇光易分解,作为闪烁体 |
您最近一年使用:0次
8 . 物质性质决定其用途,物质用途反映其性质。下列物质用途与性质对应关系不正确的是
| 选项 | 用途 | 性质 |
| A | SiO2用作光导纤维 | SiO2能把光的强弱转变为电流的强弱 |
| B | 工业上用纯碱去油污 | Na2CO3溶液水解呈碱性,油脂碱性条件下水解程度大 |
| C | 明矾用作净水剂 | 明矾溶于水形成Al(OH)3胶体,吸附水中悬浮杂质形成沉淀 |
| D | 三元催化器处理汽车尾气 | 尾气中CO有还原性,NOx有氧化性。在催化剂作用下转化为CO2和N2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。二氧化硅又称硅石,是制备硅及其化合物的重要原料,部分转化过程如图所示。回答下面问题:_______ (填字母)。
A.碳元素和硅元素都位于周期表的IVA族,非金属性较强的是碳元素
B.自然界中存在天然游离的硅单质
C.玻璃、水泥、陶瓷都是传统的硅酸盐产品
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.硅元素在金属与非金属的分界线处,因此具弱导电性,一般可用作半导体材料
(2)光导纤维是一种良好的通讯材料,其成分是_______ (填化学式,下同),高纯硅是制造半导体芯片的基础原材料,由SiO2制备高纯度硅的工业流程如上图所示,可以循环使用的物质为_______ 和_______ ,写出第①步的化学方程式_______ 。
(3)生产磨砂玻璃时可以用HF溶蚀玻璃,是因为HF溶液可与SiO2反应,其化学反应方程式为_______ 。
(4)氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。
①根据氮和硅的原子结构示意图、元素周期律的知识,写出氮化硅的化学式_______ 。
②根据以上描述,推测氮化硅可能有哪些用途:_______ (填字母)。
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具

A.碳元素和硅元素都位于周期表的IVA族,非金属性较强的是碳元素
B.自然界中存在天然游离的硅单质
C.玻璃、水泥、陶瓷都是传统的硅酸盐产品
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.硅元素在金属与非金属的分界线处,因此具弱导电性,一般可用作半导体材料
(2)光导纤维是一种良好的通讯材料,其成分是
(3)生产磨砂玻璃时可以用HF溶蚀玻璃,是因为HF溶液可与SiO2反应,其化学反应方程式为
(4)氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。
①根据氮和硅的原子结构示意图、元素周期律的知识,写出氮化硅的化学式
②根据以上描述,推测氮化硅可能有哪些用途:
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
您最近一年使用:0次
10 . 硅及其化合物在现代高科技材料中占有重要位置,广泛应用于航空航天测控、光纤通讯等领域。
(1)实验室盛放NaOH溶液的试剂瓶不能用玻璃塞,请用离子方程式解释原因___________ 。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是___________ (填化学式,下同)。
(3)“玉兔号”月球车帆板太阳能电池的材料是___________ 。
(4)氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述,推测氮化硅可能有哪些用途:___________ (填字母)。
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
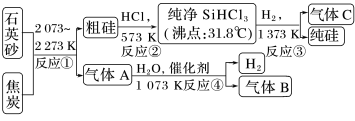
(5)如图所示流程是工业上制取纯硅的一种方法。___________ 。
(1)实验室盛放NaOH溶液的试剂瓶不能用玻璃塞,请用离子方程式解释原因
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是
(3)“玉兔号”月球车帆板太阳能电池的材料是
(4)氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述,推测氮化硅可能有哪些用途:
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
(5)如图所示流程是工业上制取纯硅的一种方法。
您最近一年使用:0次



