名校
解题方法
1 . 硅及其化合物在生产生活中有重要用途。
(1)用氮化硅 陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为
陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为 。
。
① 的电子式为
的电子式为___________ 。
②若该反应转移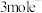 ,生成
,生成 的质量为
的质量为___________ g。
(2)芯片制作中的部分流程如图: 溶液与单晶硅反应生成
溶液与单晶硅反应生成 溶液,
溶液, 溶液俗称水玻璃,水玻璃可用作
溶液俗称水玻璃,水玻璃可用作___________ 。
②扩散制结过程发生反应I. ;反应Ⅱ.
;反应Ⅱ.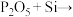
 。
。
配平反应Ⅱ.___________ 
___________ Si=___________ SiO2+___________ P,该反应的反应类型为___________ (填四大基本反应类型)。
③去除磷硅玻璃即除去扩散制结过程中产生的 ,下列试剂合适的为
,下列试剂合适的为___________ (填标号),写出其化学方程式:___________ 。
a.浓硫酸 b.氢氟酸 c.稀硝酸
(1)用氮化硅
 陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为
陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为 。
。①
 的电子式为
的电子式为②若该反应转移
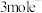 ,生成
,生成 的质量为
的质量为(2)芯片制作中的部分流程如图:

 溶液与单晶硅反应生成
溶液与单晶硅反应生成 溶液,
溶液, 溶液俗称水玻璃,水玻璃可用作
溶液俗称水玻璃,水玻璃可用作②扩散制结过程发生反应I.
 ;反应Ⅱ.
;反应Ⅱ.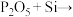
 。
。配平反应Ⅱ.

③去除磷硅玻璃即除去扩散制结过程中产生的
 ,下列试剂合适的为
,下列试剂合适的为a.浓硫酸 b.氢氟酸 c.稀硝酸
您最近半年使用:0次
2024-04-28更新
|
41次组卷
|
2卷引用:辽宁省部分高中2023-2024学年高一下学期4月月考化学试题
2021高三·全国·专题练习
解题方法
2 . 化合物 A 由三种短周期元素组成,某兴趣小组进行了如下实验:
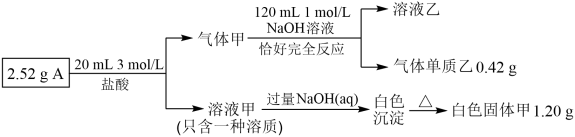
已知:气体甲为纯净物且只含两种元素,在标况下体积为 672 mL;固体甲为常用的耐火材料,溶液乙为建筑行业中常用的粘合剂。请回答下列问题:
(1)A 的组成元素为___________ (用元素符号表示),A 的化学式为___________ ;
(2)写出A溶于盐酸的化学方程式___________ 。
(3)写出气体甲与 NaOH(aq)反应的离子方程式___________ 。
(4)往溶液乙中通入少量 CO2气体发生的化学方程式___________ 。
(5)高温下A 与足量氯气能发生剧烈爆炸,生成三种常见化合物,试写出相应的化学方程式___________ 。

已知:气体甲为纯净物且只含两种元素,在标况下体积为 672 mL;固体甲为常用的耐火材料,溶液乙为建筑行业中常用的粘合剂。请回答下列问题:
(1)A 的组成元素为
(2)写出A溶于盐酸的化学方程式
(3)写出气体甲与 NaOH(aq)反应的离子方程式
(4)往溶液乙中通入少量 CO2气体发生的化学方程式
(5)高温下A 与足量氯气能发生剧烈爆炸,生成三种常见化合物,试写出相应的化学方程式
您最近半年使用:0次
20-21高一下·浙江·阶段练习
3 . 化合物X由三种短周期元素组成,为探究其组成和性质,设计完成如下实验:

已知:a.气体A是相对分子质量最小的气体,可作为新能源;
b.固体C是白色胶状沉淀,溶液D可用作黏合剂和防火剂;
c.反应③恰好消耗0.02 mol NaOH
请回答下列问题:
(1)X的组成元素为Cl和___________ (用元素符号表示)。
(2)写出反应①的化学方程式___________ 。
(3)检验溶液D中所含溶质的金属阳离子的实验方法是:___________ 。

已知:a.气体A是相对分子质量最小的气体,可作为新能源;
b.固体C是白色胶状沉淀,溶液D可用作黏合剂和防火剂;
c.反应③恰好消耗0.02 mol NaOH
请回答下列问题:
(1)X的组成元素为Cl和
(2)写出反应①的化学方程式
(3)检验溶液D中所含溶质的金属阳离子的实验方法是:
您最近半年使用:0次
名校
解题方法
4 . 已知C为二元化合物,为了确定C的组成,进行了以下的探究过程。已知F、G都是难溶于水和稀硝酸的白色沉淀,I可用于制造光导纤维或制造玻璃。有关生产过程如图:
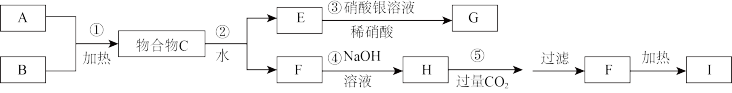
按要求回答下列问题:
(1)写出I制造玻璃的两个主要化学方程式的任意一个_______ 。普通玻璃的化学式可表示为CaNa2Si6O14,用氧化物的形式可表示为_______ 。
(2)C的化学式为_______ ;H的一种用途是_______ 。
(3)写出反应⑤的离子方程式_______ 。
写出反应①的化学方程式_______ 。

按要求回答下列问题:
(1)写出I制造玻璃的两个主要化学方程式的任意一个
(2)C的化学式为
(3)写出反应⑤的离子方程式
写出反应①的化学方程式
您最近半年使用:0次
名校
5 . 化合物 A 由三种短周期元素组成,某兴趣小组进行了如下实验:
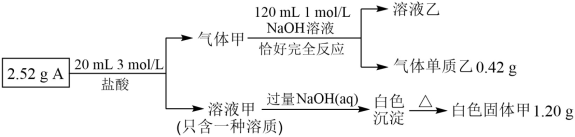
已知:气体甲为纯净物且只含两种元素,在标况下体积为 672 mL;固体甲为常用的耐火材料,溶液乙为建筑行业中常用的粘合剂。请回答下列问题:
(1)A 的组成元素为_____ (用元素符号表示),A 的化学式为_____ ;
(2)写出气体甲与 NaOH(aq)反应的离子方程式_____
(3)往溶液乙中通入少量 CO2气体发生的化学方程式_____ ;
(4)高温下A 与足量氯气能发生剧烈爆炸,生成三种常见化合物,试写出相应的化学方程式_____ 。

已知:气体甲为纯净物且只含两种元素,在标况下体积为 672 mL;固体甲为常用的耐火材料,溶液乙为建筑行业中常用的粘合剂。请回答下列问题:
(1)A 的组成元素为
(2)写出气体甲与 NaOH(aq)反应的离子方程式
(3)往溶液乙中通入少量 CO2气体发生的化学方程式
(4)高温下A 与足量氯气能发生剧烈爆炸,生成三种常见化合物,试写出相应的化学方程式
您最近半年使用:0次
6 . 硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
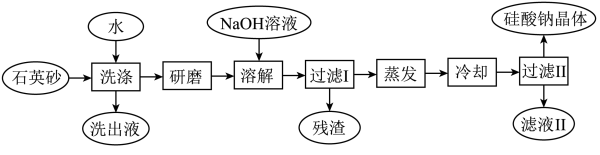
(1)要将洗出液中的溶质析出,采用的方法是_________ 。
A.蒸发结晶 B.冷却结晶
C.先蒸发,再冷却结晶 D.先冷却,再蒸发结晶
(2)在以上流程中,要将洗净的石英砂研磨成粉末,目的是_____________________________ 。
(3)蒸发时用到的硅酸盐仪器有____________________________________________________ 。
(4)上述流程中加入NaOH溶液,反应的离子方程式是_______________________________ 。
(5)硅酸钠溶液呈____ 性,硅酸钠的用途很广,其中的一种用途是_______________________ 。
(6)将用上流程中的残渣来焊接铁轨,反应的化学方程式是___________________ 。

(1)要将洗出液中的溶质析出,采用的方法是
A.蒸发结晶 B.冷却结晶
C.先蒸发,再冷却结晶 D.先冷却,再蒸发结晶
(2)在以上流程中,要将洗净的石英砂研磨成粉末,目的是
(3)蒸发时用到的硅酸盐仪器有
(4)上述流程中加入NaOH溶液,反应的离子方程式是
(5)硅酸钠溶液呈
(6)将用上流程中的残渣来焊接铁轨,反应的化学方程式是
您最近半年使用:0次
名校
7 . 钇的常见化合价为+3价,我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇。
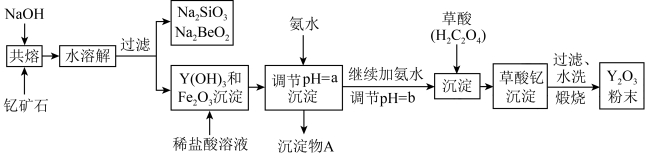
已知:①该流程中有关金属离子形成氢氧化物沉淀时的pH见下表:
②在元素周期表中,铍元素和铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)写出Na2SiO3的一种用途________________________ 。
(2)若改用氧化物的形式表示Y2FeBe2Si2O10组成,则化学式为__________ 。
(3)根据元素周期表的知识判断,常温下,氯化锶溶液pH____ 7(填“大于”、“等于”或“小于”);写出氯化锶的电子式:______________________ 。
(4)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。
① 最好选用盐酸和_______ 两种试剂,再通过必要的操作即可实现。
A.NaOH溶液 B.氨水 C.CO2 D.HNO3
② 写出Na2BeO2与足量盐酸发生反应的离子方程式___________________________ 。
(5)为使Fe3+沉淀完全,用氨水调节pH=a时,a应控制在_________ 范围内;继续加氨水调节pH =b发生反应的离子方程式为____________________________ ;检验Fe3+是否沉淀完全的操作方法是:___________________________________ 。
(6)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O]煅烧的化学方程式___________________________________ 。

已知:①该流程中有关金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.0 | 8.2 |
(1)写出Na2SiO3的一种用途
(2)若改用氧化物的形式表示Y2FeBe2Si2O10组成,则化学式为
(3)根据元素周期表的知识判断,常温下,氯化锶溶液pH
(4)欲从Na2SiO3和Na2BeO2混合溶液中制得Be(OH)2沉淀。
① 最好选用盐酸和
A.NaOH溶液 B.氨水 C.CO2 D.HNO3
② 写出Na2BeO2与足量盐酸发生反应的离子方程式
(5)为使Fe3+沉淀完全,用氨水调节pH=a时,a应控制在
(6)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O]煅烧的化学方程式
您最近半年使用:0次
9-10高一下·广东广州·期末
解题方法
8 . 实验对认识和研究物质性质有重要作用,回答下列相应问题。
(一)为证明Na2SiO3具有防火性能,同时做以下两个实验。
实验①:取一小木条,放入蒸馏水中,使之充分吸湿、浸透,取出稍沥干(不再滴液)后,放置在酒精灯外焰处。
实验②:另取一个相同的小木条,放入Na2SiO3饱和溶液中,之后重复实验①的操作。
(1)设计实验①的目的是________________________ 。
(二)性质实验中反应原理常用化学方程式表示。请用化学方程式各举一例,说明下列物质所具有的性质。
(2)SO2具有还原性_________________________ 。
(3)SO2具有酸性氧化物共同的性质_______________ 。
(4)浓硫酸具有强氧化性_____________________ 。
(一)为证明Na2SiO3具有防火性能,同时做以下两个实验。
实验①:取一小木条,放入蒸馏水中,使之充分吸湿、浸透,取出稍沥干(不再滴液)后,放置在酒精灯外焰处。
实验②:另取一个相同的小木条,放入Na2SiO3饱和溶液中,之后重复实验①的操作。
(1)设计实验①的目的是
(二)性质实验中反应原理常用化学方程式表示。请用化学方程式各举一例,说明下列物质所具有的性质。
(2)SO2具有还原性
(3)SO2具有酸性氧化物共同的性质
(4)浓硫酸具有强氧化性
您最近半年使用:0次



