名校
1 . 完成下面有关计算,并在空白处填写结果。
(1)若将0.6mol钠、铁、铝分别投入100mL1mol·L-1盐酸中,在标准状况下,产生氢气的体积之比是___ 。
(2)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为___ ,需要二者的固体质量之比为___ 。
(3)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL0.5mol/LFeSO4溶液和5.2g固体沉淀物。则反应后生成铜的质量为___ ,原Fe2(SO4)3溶液的物质的量浓度为____ 。
(1)若将0.6mol钠、铁、铝分别投入100mL1mol·L-1盐酸中,在标准状况下,产生氢气的体积之比是
(2)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为
(3)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL0.5mol/LFeSO4溶液和5.2g固体沉淀物。则反应后生成铜的质量为
您最近一年使用:0次
解题方法
2 . 含钠化合物与含硫化合物可发生多种反应,请回答下列问题:
(1)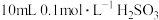 溶液与6.9gNa反应,生成的H2在标准状况下的体积为
溶液与6.9gNa反应,生成的H2在标准状况下的体积为___ L。
(2)SO2与少量NaOH溶液反应的离子方程式为___ 。
(3)查阅资料知Na2O2具有强氧化性,Na2O2与SO2反应的化学方程式为____ 。
(4)用热的NaOH溶液与硫粉反应中,氧化剂与还原剂的质量之比为___ ,当转移0.4mol电子时,生成Na2S的质量为___ g。
(1)
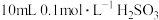 溶液与6.9gNa反应,生成的H2在标准状况下的体积为
溶液与6.9gNa反应,生成的H2在标准状况下的体积为(2)SO2与少量NaOH溶液反应的离子方程式为
(3)查阅资料知Na2O2具有强氧化性,Na2O2与SO2反应的化学方程式为
(4)用热的NaOH溶液与硫粉反应中,氧化剂与还原剂的质量之比为
您最近一年使用:0次
名校
3 . 有一块表面被氧化成Na2O的金属钠,质量5.22g,将其投入100g水中,完全反应后,收集到标准状况下的氢气体积为2.24L。
(1)写出有关反应方程式:________________________ 、_________________________
(2)求金属钠和氧化钠的质量分别是多少_______ ?
(1)写出有关反应方程式:
(2)求金属钠和氧化钠的质量分别是多少
您最近一年使用:0次



