名校
解题方法
1 . Ⅰ.汉弗里·戴维是英国著名化学家,他提出:“电流与化合物的相互作用,是最有可能将所有物质分解为元素的方法”。通过这种方法,他制备得到了金属钾和钠。
(1)戴维在1807年用电解熔融烧碱的方法制得金属钠,电极之间设置镍网做隔膜以分离电解产物,电解的总反应方程式为:___________ 。
(2)关于金属钠,下列叙述正确的是___________
(3)钠在空气中燃烧产物的颜色是___________ , 电子式为___________ 。
(4)ag钠完全燃烧后,将固体充分溶解在bg水中,所得溶液溶质的质量分数是___________ 。
(5)某实验小组把 CO2通入饱和Na2CO3溶液制取NaHCO3,装置如下图所示(气密性已检验,部分夹持装置略):
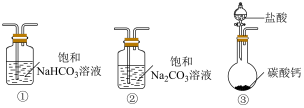
选取必要的实验装置,正确的连接顺序为___________ (填序号)。
Ⅱ.为确定制得的固体样品是纯净的 NaHCO3小组同学提出下列实验方案:
甲方案:将样品溶液与BaCl2溶液反应,观察现象
乙方案:测定 pH法
(6)为判定甲方案的可行性, 某同学用NaHCO3分析纯配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下:
此实验说明甲方案___________ (填“可行”或“不可行”)。
(7)产生浑浊(伴有气体产生)的离子方程式:___________ 。
(8)乙方案是:取等质量的固体样品和分析纯 Na2CO3加等质量的水配制的溶液,分别与 pH 计测定 pH,pH更大的是___________ (填化学式)。
(1)戴维在1807年用电解熔融烧碱的方法制得金属钠,电极之间设置镍网做隔膜以分离电解产物,电解的总反应方程式为:
(2)关于金属钠,下列叙述正确的是___________
| A.钠可保存在煤油或CCl4等液态有机物中 |
| B.氯化钠在电流作用下电离出的钠离子和氯离子 |
| C.钠与硫在常温下化合就能剧烈反应,甚至发生爆炸 |
| D.若金属钠着火,可采用干粉灭火器灭火 |
(3)钠在空气中燃烧产物的颜色是
(4)ag钠完全燃烧后,将固体充分溶解在bg水中,所得溶液溶质的质量分数是
(5)某实验小组把 CO2通入饱和Na2CO3溶液制取NaHCO3,装置如下图所示(气密性已检验,部分夹持装置略):

选取必要的实验装置,正确的连接顺序为
Ⅱ.为确定制得的固体样品是纯净的 NaHCO3小组同学提出下列实验方案:
甲方案:将样品溶液与BaCl2溶液反应,观察现象
乙方案:测定 pH法
(6)为判定甲方案的可行性, 某同学用NaHCO3分析纯配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下:
NaHCO3溶液 BaCl2溶液 | 0.2mol/L | 0.1mol/L | 0.02mol/L |
| 0.2mol/L | 浑浊 | 浑浊 | 少许浑浊 |
| 0.1mol/L | 浑浊 | 少许浑浊 | 无现象 |
| 0.02mol/L | 少许浑浊 | 无现象 | 无现象 |
(7)产生浑浊(伴有气体产生)的离子方程式:
(8)乙方案是:取等质量的固体样品和分析纯 Na2CO3加等质量的水配制的溶液,分别与 pH 计测定 pH,pH更大的是
您最近一年使用:0次
名校
2 . Ⅰ.探究金属钠与水反应实验过程中,某课外小组同学记录了如下实验现象和实验结论:
①有碱生成;②溶液变红;③钠四处游动;④钠浮在水面上;⑤有气体产生;⑥钠的密度比水小;⑦钠熔成光亮的小球;⑧反应放热,钠熔点低。
(1)请填写下表中的空格(从①~⑧中选择,填序号):
(2)写出钠与水反应的离子方程式:________ 。
Ⅱ.某课外活动小组设计下列装置,验证二氧化碳跟过氧化钠反应时,需要与水接触。
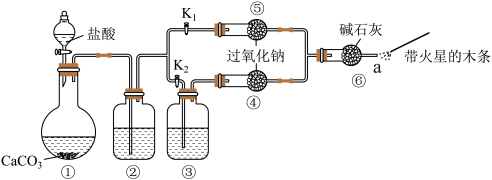
【装置分析】
(3)装置①中反应的离子方程式是________ 。
(4)已知盐酸具有挥发性。装置②中的试剂是________ ,②中反应的离子方程式是________ 。
(5)装置③中的试剂是________ 。
【进行实验】
步骤1:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
(6)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是________ 、________ 。
(7)写出过氧化钠跟二氧化碳反应的化学方程式并标出反应过程中的电子转移方向和数目:________ 。
Ⅲ.欲探究 和
和 稳定性的相对强弱,两同学分别设计以下两组装置:
稳定性的相对强弱,两同学分别设计以下两组装置:
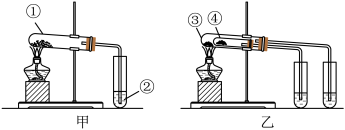
(8)如甲图所示,分别用 和
和 做实验,试管②中的试剂是
做实验,试管②中的试剂是________ 。试管①中发生反应的化学方程式是________ 。
(9)如乙图所示,试管④中装入的固体应该是________ (填化学式)。
(10)通过上述实验,得出的结论是; 比
比 的稳定性
的稳定性________ (填“强”或“弱”)。
(11)向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的 后,均稀释至100mL。向稀释后的溶液中,逐滴滴加0.1mol/L盐酸,产生
后,均稀释至100mL。向稀释后的溶液中,逐滴滴加0.1mol/L盐酸,产生 的体积(已折合至标准状况)与所加盐酸的体积关系如图所示。
的体积(已折合至标准状况)与所加盐酸的体积关系如图所示。
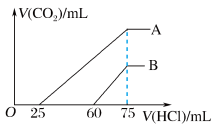
①A曲线表明,原溶液通入 后,所得溶质与盐酸反应产生
后,所得溶质与盐酸反应产生 的最大体积为
的最大体积为________ mL(标准状况)。
②B曲线表明,原溶液通入 后,所得溶液中溶质的化学式为
后,所得溶液中溶质的化学式为________ 。
③原NaOH溶液的物质的量浓度为________ 。
①有碱生成;②溶液变红;③钠四处游动;④钠浮在水面上;⑤有气体产生;⑥钠的密度比水小;⑦钠熔成光亮的小球;⑧反应放热,钠熔点低。
(1)请填写下表中的空格(从①~⑧中选择,填序号):
实验现象 | ⑦ | ③ | ||
实验结论 | ⑥ | ① |
Ⅱ.某课外活动小组设计下列装置,验证二氧化碳跟过氧化钠反应时,需要与水接触。

【装置分析】
(3)装置①中反应的离子方程式是
(4)已知盐酸具有挥发性。装置②中的试剂是
(5)装置③中的试剂是
【进行实验】
步骤1:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。步骤2:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。(6)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是
(7)写出过氧化钠跟二氧化碳反应的化学方程式并标出反应过程中的电子转移方向和数目:
Ⅲ.欲探究
 和
和 稳定性的相对强弱,两同学分别设计以下两组装置:
稳定性的相对强弱,两同学分别设计以下两组装置:
(8)如甲图所示,分别用
 和
和 做实验,试管②中的试剂是
做实验,试管②中的试剂是(9)如乙图所示,试管④中装入的固体应该是
(10)通过上述实验,得出的结论是;
 比
比 的稳定性
的稳定性(11)向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的
 后,均稀释至100mL。向稀释后的溶液中,逐滴滴加0.1mol/L盐酸,产生
后,均稀释至100mL。向稀释后的溶液中,逐滴滴加0.1mol/L盐酸,产生 的体积(已折合至标准状况)与所加盐酸的体积关系如图所示。
的体积(已折合至标准状况)与所加盐酸的体积关系如图所示。
①A曲线表明,原溶液通入
 后,所得溶质与盐酸反应产生
后,所得溶质与盐酸反应产生 的最大体积为
的最大体积为②B曲线表明,原溶液通入
 后,所得溶液中溶质的化学式为
后,所得溶液中溶质的化学式为③原NaOH溶液的物质的量浓度为
您最近一年使用:0次



