解题方法
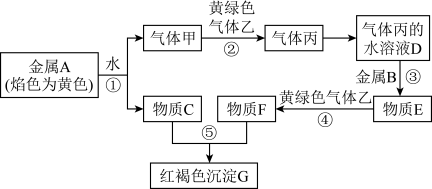
1 . 现有金属单质 A、B 和气体甲、乙、丙及物质 C、D、E、F、G,它们之间能发生如图反应(图中某些反应的产物及条件没有全部标出)。___________ ,氧化产物和还原产物的物质的量之比为 ___________ 。
(2)写出反应④的离子方程式___________ ,该反应证明 E 中的阳离子有___________ (填“氧化性”或“还原性”)。
(3)F 溶液常用于腐蚀覆铜印刷电路板,请写出相关的离子方程式___________ 。腐蚀结束后,通过以下两步可分离出铜,并实现 F 溶液再生:“试剂 a”和“操作”分别为 ___________ 、___________ 。
(2)写出反应④的离子方程式
(3)F 溶液常用于腐蚀覆铜印刷电路板,请写出相关的离子方程式

您最近一年使用:0次
名校
解题方法
2 . 据题目要求完成下列各题:
(1)写出氯气溶于水的离子反应方程式___________ 。
(2)将4.6g金属钠投入到足量水中,得ag溶液;将4.8g金属镁投入到足量盐酸中,得bg溶液,假设水的质量与盐酸的质量相等,则反应后两溶液的质量关系式为a___________ b(填>、<、=)。
(3) 在碱性溶液中可被NaClO氧化为
在碱性溶液中可被NaClO氧化为 ,而NaClO被还原为NaCl。若反应中
,而NaClO被还原为NaCl。若反应中 与NaClO的物质的量之比为1:13,则x的值为
与NaClO的物质的量之比为1:13,则x的值为___________ 。
(4) 离子在一定条件下可以把
离子在一定条件下可以把 离子氧化,若反应后
离子氧化,若反应后 离子变为
离子变为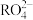 离子,又知反应中氧化剂和还原剂的物质的量之比为5:2,
离子,又知反应中氧化剂和还原剂的物质的量之比为5:2, 离子被氧化后的化合价为
离子被氧化后的化合价为___________ 。
(5)已知爆炸时硝酸铵按下式分解: 。则该反应中被氧化和被还原的N原子数之比为
。则该反应中被氧化和被还原的N原子数之比为___________ 。
(6)高铁酸钠( )是高效的饮用水处理剂,可在碱性溶液环境下由NaClO溶液氧化
)是高效的饮用水处理剂,可在碱性溶液环境下由NaClO溶液氧化 制得。
制得。
①请配平以下化学反应方程式,并用单线桥标出电子转移的方向和数目:________

②每转移3mol电子,生成 的物质的量为
的物质的量为___________ mol。
(1)写出氯气溶于水的离子反应方程式
(2)将4.6g金属钠投入到足量水中,得ag溶液;将4.8g金属镁投入到足量盐酸中,得bg溶液,假设水的质量与盐酸的质量相等,则反应后两溶液的质量关系式为a
(3)
 在碱性溶液中可被NaClO氧化为
在碱性溶液中可被NaClO氧化为 ,而NaClO被还原为NaCl。若反应中
,而NaClO被还原为NaCl。若反应中 与NaClO的物质的量之比为1:13,则x的值为
与NaClO的物质的量之比为1:13,则x的值为(4)
 离子在一定条件下可以把
离子在一定条件下可以把 离子氧化,若反应后
离子氧化,若反应后 离子变为
离子变为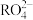 离子,又知反应中氧化剂和还原剂的物质的量之比为5:2,
离子,又知反应中氧化剂和还原剂的物质的量之比为5:2, 离子被氧化后的化合价为
离子被氧化后的化合价为(5)已知爆炸时硝酸铵按下式分解:
 。则该反应中被氧化和被还原的N原子数之比为
。则该反应中被氧化和被还原的N原子数之比为(6)高铁酸钠(
 )是高效的饮用水处理剂,可在碱性溶液环境下由NaClO溶液氧化
)是高效的饮用水处理剂,可在碱性溶液环境下由NaClO溶液氧化 制得。
制得。①请配平以下化学反应方程式,并用单线桥标出电子转移的方向和数目:

②每转移3mol电子,生成
 的物质的量为
的物质的量为
您最近一年使用:0次
2023-11-29更新
|
328次组卷
|
2卷引用:河南省开封市五县联考2023-2024学年高一上学期12月月考化学试题
名校
解题方法
3 . 为了研究钠的性质,在实验室里做了如下实验:
(1)将一小块钠投入 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为_______ 。
(2)为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为ag,将质量为bg的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为cg。

①列出计算钠相对原子质量的数学表达式_______ (用含有a、b、c的算式表示)。
②无水氯化钙的作用是_______ 。若不用无水氯化钙,求出的钠的相对原子质量的实际数值是偏大还是偏小?_______ 。
(3)现有一块部分被氧化为氧化钠的钠块,其质量为10.8g,将它投入一定量的水中完全反应,最终得到含16g溶质的氢氧化钠溶液,回答下列问题:
①反应中生成的氢气为_______ mol。
②钠的质量为_______ g。
(1)将一小块钠投入
 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为(2)为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为ag,将质量为bg的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为cg。

①列出计算钠相对原子质量的数学表达式
②无水氯化钙的作用是
(3)现有一块部分被氧化为氧化钠的钠块,其质量为10.8g,将它投入一定量的水中完全反应,最终得到含16g溶质的氢氧化钠溶液,回答下列问题:
①反应中生成的氢气为
②钠的质量为
您最近一年使用:0次
名校
解题方法
4 . 金属钠与下列溶液反应时,既有白色沉淀析出又有气体逸出的是
| A.BaCl2溶液 | B.CuSO4溶液 | C.稀H2SO4溶液 | D.MgCl2溶液 |
您最近一年使用:0次
2023-01-11更新
|
595次组卷
|
4卷引用:河南省洛阳市洛宁县第一高级中学2023-2024学年高三上学期第一次月考化学试题
河南省洛阳市洛宁县第一高级中学2023-2024学年高三上学期第一次月考化学试题江苏省靖江高级中学2022-2023学年高一上学期期末调研测试化学试题河北省石家庄市2023-2024学年高一上学期第二次月考化学试题(已下线)专题05 金属钠及钠的化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)



