据题目要求完成下列各题:
(1)写出氯气溶于水的离子反应方程式___________ 。
(2)将4.6g金属钠投入到足量水中,得ag溶液;将4.8g金属镁投入到足量盐酸中,得bg溶液,假设水的质量与盐酸的质量相等,则反应后两溶液的质量关系式为a___________ b(填>、<、=)。
(3) 在碱性溶液中可被NaClO氧化为
在碱性溶液中可被NaClO氧化为 ,而NaClO被还原为NaCl。若反应中
,而NaClO被还原为NaCl。若反应中 与NaClO的物质的量之比为1:13,则x的值为
与NaClO的物质的量之比为1:13,则x的值为___________ 。
(4) 离子在一定条件下可以把
离子在一定条件下可以把 离子氧化,若反应后
离子氧化,若反应后 离子变为
离子变为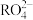 离子,又知反应中氧化剂和还原剂的物质的量之比为5:2,
离子,又知反应中氧化剂和还原剂的物质的量之比为5:2, 离子被氧化后的化合价为
离子被氧化后的化合价为___________ 。
(5)已知爆炸时硝酸铵按下式分解: 。则该反应中被氧化和被还原的N原子数之比为
。则该反应中被氧化和被还原的N原子数之比为___________ 。
(6)高铁酸钠( )是高效的饮用水处理剂,可在碱性溶液环境下由NaClO溶液氧化
)是高效的饮用水处理剂,可在碱性溶液环境下由NaClO溶液氧化 制得。
制得。
①请配平以下化学反应方程式,并用单线桥标出电子转移的方向和数目:________

②每转移3mol电子,生成 的物质的量为
的物质的量为___________ mol。
(1)写出氯气溶于水的离子反应方程式
(2)将4.6g金属钠投入到足量水中,得ag溶液;将4.8g金属镁投入到足量盐酸中,得bg溶液,假设水的质量与盐酸的质量相等,则反应后两溶液的质量关系式为a
(3)
 在碱性溶液中可被NaClO氧化为
在碱性溶液中可被NaClO氧化为 ,而NaClO被还原为NaCl。若反应中
,而NaClO被还原为NaCl。若反应中 与NaClO的物质的量之比为1:13,则x的值为
与NaClO的物质的量之比为1:13,则x的值为(4)
 离子在一定条件下可以把
离子在一定条件下可以把 离子氧化,若反应后
离子氧化,若反应后 离子变为
离子变为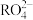 离子,又知反应中氧化剂和还原剂的物质的量之比为5:2,
离子,又知反应中氧化剂和还原剂的物质的量之比为5:2, 离子被氧化后的化合价为
离子被氧化后的化合价为(5)已知爆炸时硝酸铵按下式分解:
 。则该反应中被氧化和被还原的N原子数之比为
。则该反应中被氧化和被还原的N原子数之比为(6)高铁酸钠(
 )是高效的饮用水处理剂,可在碱性溶液环境下由NaClO溶液氧化
)是高效的饮用水处理剂,可在碱性溶液环境下由NaClO溶液氧化 制得。
制得。①请配平以下化学反应方程式,并用单线桥标出电子转移的方向和数目:

②每转移3mol电子,生成
 的物质的量为
的物质的量为
更新时间:2023-11-29 19:06:14
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:_____ ,若是改加氢氧化钡溶液至中性,离子反应方程式为:______ 。
(2)向1L 1mol/L的NH4Al(SO4)2溶液中滴加2.25L 等浓度的Ba(OH)2溶液,离子反应方程式为:__ 。
(3)向含FeI2和FeBr2各1mol 的混合液中通入氯气2.5 mol,离子反应方程式为:____ 。
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO3-还原为N2。上述反应的离子方程式为___ 。
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为____ 。
(6) Fe的一种含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是______ 。
(2)向1L 1mol/L的NH4Al(SO4)2溶液中滴加2.25L 等浓度的Ba(OH)2溶液,离子反应方程式为:
(3)向含FeI2和FeBr2各1mol 的混合液中通入氯气2.5 mol,离子反应方程式为:
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO3-还原为N2。上述反应的离子方程式为
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
(6) Fe的一种含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】将19.2g的铜和某浓度的硝酸反应,生成8.96L(标况)的气体,则参加反应的硝酸为____ mol,将这8.96L的气体和标况下________ L的氧气混合,再通入水中没有气体剩余。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将化学方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(未配平,不考虑2NO2 N2O4)
N2O4)
完成下列填空:
(1)硝酸在该反应中的作用是_________ ,该反应的还原产物是_______ 。
(2)0.3molCu被硝酸完全溶解后,Cu失去的电子数是____ 个,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______ ,若用排水法收集这些气体,可得标准状况下的气体______ L。
(3)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出该反应的离子方程式________ 。
(4)如果没有对该反应中的某些物质的比例作限定,则化学方程式可能的配平系数有许多组。原因是_______________________ 。
 N2O4)
N2O4)完成下列填空:
(1)硝酸在该反应中的作用是
(2)0.3molCu被硝酸完全溶解后,Cu失去的电子数是
(3)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出该反应的离子方程式
(4)如果没有对该反应中的某些物质的比例作限定,则化学方程式可能的配平系数有许多组。原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】饮用水消毒一直是科学家致力研究的课题
(1)Cl2常用于饮用水消毒。Cl2溶于水得到氯水,氯水中HClO的浓度越大杀菌能力越强。已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、ClO-三种微粒分别在三者中所占百分数与pH的关系如图。新制饱和氯水pH约为1~2,此时反应的离子方程式为_______ ,而要达到良好的杀菌效果,Cl2处理饮用水时溶液的pH最佳 控制范围是 _______ 。

(2)已知溴的性质和氯有一定的相似性,臭氧氧化技术被广泛用于饮用水的处理,但当水中含有Br-时也会产生易致癌的 BrO 。
。
①取含 Br-的水样,向其中投加一定量的 H2O2,再经 O3氧化后,水中溴酸盐(BrO )的含量如图所示
)的含量如图所示

投加过氧化氢,其目的是_______ ,未投加过氧化氢,臭氧投加量在 0~1.0 mg·L-1时,BrO 的浓度为 0 的可能原因是
的浓度为 0 的可能原因是_______ 。
②科研小组在控制其他条件一定时,研究投入H2O2和O3比例 [用n(H2O2)/n(O3)表示]不同时对水样中 Br-浓度的影响,结果如图。在相同时刻,投加 H2O2的反应中 Br-的浓度高于未投加 H2O2的浓度,其可能原因是反应过程中生成的HBrO 被 H2O2还原所致,该反应的化学方程式为_______ 。

③水中BrO 能被活性炭有效去除,其去除机理分为两步,第一步是
能被活性炭有效去除,其去除机理分为两步,第一步是_______ ;第二步是BrO 被活性炭还原为Br-,其反应方程式(未配平)如下:
被活性炭还原为Br-,其反应方程式(未配平)如下:
≡C+BrO → BrO-+≡CO2①
→ BrO-+≡CO2①
≡C+BrO-→ Br-+ ≡CO2②
反应的总方程式为:2BrO + 3 ≡C = 2Br-+ 3 ≡CO2。
+ 3 ≡C = 2Br-+ 3 ≡CO2。
其中≡C 代表活性炭表面,≡CO2代表活性炭表面氧化物。
则反应①与反应②中参加反应的≡C 个数之比为_______ 。
(1)Cl2常用于饮用水消毒。Cl2溶于水得到氯水,氯水中HClO的浓度越大杀菌能力越强。已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、ClO-三种微粒分别在三者中所占百分数与pH的关系如图。新制饱和氯水pH约为1~2,此时反应的离子方程式为

(2)已知溴的性质和氯有一定的相似性,臭氧氧化技术被广泛用于饮用水的处理,但当水中含有Br-时也会产生易致癌的 BrO
 。
。①取含 Br-的水样,向其中投加一定量的 H2O2,再经 O3氧化后,水中溴酸盐(BrO
 )的含量如图所示
)的含量如图所示
投加过氧化氢,其目的是
 的浓度为 0 的可能原因是
的浓度为 0 的可能原因是②科研小组在控制其他条件一定时,研究投入H2O2和O3比例 [用n(H2O2)/n(O3)表示]不同时对水样中 Br-浓度的影响,结果如图。在相同时刻,投加 H2O2的反应中 Br-的浓度高于未投加 H2O2的浓度,其可能原因是反应过程中生成的HBrO 被 H2O2还原所致,该反应的化学方程式为

③水中BrO
 能被活性炭有效去除,其去除机理分为两步,第一步是
能被活性炭有效去除,其去除机理分为两步,第一步是 被活性炭还原为Br-,其反应方程式(未配平)如下:
被活性炭还原为Br-,其反应方程式(未配平)如下:≡C+BrO
 → BrO-+≡CO2①
→ BrO-+≡CO2①≡C+BrO-→ Br-+ ≡CO2②
反应的总方程式为:2BrO
 + 3 ≡C = 2Br-+ 3 ≡CO2。
+ 3 ≡C = 2Br-+ 3 ≡CO2。其中≡C 代表活性炭表面,≡CO2代表活性炭表面氧化物。
则反应①与反应②中参加反应的≡C 个数之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
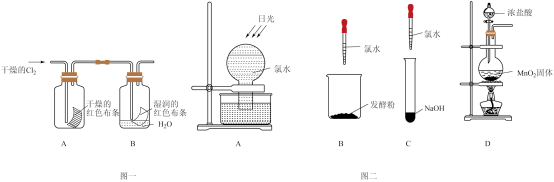
【推荐2】Cl2是一种重要的化工原料,可以制备许多含氯产品,从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。某化学兴趣小组为了探究Cl2的相关性质,设计了如图的一系列实验。以下是氯元素形成物质的二维图的部分信息及相关实验装置。
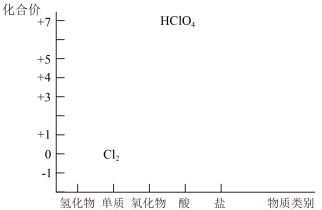
(1)根据二维图中信息,写出任意一种氯的氧化物的化学式:_______ 。
(2)结合二维图,从氧化还原的角度说明Cl2具有性质是:_______ 。
(3)将Cl2通入水中,其化学方程式为:_______ 。
(4)图一中,通入Cl2后,从集气瓶A、B的现象可得出的结论是_______ 。
(5)从化学实验的安全环保角度考虑,你认为再应增加的装置是_______ 。该装置中发生反应的离子方程式为_______ 。
(6)图二中四组实验,不会产生气体的是_______ ,B中反应的离子方程式为_______ 。


(1)根据二维图中信息,写出任意一种氯的氧化物的化学式:
(2)结合二维图,从氧化还原的角度说明Cl2具有性质是:
(3)将Cl2通入水中,其化学方程式为:
(4)图一中,通入Cl2后,从集气瓶A、B的现象可得出的结论是
(5)从化学实验的安全环保角度考虑,你认为再应增加的装置是
(6)图二中四组实验,不会产生气体的是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】为了研究钠的性质,在实验室里做了如下实验:
(1)将一小块钠投入 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为_______ 。
(2)为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为ag,将质量为bg的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为cg。

①列出计算钠相对原子质量的数学表达式_______ (用含有a、b、c的算式表示)。
②无水氯化钙的作用是_______ 。若不用无水氯化钙,求出的钠的相对原子质量的实际数值是偏大还是偏小?_______ 。
(3)现有一块部分被氧化为氧化钠的钠块,其质量为10.8g,将它投入一定量的水中完全反应,最终得到含16g溶质的氢氧化钠溶液,回答下列问题:
①反应中生成的氢气为_______ mol。
②钠的质量为_______ g。
(1)将一小块钠投入
 溶液中,发生反应的总化学方程式为
溶液中,发生反应的总化学方程式为(2)为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为ag,将质量为bg的钠(不足量)放入水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为cg。

①列出计算钠相对原子质量的数学表达式
②无水氯化钙的作用是
(3)现有一块部分被氧化为氧化钠的钠块,其质量为10.8g,将它投入一定量的水中完全反应,最终得到含16g溶质的氢氧化钠溶液,回答下列问题:
①反应中生成的氢气为
②钠的质量为
您最近一年使用:0次



