铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将化学方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(未配平,不考虑2NO2 N2O4)
N2O4)
完成下列填空:
(1)硝酸在该反应中的作用是_________ ,该反应的还原产物是_______ 。
(2)0.3molCu被硝酸完全溶解后,Cu失去的电子数是____ 个,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______ ,若用排水法收集这些气体,可得标准状况下的气体______ L。
(3)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出该反应的离子方程式________ 。
(4)如果没有对该反应中的某些物质的比例作限定,则化学方程式可能的配平系数有许多组。原因是_______________________ 。
 N2O4)
N2O4)完成下列填空:
(1)硝酸在该反应中的作用是
(2)0.3molCu被硝酸完全溶解后,Cu失去的电子数是
(3)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出该反应的离子方程式
(4)如果没有对该反应中的某些物质的比例作限定,则化学方程式可能的配平系数有许多组。原因是
更新时间:2017-04-08 13:24:19
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】铜及其化合物是中学化学的重要学习内容。
(1)铜和浓硫酸在加热条件下能反应: ,该反应中氧化剂和还原剂物质的量之比为
,该反应中氧化剂和还原剂物质的量之比为_______ ;
(2)CuSO4溶液与少量氨水反应,开始生成浅蓝色的碱式硫酸铜[Cu2(OH)2SO4]沉淀。写出该反应的离子方程式:_______ ;
(3)将50g胆矾放在坩埚中加热,使温度缓慢升高,在加热过程中,温度与固体质量的关系如下图所示。A点的固体成分是_______ ,B点的固体成分是_______ ,C点的固体成分是_______ 。(填物质的化学式)

(1)铜和浓硫酸在加热条件下能反应:
 ,该反应中氧化剂和还原剂物质的量之比为
,该反应中氧化剂和还原剂物质的量之比为(2)CuSO4溶液与少量氨水反应,开始生成浅蓝色的碱式硫酸铜[Cu2(OH)2SO4]沉淀。写出该反应的离子方程式:
(3)将50g胆矾放在坩埚中加热,使温度缓慢升高,在加热过程中,温度与固体质量的关系如下图所示。A点的固体成分是

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】完成下列问题。
(1)若将50mL4mol·L-1稀硝酸和200mL0.5mol·L-1稀硫酸混合后,加入19.2g铜粉,微热,充分反应。若忽略溶液体积变化,溶液中铜离子物质的量浓度为___________ mol·L-1。
(2)处理某废水时,反应过程中部分离子浓度与反应进程关系如图,反应过程中主要存在N2、 、ClO-、CNO-(C为+4价)、Cl-等微粒。写出处理该废水时发生反应的离子方程式
、ClO-、CNO-(C为+4价)、Cl-等微粒。写出处理该废水时发生反应的离子方程式_______ 。

(3)Na2SX(X=2,4,6,8等)在碱性溶液中可被NaClO氧化为Na2SO4。Na2SX中含有的化学键类型有___________ 。
(4)足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.12LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol•L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是___________ mL。
(5)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
①H3PO2与足量NaOH溶液反应生成NaH2PO2。已知:NaH2PO2的水溶液呈碱性,则H3PO2是___________ 酸(填“强”或“弱”);写出H3PO2的电离方程式:___________ 。
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银,利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,写出化学镀银反应的离子方程式_______ 。
(1)若将50mL4mol·L-1稀硝酸和200mL0.5mol·L-1稀硫酸混合后,加入19.2g铜粉,微热,充分反应。若忽略溶液体积变化,溶液中铜离子物质的量浓度为
(2)处理某废水时,反应过程中部分离子浓度与反应进程关系如图,反应过程中主要存在N2、
 、ClO-、CNO-(C为+4价)、Cl-等微粒。写出处理该废水时发生反应的离子方程式
、ClO-、CNO-(C为+4价)、Cl-等微粒。写出处理该废水时发生反应的离子方程式
(3)Na2SX(X=2,4,6,8等)在碱性溶液中可被NaClO氧化为Na2SO4。Na2SX中含有的化学键类型有
(4)足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.12LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol•L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
(5)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
①H3PO2与足量NaOH溶液反应生成NaH2PO2。已知:NaH2PO2的水溶液呈碱性,则H3PO2是
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银,利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,写出化学镀银反应的离子方程式
您最近一年使用:0次
【推荐3】Ⅰ、从金属锌、氢气、氧气、水、一氧化碳、氧化铜、盐酸中任挑选作为反应物,按下列要求写出化学方程式:
(1)既属于化合反应,又属于氧化还原反应:______________________________________
(2)属于氧化还原反应,不属于置换反应、化合反应、分解反应、复分解反应:_______________________
Ⅱ、某汽车安全气囊的产气药剂主要含有 、
、 、
、 等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1) 是气体发生剂,是
是气体发生剂,是___________ (用“电解质”或者“非电解质”填空),其中N的化合价为____________ 。 受热分解产生
受热分解产生 和Na,则该反应方程式为:
和Na,则该反应方程式为:_________________________ 。已知常温常压下气体摩尔体积为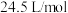 ,则在常温常压下,反应
,则在常温常压下,反应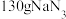 能产生
能产生__________ L的 。
。
(2) 是主氧化剂,与Na反应生成的还原产物为
是主氧化剂,与Na反应生成的还原产物为___________ (已知该反应为置换反应)。若已知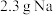 完全反应,转移的电子物质的量为
完全反应,转移的电子物质的量为___________ 。
(3) 是助氧化剂,反应过程中与Na作用生成KCl和
是助氧化剂,反应过程中与Na作用生成KCl和 ,请用单线桥表示该反应电子转移:
,请用单线桥表示该反应电子转移: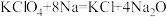
_______________________ 。
(1)既属于化合反应,又属于氧化还原反应:
(2)属于氧化还原反应,不属于置换反应、化合反应、分解反应、复分解反应:
Ⅱ、某汽车安全气囊的产气药剂主要含有
 、
、 、
、 等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。(1)
 是气体发生剂,是
是气体发生剂,是 受热分解产生
受热分解产生 和Na,则该反应方程式为:
和Na,则该反应方程式为: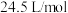 ,则在常温常压下,反应
,则在常温常压下,反应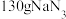 能产生
能产生 。
。(2)
 是主氧化剂,与Na反应生成的还原产物为
是主氧化剂,与Na反应生成的还原产物为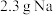 完全反应,转移的电子物质的量为
完全反应,转移的电子物质的量为(3)
 是助氧化剂,反应过程中与Na作用生成KCl和
是助氧化剂,反应过程中与Na作用生成KCl和 ,请用单线桥表示该反应电子转移:
,请用单线桥表示该反应电子转移: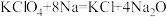
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】铜在化合物中的常见化合价有 、
、 。已知
。已知 与稀硫酸反应,溶液呈蓝色。
与稀硫酸反应,溶液呈蓝色。
(1)工业上可用 反应制取粗铜,该反应中
反应制取粗铜,该反应中_______ 元素被还原。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为_______ 。温度控制在50~60℃的原因除了加快反应速率外,还有_______ 。在 溶液中加入一定量的
溶液中加入一定量的 和
和 溶液加热,生成
溶液加热,生成 沉淀,写出生成
沉淀,写出生成 的离子方程式:
的离子方程式:_______ 。
(3)现向 、
、 和
和 组成的混合物中,加入
组成的混合物中,加入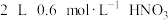 溶液恰好使混合物溶解,同时收集到
溶液恰好使混合物溶解,同时收集到 气体(标准状况)。
气体(标准状况)。 与稀硝酸反应的离方程式为
与稀硝酸反应的离方程式为_______ 。若混合物中含 ,将该混合物与稀硫酸充分反应,消耗
,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为_______  。
。
 、
、 。已知
。已知 与稀硫酸反应,溶液呈蓝色。
与稀硫酸反应,溶液呈蓝色。(1)工业上可用
 反应制取粗铜,该反应中
反应制取粗铜,该反应中(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入
 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为 溶液中加入一定量的
溶液中加入一定量的 和
和 溶液加热,生成
溶液加热,生成 沉淀,写出生成
沉淀,写出生成 的离子方程式:
的离子方程式:(3)现向
 、
、 和
和 组成的混合物中,加入
组成的混合物中,加入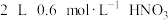 溶液恰好使混合物溶解,同时收集到
溶液恰好使混合物溶解,同时收集到 气体(标准状况)。
气体(标准状况)。 与稀硝酸反应的离方程式为
与稀硝酸反应的离方程式为 ,将该混合物与稀硫酸充分反应,消耗
,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为 。
。
您最近一年使用:0次
【推荐2】含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠( )较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________
)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________
(2)我国从2000年起逐步用 气体替代氯气进行消毒,实验室常用
气体替代氯气进行消毒,实验室常用 、草酸(
、草酸( )和稀硫酸制备
)和稀硫酸制备 ,草酸被氧化成
,草酸被氧化成 ,则该反应的离子方程式为
,则该反应的离子方程式为___________ 。
(3)工业上可利用 制备亚氯酸钠(
制备亚氯酸钠( ),反应体系中涉及下列物质:
),反应体系中涉及下列物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。
(4)某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、 的混合液,经测定溶液中
的混合液,经测定溶液中 与
与 的离子个数比为1:4,则该反应中被还原与被氧化的
的离子个数比为1:4,则该反应中被还原与被氧化的 的分子个数比为
的分子个数比为___________ 。
(5)请完成该过程的化学方程式并配平。
______ _______
_______ ______
______ _______
_______ _______
_______ ______(________)
______(________) ___________
若反应生成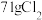 ,被氧化的HCl质量为
,被氧化的HCl质量为___________ 。
(6)已知氧化性: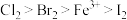 ,则:
,则:
① 溶液中通入一定量的
溶液中通入一定量的 ,发生反应的离子方程式为:
,发生反应的离子方程式为: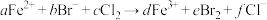 ,下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是
,下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是___________ 。
A.2;4;3;2;2;6 B.0;2;1;0;1;2
C.2;2;2;2;1;4 D.2;6;4;2;3;8
② 、
、 和
和 的个数之比为2:2:5,在溶液中反应的离子反应方程式为
的个数之比为2:2:5,在溶液中反应的离子反应方程式为___________ 。
(7)实验室用下列方法均可制取氯气
①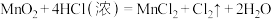
②
③
④
若各反应转移的电子数相同,①②③④生成的氯气质量比为___________ 。
(1)亚氯酸钠(
 )较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________
)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________A.NaCl、 | B.NaCl、NaClO |
C. 、 、 | D.NaCl、 |
 气体替代氯气进行消毒,实验室常用
气体替代氯气进行消毒,实验室常用 、草酸(
、草酸( )和稀硫酸制备
)和稀硫酸制备 ,草酸被氧化成
,草酸被氧化成 ,则该反应的离子方程式为
,则该反应的离子方程式为(3)工业上可利用
 制备亚氯酸钠(
制备亚氯酸钠( ),反应体系中涉及下列物质:
),反应体系中涉及下列物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 ,写出反应的化学方程式:
,写出反应的化学方程式:(4)某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、
 的混合液,经测定溶液中
的混合液,经测定溶液中 与
与 的离子个数比为1:4,则该反应中被还原与被氧化的
的离子个数比为1:4,则该反应中被还原与被氧化的 的分子个数比为
的分子个数比为(5)请完成该过程的化学方程式并配平。
______
 _______
_______ ______
______ _______
_______ _______
_______ ______(________)
______(________) 若反应生成
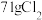 ,被氧化的HCl质量为
,被氧化的HCl质量为(6)已知氧化性:
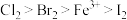 ,则:
,则:①
 溶液中通入一定量的
溶液中通入一定量的 ,发生反应的离子方程式为:
,发生反应的离子方程式为: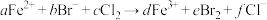 ,下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是
,下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是A.2;4;3;2;2;6 B.0;2;1;0;1;2
C.2;2;2;2;1;4 D.2;6;4;2;3;8
②
 、
、 和
和 的个数之比为2:2:5,在溶液中反应的离子反应方程式为
的个数之比为2:2:5,在溶液中反应的离子反应方程式为(7)实验室用下列方法均可制取氯气
①
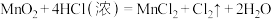
②

③

④

若各反应转移的电子数相同,①②③④生成的氯气质量比为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】(1)向NaHSO4溶液中滴加NaHSO3溶液的离子反应方程式为:_____ ,若是改加氢氧化钡溶液至中性,离子反应方程式为:______ 。
(2)向1L 1mol/L的NH4Al(SO4)2溶液中滴加2.25L 等浓度的Ba(OH)2溶液,离子反应方程式为:__ 。
(3)向含FeI2和FeBr2各1mol 的混合液中通入氯气2.5 mol,离子反应方程式为:____ 。
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO3-还原为N2。上述反应的离子方程式为___ 。
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为____ 。
(6) Fe的一种含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是______ 。
(2)向1L 1mol/L的NH4Al(SO4)2溶液中滴加2.25L 等浓度的Ba(OH)2溶液,离子反应方程式为:
(3)向含FeI2和FeBr2各1mol 的混合液中通入氯气2.5 mol,离子反应方程式为:
(4)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染,催化反硝化法中H2能将NO3-还原为N2。上述反应的离子方程式为
(5)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为
(6) Fe的一种含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁和铝等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示: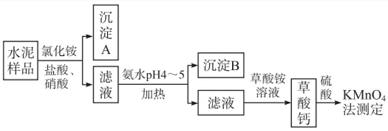
(1)在溶解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是_____ ,还常使用_____ (填一种) 等物质代替硝酸。
(2)沉淀A的主要成分能与氢氟酸发生反应,该反应的化学方程式为__________ 。
(3)沉淀B 的主要成分有_____ (填化学式)。
(4)加氨水的过程中,加热的目的是__________ 。
(5)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定过程中发生反应的离子方程式为._________________ 。

(1)在溶解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(2)沉淀A的主要成分能与氢氟酸发生反应,该反应的化学方程式为
(3)沉淀B 的主要成分有
(4)加氨水的过程中,加热的目的是
(5)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定过程中发生反应的离子方程式为.
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】完成下列问题。
(1)若将50mL4mol·L-1稀硝酸和200mL0.5mol·L-1稀硫酸混合后,加入19.2g铜粉,微热,充分反应。若忽略溶液体积变化,溶液中铜离子物质的量浓度为___________ mol·L-1。
(2)处理某废水时,反应过程中部分离子浓度与反应进程关系如图,反应过程中主要存在N2、 、ClO-、CNO-(C为+4价)、Cl-等微粒。写出处理该废水时发生反应的离子方程式
、ClO-、CNO-(C为+4价)、Cl-等微粒。写出处理该废水时发生反应的离子方程式_______ 。

(3)Na2SX(X=2,4,6,8等)在碱性溶液中可被NaClO氧化为Na2SO4。Na2SX中含有的化学键类型有___________ 。
(4)足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.12LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol•L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是___________ mL。
(5)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
①H3PO2与足量NaOH溶液反应生成NaH2PO2。已知:NaH2PO2的水溶液呈碱性,则H3PO2是___________ 酸(填“强”或“弱”);写出H3PO2的电离方程式:___________ 。
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银,利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,写出化学镀银反应的离子方程式_______ 。
(1)若将50mL4mol·L-1稀硝酸和200mL0.5mol·L-1稀硫酸混合后,加入19.2g铜粉,微热,充分反应。若忽略溶液体积变化,溶液中铜离子物质的量浓度为
(2)处理某废水时,反应过程中部分离子浓度与反应进程关系如图,反应过程中主要存在N2、
 、ClO-、CNO-(C为+4价)、Cl-等微粒。写出处理该废水时发生反应的离子方程式
、ClO-、CNO-(C为+4价)、Cl-等微粒。写出处理该废水时发生反应的离子方程式
(3)Na2SX(X=2,4,6,8等)在碱性溶液中可被NaClO氧化为Na2SO4。Na2SX中含有的化学键类型有
(4)足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.12LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol•L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
(5)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
①H3PO2与足量NaOH溶液反应生成NaH2PO2。已知:NaH2PO2的水溶液呈碱性,则H3PO2是
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银,利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,写出化学镀银反应的离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】为探究Ba(NO3)2和BaCl2的性质,某课外小组同学进行下列实验。
(1)甲组同学向Ba(NO3)2溶液中通入SO2,有白色沉淀生成。向BaCl2溶液中通入SO2,无明显现象。
①向Ba(NO3)2溶液中通入SO2产生的沉淀为___________ (填化学式)。
②若向通入SO2的BaCl2溶液中再加入H2O2,也可产生白色沉淀,则该反应的离子方程式为________________ 。
(2)乙组同学向BaCl2溶液中同时通入NH3和SO2,然后滴入Na2CrO4溶液,沉淀由____ (填“白色”或“黄色”,下同)转变为_____ 。[已知:BaCrO4为黄色固体,Ksp(BaCrO4)sp(BaSO3)]
(3)已知25 ℃时,Ksp(BaSO3)=5.5×10-7,Ksp(BaSO4)= 1.1×10-10,则该温度下,反应:
BaSO3(s) +SO42-(aq) BaSO4(s) +SO32-(aq)的平衡常数为
BaSO4(s) +SO32-(aq)的平衡常数为__________ 。
(4)向Ba(NO3)2溶液中加入少量稀硫酸调至溶液pH为2.5,加入少量新制的纳米铁粉,充分反应后,加入NaOH溶液调至碱性,产生白色沉淀。一段时间后沉淀变为灰绿色,最后变为红褐色,将悬浊液微热,可产生使湿润的红色石蕊试纸变蓝的气体。则纳米铁粉与Ba(NO3)2酸性溶液发生的主要反应的离子方程式为_______________________ 。
(1)甲组同学向Ba(NO3)2溶液中通入SO2,有白色沉淀生成。向BaCl2溶液中通入SO2,无明显现象。
①向Ba(NO3)2溶液中通入SO2产生的沉淀为
②若向通入SO2的BaCl2溶液中再加入H2O2,也可产生白色沉淀,则该反应的离子方程式为
(2)乙组同学向BaCl2溶液中同时通入NH3和SO2,然后滴入Na2CrO4溶液,沉淀由
(3)已知25 ℃时,Ksp(BaSO3)=5.5×10-7,Ksp(BaSO4)= 1.1×10-10,则该温度下,反应:
BaSO3(s) +SO42-(aq)
 BaSO4(s) +SO32-(aq)的平衡常数为
BaSO4(s) +SO32-(aq)的平衡常数为(4)向Ba(NO3)2溶液中加入少量稀硫酸调至溶液pH为2.5,加入少量新制的纳米铁粉,充分反应后,加入NaOH溶液调至碱性,产生白色沉淀。一段时间后沉淀变为灰绿色,最后变为红褐色,将悬浊液微热,可产生使湿润的红色石蕊试纸变蓝的气体。则纳米铁粉与Ba(NO3)2酸性溶液发生的主要反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】将128g铜置于一定量的浓硝酸中并微热。当铜片完全消失时,共收集到NO2和NO的混合气体44.8L(标准状况下)。
(1)写出上述过程中,有关反应的离子方程式______________ 、_____________ 。
(2)完成该反应至少需要量取10mol/L的浓硝酸__________ mL。
(3)混合气体中NO2的体积为__________ L,NO的体积为__________ L(均为标准状况下)。
(4)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2使其充分反应,若要使溶液恰好充满容器,则理论上需要参加反应的O2的物质的量为____________ mol。
(1)写出上述过程中,有关反应的离子方程式
(2)完成该反应至少需要量取10mol/L的浓硝酸
(3)混合气体中NO2的体积为
(4)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2使其充分反应,若要使溶液恰好充满容器,则理论上需要参加反应的O2的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】将19.2g的铜和某浓度的硝酸反应,生成8.96L(标况)的气体,则参加反应的硝酸为____ mol,将这8.96L的气体和标况下________ L的氧气混合,再通入水中没有气体剩余。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】某化工厂制取硝酸铜有以下两种途径:
A.铜与稀硝酸反应,反应的化学方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
B.铜与浓硝酸反应,反应的化学方程式:Cu+4HNO3(浓)=Cu(NO3)2+2X↑+2H2O
(1)试确定X的化学式_______ ,硝酸铜中氮元素化合价为_______ 。
(2)对比A、B两个反应可得到的结论是_______ 。
(3)一氧化氮,二氧化氮是大气污染物,在生产中要尽可能减少排放,判断:若要制得等质量的硝酸铜,以上的_______ 途径较好?说明理由_______ ,_______ 。(两条)
(4)根据所学知识,设计制取硝酸铜的最佳途径(用化学方程式表示)。______________ 。
A.铜与稀硝酸反应,反应的化学方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
B.铜与浓硝酸反应,反应的化学方程式:Cu+4HNO3(浓)=Cu(NO3)2+2X↑+2H2O
(1)试确定X的化学式
(2)对比A、B两个反应可得到的结论是
(3)一氧化氮,二氧化氮是大气污染物,在生产中要尽可能减少排放,判断:若要制得等质量的硝酸铜,以上的
(4)根据所学知识,设计制取硝酸铜的最佳途径(用化学方程式表示)。
您最近一年使用:0次



