解题方法
1 . 钠元素在自然界中分布很广,储量极为丰富,都以化合态存在,如氯化钠、碳酸钠、硫酸钠等。钠单质和钠的化合物在生产、生活中被广泛应用。请根据钠及其化合物性质按要求完成各题。
(1)钠原子在周期表中的位置为___________ ,钠离子的结构示意图___________ 。
(2)请选择下列物质中合适的物质,按要求填空:
NaOH、 CaCl2 、 SO2 、H2O 、 NH4Cl
只含有离子键的有___________ (填化学式,下同),既含有离子键又含有共价键的有___________ ,只含共价键的有___________ 。
(3)钠的化学性质活泼,暴露在空气中生成___________ 色Na2O,在空气中加热,生成___________ 色的Na2O2,Na2O2可用作呼吸面具、潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:___________ 。
(4)钠能在冷水中剧烈反应,该反应的实验现象中描述错误的是____。
(5)下列有关物质的性质描述正确的是____。
(6)Na2CO3和NaHCO3是常见的钠盐,且两者之间可以相互转化,请回答下列问题:
①下列有关碳酸钠和碳酸氢钠的说法正确的是____ 。
A.热稳定性:Na2CO3<NaHCO3
B.溶于水后,碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性
C.相同条件下,与同种酸反应的剧烈程度:Na2CO3<NaHCO3
D.石碱风化是物理过程
②写出Na2CO3在水溶液中的电离方程式___________ ;
③向Na2CO3溶液中通入CO2可生成NaHCO3,该反应的化学方程式为___________ ;
④加热15.0g碳酸钠和碳酸氢钠的固体混合物至质量不再发生变化,剩余固体的质量为11.9g,则混合物中碳酸氢钠的质量分数为____ 。
A.42% B.44% C.56% D.58%
(1)钠原子在周期表中的位置为
(2)请选择下列物质中合适的物质,按要求填空:
NaOH、 CaCl2 、 SO2 、H2O 、 NH4Cl
只含有离子键的有
(3)钠的化学性质活泼,暴露在空气中生成
(4)钠能在冷水中剧烈反应,该反应的实验现象中描述错误的是____。
| A.钠熔化成银白色小球 | B.钠在水面上迅速游动 |
| C.发出嘶嘶的声响 | D.溶液逐渐变红色 |
| A.钠与氧气反应时的产物主要取决于氧气的用量及纯度 |
| B.钠投入硫酸铜溶液中有气体和蓝色沉淀产生 |
| C.Na2O和Na2O2分别溶于水中,所得的产物相同 |
| D.FeCl3溶液用于铜质印刷线路制作,原因是两者发生置换反应 |
①下列有关碳酸钠和碳酸氢钠的说法正确的是
A.热稳定性:Na2CO3<NaHCO3
B.溶于水后,碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性
C.相同条件下,与同种酸反应的剧烈程度:Na2CO3<NaHCO3
D.石碱风化是物理过程
②写出Na2CO3在水溶液中的电离方程式
③向Na2CO3溶液中通入CO2可生成NaHCO3,该反应的化学方程式为
④加热15.0g碳酸钠和碳酸氢钠的固体混合物至质量不再发生变化,剩余固体的质量为11.9g,则混合物中碳酸氢钠的质量分数为
A.42% B.44% C.56% D.58%
您最近一年使用:0次
解题方法
2 . 某小组想通过实验探究 Na、Mg、Al 三种金属元素性质的递变规律。
I.探究 Na、Mg、Al 分别与水反应的情况。
实验①:切一小块绿豆大小的金属 Na,用滤纸吸干其表面的煤油,将其投入盛有 100ml 水(含酚酞)的烧杯中。观察到 Na 与冷水发生剧烈反应,烧杯内溶液变红。
(1)与水反应生成氢氧化钠和氢气,写出该反应的化学方程式___________ 。
(2)上述反应中,作还原剂的是___________ 。
A.Na B.H2O C.NaOH
(3)上述反应中若有23克金属Na被充分反应,则产生气体在标况下的体积约为___________ L。
(4)溶液中,使酚酞试液变红的微粒是___________ 。
A.Na+ B.H+ C.OH-
实验②:分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 2ml 水,再滴入2 滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③:另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验 操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 Al 与水反应现象仍不明显。
(5)实验②的设计中未考虑到的因素是___________ 。
(6)通过上述实验,得出 Na、Mg、Al 的金属性由强到弱的顺序是___________ 。
Ⅱ.比较 NaOH、Mg(OH)2、Al(OH)3碱性的强弱。
实验④:在试管中加入2ml 0.5mol·L-1 Al2(SO4)3溶液,然后逐滴滴加 2mol·L-1 NaOH溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤:在试管中加入2ml 1mol·L-1 MgSO4溶液,然后逐滴滴加2mol·L-1 NaOH 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
(7)写出由实验④、⑤的实验现象可推导得出的结论。
(8)综上实验可知,NaOH、Mg(OH)2、Al(OH)3的碱性由强到弱的顺序是___________ 。
I.探究 Na、Mg、Al 分别与水反应的情况。
实验①:切一小块绿豆大小的金属 Na,用滤纸吸干其表面的煤油,将其投入盛有 100ml 水(含酚酞)的烧杯中。观察到 Na 与冷水发生剧烈反应,烧杯内溶液变红。
(1)与水反应生成氢氧化钠和氢气,写出该反应的化学方程式
(2)上述反应中,作还原剂的是
A.Na B.H2O C.NaOH
(3)上述反应中若有23克金属Na被充分反应,则产生气体在标况下的体积约为
(4)溶液中,使酚酞试液变红的微粒是
A.Na+ B.H+ C.OH-
实验②:分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 2ml 水,再滴入2 滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③:另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验 操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 Al 与水反应现象仍不明显。
(5)实验②的设计中未考虑到的因素是
(6)通过上述实验,得出 Na、Mg、Al 的金属性由强到弱的顺序是
Ⅱ.比较 NaOH、Mg(OH)2、Al(OH)3碱性的强弱。
实验④:在试管中加入2ml 0.5mol·L-1 Al2(SO4)3溶液,然后逐滴滴加 2mol·L-1 NaOH溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤:在试管中加入2ml 1mol·L-1 MgSO4溶液,然后逐滴滴加2mol·L-1 NaOH 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
(7)写出由实验④、⑤的实验现象可推导得出的结论。
| 现象 | 结论 | |
| ④ | 出现白色沉淀 | Al(OH)3的碱性比NaOH弱 |
| 沉淀全部溶解 | ||
| ⑤ | 出现白色沉淀 | |
| 沉淀不溶解 | Mg(OH)2无酸性 |
您最近一年使用:0次
解题方法
3 . (一)金属种类繁多,性质各异,应用十分广泛。
(1)将一小块金属钠分别放入下列溶液中,对应的现象正确的是_______
(2)少量Na2O2与H2O反应生成H2O2和NaOH。下列说法正确的是_______
(3)向某溶液中加入少量Na2O2后,原溶液中所含的下列离子浓度会显著改变的是_______
(二)在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:(已知:室温下Ksp[Fe(OH)3]= 4.0×10-38)Ⅰ:向废液中投入过量铁屑,充分反应后分离出固体和滤液;Ⅱ:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
(4)FeCl3蚀刻铜箔反应的离子方程式为___________ :过程Ⅰ分离得到固体的主要成分是___________ 。
(5)过程Ⅱ中发生反应的化学方程式为___________ ;过程Ⅱ中调节溶液的pH为5,最终溶液中金属离子浓度为___________ 。(列式计算)
(6)有同学研究上述“过程Ⅱ”方案后,设计了下列方案:向滤液中加入足量的NaOH溶液使Fe2+完全沉淀,过滤,小心加热沉淀直到水分蒸干,再灼烧到质量不再变化。假设现有200mL0.1mol·L-1FeCl2溶液,按照上述操作,理想情况下,该同学应该得到的固体质量为___________ ;通过比较,说明石灰水—空气法与氢氧化钠—加热法相比的一个优点是___________ 。
(1)将一小块金属钠分别放入下列溶液中,对应的现象正确的是_______
| A.饱和NaOH溶液:产生气体,恢复至室温后溶液的pH增大 |
| B.稀CuSO4溶液:产生气体,有紫红色物质析出 |
| C.MgCl2溶液:产生气体,生成白色沉淀 |
| D.NH4NO3溶液:产生无色无味气体 |
(2)少量Na2O2与H2O反应生成H2O2和NaOH。下列说法正确的是_______
A.Na2O2的电子式为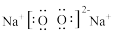 | B.H2O的空间构型为直线形 |
| C.H2O2中O元素的化合价为-1 | D.NaOH仅含离子键 |
(3)向某溶液中加入少量Na2O2后,原溶液中所含的下列离子浓度会显著改变的是_______
A.NO | B.NH | C.HCO | D.SO |
(二)在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:(已知:室温下Ksp[Fe(OH)3]= 4.0×10-38)Ⅰ:向废液中投入过量铁屑,充分反应后分离出固体和滤液;Ⅱ:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
(4)FeCl3蚀刻铜箔反应的离子方程式为
(5)过程Ⅱ中发生反应的化学方程式为
(6)有同学研究上述“过程Ⅱ”方案后,设计了下列方案:向滤液中加入足量的NaOH溶液使Fe2+完全沉淀,过滤,小心加热沉淀直到水分蒸干,再灼烧到质量不再变化。假设现有200mL0.1mol·L-1FeCl2溶液,按照上述操作,理想情况下,该同学应该得到的固体质量为
您最近一年使用:0次
名校
解题方法
4 . 将一小块金属钠分别放入下列溶液中,对应的现象正确的是
| A.饱和NaOH溶液:产生气体,恢复至室温后溶液的pH增大 |
| B.稀CuSO4溶液:产生气体,有紫红色物质析出 |
| C.MgCl2溶液:产生气体,生成白色沉淀 |
| D.NH4NO3溶液:产生无色无味气体 |
您最近一年使用:0次
2023-12-04更新
|
74次组卷
|
6卷引用:上海市南洋中学2023-2024学年高二上学期期中考试(等级)化学试题
上海市南洋中学2023-2024学年高二上学期期中考试(等级)化学试题上海市松江二中2021-2022学年高一下学期期末学情调研化学试题(已下线)第5章 金属及其化合物 5.1金属的性质上海市南洋中学2023-2024学年高一下学期期中考试化学试题 (已下线)专题06 常见金属及其化合物-备战2022年高考化学学霸纠错(全国通用)(已下线)专题02 海水中的重要元素——钠和氯-2023年高考化学一轮复习小题多维练(全国通用)
名校
解题方法
5 . Ⅰ.汉弗里·戴维是英国著名化学家,他提出:“电流与化合物的相互作用,是最有可能将所有物质分解为元素的方法”。通过这种方法,他制备得到了金属钾和钠。
(1)戴维在1807年用电解熔融烧碱的方法制得金属钠,电极之间设置镍网做隔膜以分离电解产物,电解的总反应方程式为:___________ 。
(2)关于金属钠,下列叙述正确的是___________
(3)钠在空气中燃烧产物的颜色是___________ , 电子式为___________ 。
(4)ag钠完全燃烧后,将固体充分溶解在bg水中,所得溶液溶质的质量分数是___________ 。
(5)某实验小组把 CO2通入饱和Na2CO3溶液制取NaHCO3,装置如下图所示(气密性已检验,部分夹持装置略):
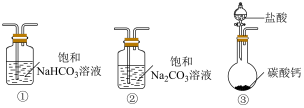
选取必要的实验装置,正确的连接顺序为___________ (填序号)。
Ⅱ.为确定制得的固体样品是纯净的 NaHCO3小组同学提出下列实验方案:
甲方案:将样品溶液与BaCl2溶液反应,观察现象
乙方案:测定 pH法
(6)为判定甲方案的可行性, 某同学用NaHCO3分析纯配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下:
此实验说明甲方案___________ (填“可行”或“不可行”)。
(7)产生浑浊(伴有气体产生)的离子方程式:___________ 。
(8)乙方案是:取等质量的固体样品和分析纯 Na2CO3加等质量的水配制的溶液,分别与 pH 计测定 pH,pH更大的是___________ (填化学式)。
(1)戴维在1807年用电解熔融烧碱的方法制得金属钠,电极之间设置镍网做隔膜以分离电解产物,电解的总反应方程式为:
(2)关于金属钠,下列叙述正确的是___________
| A.钠可保存在煤油或CCl4等液态有机物中 |
| B.氯化钠在电流作用下电离出的钠离子和氯离子 |
| C.钠与硫在常温下化合就能剧烈反应,甚至发生爆炸 |
| D.若金属钠着火,可采用干粉灭火器灭火 |
(3)钠在空气中燃烧产物的颜色是
(4)ag钠完全燃烧后,将固体充分溶解在bg水中,所得溶液溶质的质量分数是
(5)某实验小组把 CO2通入饱和Na2CO3溶液制取NaHCO3,装置如下图所示(气密性已检验,部分夹持装置略):

选取必要的实验装置,正确的连接顺序为
Ⅱ.为确定制得的固体样品是纯净的 NaHCO3小组同学提出下列实验方案:
甲方案:将样品溶液与BaCl2溶液反应,观察现象
乙方案:测定 pH法
(6)为判定甲方案的可行性, 某同学用NaHCO3分析纯配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下:
NaHCO3溶液 BaCl2溶液 | 0.2mol/L | 0.1mol/L | 0.02mol/L |
| 0.2mol/L | 浑浊 | 浑浊 | 少许浑浊 |
| 0.1mol/L | 浑浊 | 少许浑浊 | 无现象 |
| 0.02mol/L | 少许浑浊 | 无现象 | 无现象 |
(7)产生浑浊(伴有气体产生)的离子方程式:
(8)乙方案是:取等质量的固体样品和分析纯 Na2CO3加等质量的水配制的溶液,分别与 pH 计测定 pH,pH更大的是
您最近一年使用:0次
名校
解题方法
6 . 已知: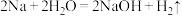 ,将
,将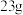 钠与过量的重水
钠与过量的重水 反应,产生气体的质量是
反应,产生气体的质量是___________ 。
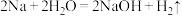 ,将
,将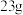 钠与过量的重水
钠与过量的重水 反应,产生气体的质量是
反应,产生气体的质量是
您最近一年使用:0次
名校
解题方法
7 . 等物质的量的钠和铁分别与足量的水反应,下列说法正确的是
| A.反应条件相同 | B.金属单质都作氧化剂 |
| C.转移电子的数目相同 | D.反应的还原产物相同 |
您最近一年使用:0次
名校
8 . 金属的性质
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
(2)我国自主研发的大飞机C919大量使用了铝锂合金。这是利用了铝锂合金的下列性质___________
(3)常温下,将铁片放到浓硫酸中,一段时间后___________
(4)下列关于碳酸钠和碳酸氢钠的叙述正确的是___________
(5)实验室测定氧化物X(FexOy)的组成实验如下:

下列有关说法正确的是___________
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
| A.钠沉入水底 | B.钠熔成小球 |
| C.发出“嘶嘶”声音 | D.溶液变红 |
| A.低强度 | B.低密度 | C.导热性 | D.熔点低 |
| A.溶液呈棕黄色 | B.铁片质量减轻 |
| C.有大量气泡产生 | D.铁片表面生成致密氧化膜 |
| A.相同条件下,在水中的溶解性:碳酸钠<碳酸氢钠 |
| B.相同条件下,热稳定性:碳酸钠>碳酸氢钠 |
| C.相同条件下,与酸反应的速率:碳酸钠>碳酸氢钠 |
| D.一定条件下,碳酸钠不能转化为碳酸氢钠,而碳酸氢钠可以转化为碳酸钠 |

下列有关说法正确的是___________
A.样品X中含有+2价铁元素 |
B.溶液 中 中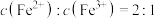 |
C.溶液 中的离子只有 中的离子只有 和 和 |
D.根据步骤I、II可判断 为 为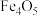 |
您最近一年使用:0次
名校
9 . 下列说法正确的是
A.切开的金属Na暴露在空气中,光亮的表面逐渐变暗,发生的反应为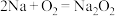 |
B.Na与稀硫酸反应的离子方程式为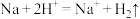 |
| C.4.6gNa与O2完全反应,生成7g产物时失去电子的物质的量为0.2mol |
| D.将少量Na投入到稀的CuSO4溶液中,会析出红色金属 |
您最近一年使用:0次
2023-07-16更新
|
191次组卷
|
2卷引用:上海市大同中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
10 . 按图所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列两种情况:
①用铝箔包住钠、②用铜箔包住钠。则收集产生的气体在相同条件下体积的关系是

①用铝箔包住钠、②用铜箔包住钠。则收集产生的气体在相同条件下体积的关系是

| A.二者收集气体一样多 | B.①收集气体体积较大 |
| C.②收集气体体积较大 | D.无法确定 |
您最近一年使用:0次



