名校
1 . 金属的性质
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
(2)我国自主研发的大飞机C919大量使用了铝锂合金。这是利用了铝锂合金的下列性质___________
(3)常温下,将铁片放到浓硫酸中,一段时间后___________
(4)下列关于碳酸钠和碳酸氢钠的叙述正确的是___________
(5)实验室测定氧化物X(FexOy)的组成实验如下:

下列有关说法正确的是___________
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
| A.钠沉入水底 | B.钠熔成小球 |
| C.发出“嘶嘶”声音 | D.溶液变红 |
| A.低强度 | B.低密度 | C.导热性 | D.熔点低 |
| A.溶液呈棕黄色 | B.铁片质量减轻 |
| C.有大量气泡产生 | D.铁片表面生成致密氧化膜 |
| A.相同条件下,在水中的溶解性:碳酸钠<碳酸氢钠 |
| B.相同条件下,热稳定性:碳酸钠>碳酸氢钠 |
| C.相同条件下,与酸反应的速率:碳酸钠>碳酸氢钠 |
| D.一定条件下,碳酸钠不能转化为碳酸氢钠,而碳酸氢钠可以转化为碳酸钠 |

下列有关说法正确的是___________
A.样品X中含有+2价铁元素 |
B.溶液 中 中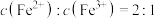 |
C.溶液 中的离子只有 中的离子只有 和 和 |
D.根据步骤I、II可判断 为 为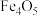 |
您最近一年使用:0次
名校
2 . 回答下列问题:
(1)盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,观察到的现象是_______。
(2)钠在空气中燃烧可制得过氧化钠,过氧化钠的用途之一便是在呼吸面具中做供氧剂,用化学语言(反应方程式)来说明其原理:(提示:人呼出的气体中含有CO2和水蒸气)_______ 。
(3)某实验小组通过以下实验来比较Na2CO3和NaHCO3两种物质的性质。称取两种固体各2g,分别放入两个小烧杯中,再各滴加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加2滴酚酞试液。
①a烧杯中固体完全溶解,而b烧杯固体有剩余,b烧杯内的物质是_______ 。
②同学们在两烧杯中还观察到了其它现象,其中a烧杯中出现的现象:Ⅰ溶液温度_______ (填“升高”或“降低”),Ⅱ滴加酚酞试液显_______ (填“红色”或“浅红)”。
(4)为比较两者热稳定性设计了“套管实验”,实验装置如图所示,整个实验过程中,能观察到澄清石灰水变浑浊的是烧杯_______ (填“A”成“B”)。

(5)以下能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是_______ 。
A.用pH试纸测定同浓度的Na2CO3和NaHCO3溶液pH值并做比较
B.分别在这两种物质的溶液中,加入少量CaCl2溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(6)常温下,用如图1所示装置,分别向 溶液和
溶液和 溶液中逐滴滴加
溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。

①表示向NaHCO3溶液中滴加盐酸的是曲线_______ (填X或Y)。
②写出ac段反应实质(离子方程式):_______ 。
(7)向 的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量_______ 。
(1)盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,观察到的现象是_______。
| A.钠在水层中反应并四处游动 | B.钠停留在煤油层中不发生反应 |
| C.钠在煤油的液面上反应并四处游动 | D.钠在煤油与水的界面处反应并上下跳动 |
(3)某实验小组通过以下实验来比较Na2CO3和NaHCO3两种物质的性质。称取两种固体各2g,分别放入两个小烧杯中,再各滴加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加2滴酚酞试液。
①a烧杯中固体完全溶解,而b烧杯固体有剩余,b烧杯内的物质是
②同学们在两烧杯中还观察到了其它现象,其中a烧杯中出现的现象:Ⅰ溶液温度
(4)为比较两者热稳定性设计了“套管实验”,实验装置如图所示,整个实验过程中,能观察到澄清石灰水变浑浊的是烧杯

(5)以下能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.用pH试纸测定同浓度的Na2CO3和NaHCO3溶液pH值并做比较
B.分别在这两种物质的溶液中,加入少量CaCl2溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(6)常温下,用如图1所示装置,分别向
 溶液和
溶液和 溶液中逐滴滴加
溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
①表示向NaHCO3溶液中滴加盐酸的是曲线
②写出ac段反应实质(离子方程式):
(7)向
 的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
您最近一年使用:0次
3 . 钠及其化合物具有独特的性质和广泛的用途。
I.
(1)下图为钠与水反应的实验示意图。
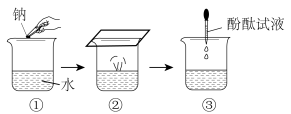
i.②中现象说明钠的密度比水___________ (“大”或“小”)。
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是___________ 。
a.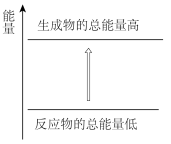 B.
B.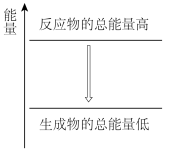
iii.③中加入酚酞试液后的现象是___________ 。
(2)用化学方程式表示由氯化钠制取金属钠的原理。___________
(3)将一定量的 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
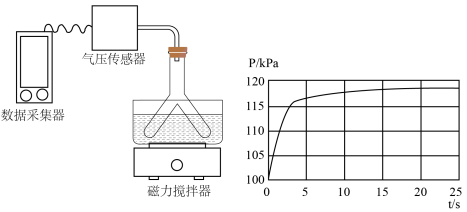
其中0~5s发生反应的离子方程式为___________ 。20s时溶液中的溶质是___________ (不考虑气体在水中的溶解)。
II.过碳酸钠( ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)
(4)结合 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应___________  。
。
A.大于 B.等于 C.小于
向 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是___________ 。
(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:
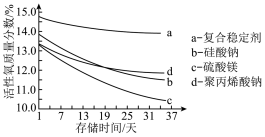
由图可知,制备过碳酸钠时应选择的稳定剂是___________ ,理由是___________ 。
A.a B.b C.c D.d
I.
(1)下图为钠与水反应的实验示意图。

i.②中现象说明钠的密度比水
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是
a.
 B.
B.
iii.③中加入酚酞试液后的现象是
(2)用化学方程式表示由氯化钠制取金属钠的原理。
(3)将一定量的
 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
其中0~5s发生反应的离子方程式为
II.过碳酸钠(
 ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)(4)结合
 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应 。
。A.大于 B.等于 C.小于
向
 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:

由图可知,制备过碳酸钠时应选择的稳定剂是
A.a B.b C.c D.d
您最近一年使用:0次
名校
4 . I.金属在生活中有着广泛的应用,人们甚至根据使用材料的种类,将人类漫长的历史分为了三个大的时代,分别是石器时代、青铜器时代,而后是铁器时代,直到19世纪早期,戴维组装了一个特别大的电池用于实验,先后发现了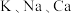 等许多金属。
等许多金属。
(1)造成上述人们利用金属先后顺序事实的最主要因素是_______。
(2)1827年维勒用金属钾还原熔融的无水氯化铝得到较纯的金属铝单质,但今天人们早已舍弃这种制备金属铝的方法,你认为可能的原因有_______ (写出一种合理原因即可)。写出现代工业上获得金属铝的化学反应方程式_______ 。
(3)已知铍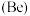 与铝的性质相似。则下列判断正确的是_______。
与铝的性质相似。则下列判断正确的是_______。
(4)钠是一种活泼的金属,将绿豆大的钠块投入如图所示的烧杯中,可能出现的现象_______。

(5)在蒸发皿中放一小块钠,加热至熔化成小球时,用玻璃棒蘸取少量无水 粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
(6)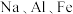 都是重要的金属元素。下列说法正确的是_______。
都是重要的金属元素。下列说法正确的是_______。
(7)类推的思维方法在化学学习中有时会产生错误结论,因此结论最终要经过实践的检验,才能决定其正确与否,下列几种关于金属的类推结论中,错误的是_______。
①钠与水反应生成 和
和 ;所有金属与水反应都生成碱和
;所有金属与水反应都生成碱和
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③ 与S直接化合时可得到
与S直接化合时可得到 ;
; 与S直接化合时也可得到
与S直接化合时也可得到
④ 受热易分解,
受热易分解,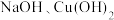 受热也易分解
受热也易分解
(8)单质A的燃烧热大。已知A为短周期元素,其气态原子逐个失去1~4个电子所需吸收能量如表所示。若该原子核外电子有三层,则该元素位于周期表_______ 族,写出A燃烧后形成的氧化物的电子式:_______ 。
Ⅱ.炼铁的主要原理之一是赤铁矿。它的主要成分在一定条件下有下列反应: 。在反应形成的固体混合物(
。在反应形成的固体混合物( 、
、 )中,元素铁和氧的质量比用
)中,元素铁和氧的质量比用 表示。
表示。
(9)根据上述反应,固体质量每减轻 ,将产生
,将产生
_______ L(S.T.P)。
(10)上述反应形成的固体混和物中, 不可能是_______。
不可能是_______。
(11) 也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式_______ 。
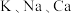 等许多金属。
等许多金属。(1)造成上述人们利用金属先后顺序事实的最主要因素是_______。
| A.地壳中金属元素的含量 | B.金属的延展性 |
| C.金属的导电性 | D.金属活泼性的差异 |
(3)已知铍
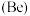 与铝的性质相似。则下列判断正确的是_______。
与铝的性质相似。则下列判断正确的是_______。| A.铍遇冷水剧烈反应 | B.氧化铍的化学式为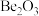 |
| C.氢氧化铍能与氢氧化钠溶液反应 | D. 能置换出 能置换出 中的镁单质 中的镁单质 |

| A.钠块在煤油、水两液体界面处反应,上下跳动,水层变红 |
| B.钠块只在煤油层中游动,并放出气体 |
| C.钠块只在水层中游动,钠块熔化,水层变红 |
| D.钠块在四氯化碳、水两液体界面处反应,熔化成小球并上下跳动,水层变红 |
 粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成。下列说法错误的是_______。
| A.钠受热易熔成小球说明其熔点低 |
B.钠与 粉末反应时放出大量热 粉末反应时放出大量热 |
C.一定条件下, 可与 可与 反应生成 反应生成 |
D.将无水 粉末改为 粉末改为 溶液,反应现象相同 溶液,反应现象相同 |
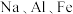 都是重要的金属元素。下列说法正确的是_______。
都是重要的金属元素。下列说法正确的是_______。| A.三者的最高价氧化物对应水化物均为碱性 | B.三者的氢氧化物都是白色固体 |
| C.三者的氯化物都可用化合反应制得 | D.三者的单质在空气中最终都生成氧化物 |
①钠与水反应生成
 和
和 ;所有金属与水反应都生成碱和
;所有金属与水反应都生成碱和
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③
 与S直接化合时可得到
与S直接化合时可得到 ;
; 与S直接化合时也可得到
与S直接化合时也可得到
④
 受热易分解,
受热易分解,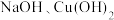 受热也易分解
受热也易分解| A.①② | B.③④ | C.①②③ | D.①②③④ |
 |  |  |  | …后续省略 | |
电离能( ) ) | 738 | 1451 | 7733 | 10540 | … |
Ⅱ.炼铁的主要原理之一是赤铁矿。它的主要成分在一定条件下有下列反应:
 。在反应形成的固体混合物(
。在反应形成的固体混合物( 、
、 )中,元素铁和氧的质量比用
)中,元素铁和氧的质量比用 表示。
表示。(9)根据上述反应,固体质量每减轻
 ,将产生
,将产生
(10)上述反应形成的固体混和物中,
 不可能是_______。
不可能是_______。| A.21∶9 | B.21∶7.5 | C.21∶5 | D.21∶8 |
 也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
也是铁重要的氧化物之一,其在高温下与金属铝反应,也能获得单质铁,写出相关的化学反应方程式
您最近一年使用:0次
5 . 把9.2 g金属钠投入到足量的重水(D2O)中
(1)写出该反应的化学方程式_______ 。
(2)产生的气体中含有_______ mol中子,_______ mol电子。
(3)若反应后溶液的体积为2升,则所得溶液的物质的量浓度为_______ 。
(1)写出该反应的化学方程式
(2)产生的气体中含有
(3)若反应后溶液的体积为2升,则所得溶液的物质的量浓度为
您最近一年使用:0次



