解题方法
1 . (一)金属种类繁多,性质各异,应用十分广泛。
(1)将一小块金属钠分别放入下列溶液中,对应的现象正确的是_______
(2)少量Na2O2与H2O反应生成H2O2和NaOH。下列说法正确的是_______
(3)向某溶液中加入少量Na2O2后,原溶液中所含的下列离子浓度会显著改变的是_______
(二)在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:(已知:室温下Ksp[Fe(OH)3]= 4.0×10-38)Ⅰ:向废液中投入过量铁屑,充分反应后分离出固体和滤液;Ⅱ:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
(4)FeCl3蚀刻铜箔反应的离子方程式为___________ :过程Ⅰ分离得到固体的主要成分是___________ 。
(5)过程Ⅱ中发生反应的化学方程式为___________ ;过程Ⅱ中调节溶液的pH为5,最终溶液中金属离子浓度为___________ 。(列式计算)
(6)有同学研究上述“过程Ⅱ”方案后,设计了下列方案:向滤液中加入足量的NaOH溶液使Fe2+完全沉淀,过滤,小心加热沉淀直到水分蒸干,再灼烧到质量不再变化。假设现有200mL0.1mol·L-1FeCl2溶液,按照上述操作,理想情况下,该同学应该得到的固体质量为___________ ;通过比较,说明石灰水—空气法与氢氧化钠—加热法相比的一个优点是___________ 。
(1)将一小块金属钠分别放入下列溶液中,对应的现象正确的是_______
| A.饱和NaOH溶液:产生气体,恢复至室温后溶液的pH增大 |
| B.稀CuSO4溶液:产生气体,有紫红色物质析出 |
| C.MgCl2溶液:产生气体,生成白色沉淀 |
| D.NH4NO3溶液:产生无色无味气体 |
(2)少量Na2O2与H2O反应生成H2O2和NaOH。下列说法正确的是_______
A.Na2O2的电子式为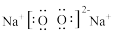 | B.H2O的空间构型为直线形 |
| C.H2O2中O元素的化合价为-1 | D.NaOH仅含离子键 |
(3)向某溶液中加入少量Na2O2后,原溶液中所含的下列离子浓度会显著改变的是_______
A.NO | B.NH | C.HCO | D.SO |
(二)在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:(已知:室温下Ksp[Fe(OH)3]= 4.0×10-38)Ⅰ:向废液中投入过量铁屑,充分反应后分离出固体和滤液;Ⅱ:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
(4)FeCl3蚀刻铜箔反应的离子方程式为
(5)过程Ⅱ中发生反应的化学方程式为
(6)有同学研究上述“过程Ⅱ”方案后,设计了下列方案:向滤液中加入足量的NaOH溶液使Fe2+完全沉淀,过滤,小心加热沉淀直到水分蒸干,再灼烧到质量不再变化。假设现有200mL0.1mol·L-1FeCl2溶液,按照上述操作,理想情况下,该同学应该得到的固体质量为
您最近一年使用:0次



