解题方法
1 . 下列指定反应的离子方程式正确的是
A. 与稀硫酸反应: 与稀硫酸反应: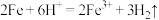 |
B. 与 与 溶液反应: 溶液反应: |
C.向氢氧化钡溶液中加入稀硫酸: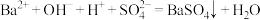 |
D.向碳酸氢铵溶液中加入足量石灰水: |
您最近一年使用:0次
2 . 下列图示方法能完成相应实验的是

A.用图①配制一定物质的量浓度的 溶液 溶液 |
B.用图②在实验室制取 |
| C.用图③探究碳酸氢钠和碳酸钠的热稳定性 |
D.用图④制备少量 并能较长时间看到其白色时,应先打开止水夹 并能较长时间看到其白色时,应先打开止水夹 C C |
您最近一年使用:0次
解题方法
3 . 下列关于Na2CO3和NaHCO3的性质比较中,不正确的是
| A.热稳定性:Na2CO3>NaHCO3 |
| B.常温时在水中的溶解度:NaHCO3>Na2CO3 |
| C.与盐酸反应剧烈程度:Na2CO3<NaHCO3 |
| D.等质量的固体与足量盐酸反应放出CO2的质量:Na2CO3<NaHCO3 |
您最近一年使用:0次
解题方法
4 . 生活离不开化学。下列有关说法正确的是
| A.聚氯乙烯塑料制品可用于食品包装 |
| B.1 mol葡萄糖可水解生成2 mol乳酸(C3H6O3) |
| C.维生素C具有还原性,在人体内起抗氧化作用 |
| D.碳酸氢钠用作食品膨松剂而谷氨酸钠用作食品防腐剂 |
您最近一年使用:0次
名校
解题方法
5 . 侯德榜为我国化工事业的发展做出了卓越贡献,是我国近代化学工业的奠基人之一,他结合中国国情对氨碱法进行改进,确定了新的工艺流程——侯氏制碱法:将氨碱法和合成氨法两种工艺联合起来,方法流程如图所示。
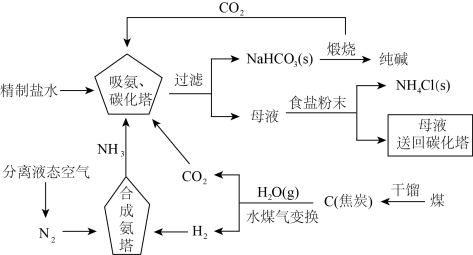
回答下列问题:
(1)向精制盐水中通入 、
、 的顺序及理由为
的顺序及理由为_______ (提示:从两种气体的溶解度进行分析)。
(2)写出 煅烧时发生反应的化学方程式:
煅烧时发生反应的化学方程式:_______ 。
(3)该流程中循环利用的物质为_______ (填化学式)。
(4)所得纯碱中可能含有少量NaCl杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:
i.称取ag样品,溶于水中;
ii.加入足量氯化钙溶液;
iii.过滤、洗涤、干燥、称量,所得沉淀质量为bg。
①证明步骤ⅱ中 已经沉淀完全的方法是
已经沉淀完全的方法是_______ 。
②该样品中碳酸钠的质量分数为_______ %(用含a、b的代数式表示)。

回答下列问题:
(1)向精制盐水中通入
 、
、 的顺序及理由为
的顺序及理由为(2)写出
 煅烧时发生反应的化学方程式:
煅烧时发生反应的化学方程式:(3)该流程中循环利用的物质为
(4)所得纯碱中可能含有少量NaCl杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:
i.称取ag样品,溶于水中;
ii.加入足量氯化钙溶液;
iii.过滤、洗涤、干燥、称量,所得沉淀质量为bg。
①证明步骤ⅱ中
 已经沉淀完全的方法是
已经沉淀完全的方法是②该样品中碳酸钠的质量分数为
您最近一年使用:0次
6 . 下列除去物质中的少量杂质(括号内为杂质),除杂方案或试剂正确的是
| 选项 | 物质 | 除杂方案或试剂 |
| A |  ( ( ) ) | 足量NaOH溶液 |
| B |  (HCl) (HCl) | 足量 溶液 溶液 |
| C |  溶液( 溶液( ) ) | 足量铜 |
| D |  溶液( 溶液( ) ) | 适量盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 下列实验操作正确且能达到实验目的的是
| A | B | C | D |
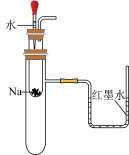 |  | 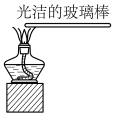 |  |
验证 和水反应放出热量 和水反应放出热量 | 配制 溶液 溶液 | 观察纯碱的焰色试验 | 比较 、 、 的稳定性 的稳定性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-02更新
|
116次组卷
|
3卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高一上学期2月期末化学试题
8 . 下列实验装置或操作中不能达到实验目的是
| A | B | C | D |
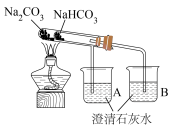 | 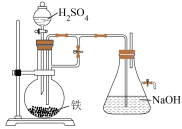 | 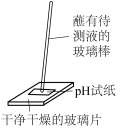 | 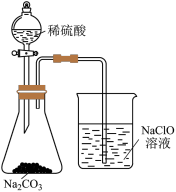 |
| 比较碳酸钠和碳酸氢钠的热稳定性 | 制备 | 检测过氧化钠与水反应后溶液酸碱性 | 验证酸性的强弱: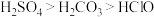 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 下列物质能通过化合反应得到的是
①FeCl2 ②Fe(OH)3 ③NaHCO3 ④FeCl3
①FeCl2 ②Fe(OH)3 ③NaHCO3 ④FeCl3
| A.全部 | B.③④ | C.①②③ | D.②③④ |
您最近一年使用:0次
2024-02-04更新
|
136次组卷
|
2卷引用:辽宁省朝阳市建平县第二高级中学2023-2024学年高一上学期1月期末化学试题
解题方法
10 . 下列有关Na2CO3和NaHCO3性质的说法中,正确的是
| A.Na2CO3和NaHCO3均可用于治疗胃酸过多 |
| B.可用加盐酸的方法除去Na2CO3粉末中混有少量的NaHCO3 |
| C.分别向Na2CO3、NaHCO3溶液中加入Ca(OH)2溶液,都产生白色沉淀 |
| D.等质量的Na2CO3和NaHCO3分别与足量盐酸反应,Na2CO3产生CO2多些 |
您最近一年使用:0次



