1 . 海洋是巨大的化学资源宝库,含有80多种元素。下图为利用海水制备部分物质的过程(已知:二氧化硫具有较强的还原性)。下列说法正确的是

| A.制取NaHCO3的反应是利用物质之间溶解度的差异实现的 |
| B.用澄清的石灰水可鉴别NaHCO3溶液和Na2CO3溶液 |
| C.在第③、④、⑤反应中,溴元素经历了被还原、被氧化、被还原的过程 |
| D.工业可利用氯碱工业原理制备金属钠 |
您最近一年使用:0次
解题方法
2 . 下列有关 和
和 的叙述正确的是
的叙述正确的是
 和
和 的叙述正确的是
的叙述正确的是A.向 溶液中逐滴加入等体积、等物质的量浓度的稀盐酸,不会生成 溶液中逐滴加入等体积、等物质的量浓度的稀盐酸,不会生成 |
B.相同条件下,等物质的量的 和 和 分别与足量盐酸反应, 分别与足量盐酸反应, 生成的 生成的 多 多 |
C. 与 与 的水溶液均显酸性 的水溶液均显酸性 |
D. 稳定性大于 稳定性大于 , , 的溶解度小于 的溶解度小于 |
您最近一年使用:0次
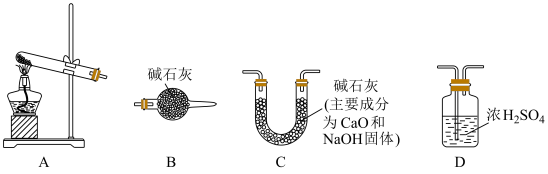
3 . 下列实验中,利用图中装置不能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 | 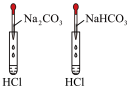 | 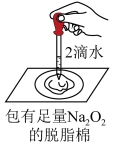 | 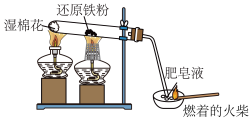 | 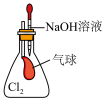 |
| 目的 | 鉴别碳酸钠和碳酸氢钠溶液 | 证明Na2O2与水反应放热 | 验证铁粉与水蒸气的反应 | 验证Cl2和NaOH溶液的反应密性 |
| 预期现象 | 滴入Na2CO3时,无明显现象,滴入NaHCO3时,立刻有气体生成 | 脱脂棉剧烈燃烧 | 肥皂液有肥皂泡冒出,点燃有爆鸣声 | 滴入氢氧化钠溶液后,气球逐渐变大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列有关钠的化合物的说法正确的是
A.用加热法除去 固体中混有的 固体中混有的 |
B. 与 与 的反应中只有氢氧化钠生成 的反应中只有氢氧化钠生成 |
| C.向酚酞溶液中加入过量的过氧化钠粉末,可以观察到:先变红,后褪色 |
| D.某溶液样品的焰色试验火焰呈黄色,证明原溶液中有钠元素,没有钾元素 |
您最近一年使用:0次
5 . 回答下列问题
(1)碳酸钠是白色粉末,俗称________ ,常温下溶解度________ (填大于、小于或等于)碳酸氢钠,水溶液呈________ (填酸性、碱性或中性);电离方程式为________ 。
(2)书写碳酸氢钠与下列物质反应的化学反应方程式:
①与盐酸反应:________ 。
②受热分解:________ 。
③与 反应:
反应:________ 。
(3)焰色试验:若要观察钾元素的焰色,需要透过________ 观察火焰颜色。
(1)碳酸钠是白色粉末,俗称
(2)书写碳酸氢钠与下列物质反应的化学反应方程式:
①与盐酸反应:
②受热分解:
③与
 反应:
反应:(3)焰色试验:若要观察钾元素的焰色,需要透过
您最近一年使用:0次
名校
解题方法
6 . Na2CO3和NaHCO3是两种重要的化工原料,二者的性质存在差异,为进一步探究其性质,请根据某实验小组的实验探究回答有关问题。
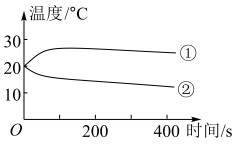
(1)分别将1.0g Na2CO3和NaHCO3的固体加入50mL盛有10mL蒸馏水的烧杯中,测定烧杯中溶液的温度变化如图所示。则曲线②代表的物质是(填化学式)______ 。
(2)如下图所示,分别向盛有10mL澄清石灰水的烧杯中加入蒸馏水和等浓度的Na2CO3、NaHCO3溶液,利用传感器测得溶液pH与加入试剂体积的变化曲线如下图所示。滴加Na2CO3溶液的烧杯中OH-未参与该反应的实验证据是___________ ;滴加NaHCO3溶液的烧杯中开始时发生反应的离子方程式为:___________ 。(提示:溶液pH越小,OH-的浓度越小,溶液碱性越弱。)

(3)某NaHCO3固体样品中含有Na2CO3杂质,某小组拟通过下列装置(气密性良好)测定CO2的质量来计算样品中NaHCO3的含量,装置的连接顺序为___→___→___→ B (每个装置仅使用一次),_____ 。经分析,上述方案存在缺陷(假定固体充分反应),会导致测定结果偏小,原因可能为:________ 。利用改进装置进行实验,ag样品加热至恒重后,称量所得固体质量为bg,则样品中NaHCO3质量分数为____ %(用含a、b的代数式表示)。
(1)分别将1.0g Na2CO3和NaHCO3的固体加入50mL盛有10mL蒸馏水的烧杯中,测定烧杯中溶液的温度变化如图所示。则曲线②代表的物质是(填化学式)

(2)如下图所示,分别向盛有10mL澄清石灰水的烧杯中加入蒸馏水和等浓度的Na2CO3、NaHCO3溶液,利用传感器测得溶液pH与加入试剂体积的变化曲线如下图所示。滴加Na2CO3溶液的烧杯中OH-未参与该反应的实验证据是

(3)某NaHCO3固体样品中含有Na2CO3杂质,某小组拟通过下列装置(气密性良好)测定CO2的质量来计算样品中NaHCO3的含量,装置的连接顺序为___→___→___→ B (每个装置仅使用一次),

您最近一年使用:0次
名校
解题方法
7 . 小组同学探究 和
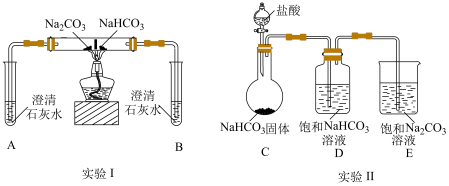
和 的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是
的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是
 和
和 的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是
的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是
| A.实验Ⅰ,A中澄清石灰水无明显变化,B中澄清石灰水变浑浊 |
B.实验Ⅱ,C中发生反应的离子方程式为: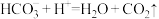 |
C.实验Ⅱ中,一段时间之后,可观察到 中有细小晶体析出 中有细小晶体析出 |
D.等物质的量的 、 、 分别与足量盐酸反应, 分别与足量盐酸反应, 生成的 生成的 更多 更多 |
您最近一年使用:0次
解题方法
8 . 室温下,下列实验探究方案不能 达到实验目的的是
选项 | 探究方案 | 探究目的 |
A | 室温下,向一定量饱和 溶液中通入足量 溶液中通入足量 气体,观察是否有晶体析出 气体,观察是否有晶体析出 | 室温下固体在水中的溶解性: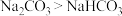 |
B | 石蜡油加强热,产生的气体通入 的 的 溶液,观察溶液是否褪色 溶液,观察溶液是否褪色 | 气体中含有不饱和烃 |
C | 用  计测量相同温度、相同浓度 计测量相同温度、相同浓度  溶液、 溶液、 溶液的 溶液的  ,比较 ,比较  大小 大小 |  的酸性比 的酸性比  的强 的强 |
D | 向 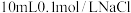 溶液中滴2滴 溶液中滴2滴 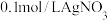 溶液,有沉淀生成,再滴入4滴 溶液,有沉淀生成,再滴入4滴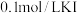 溶液,观察沉淀颜色变化 溶液,观察沉淀颜色变化 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 下列装置或操作能达到相应实验目的的是
| 选项 | A | B | C | D |
| 装置或操作 | 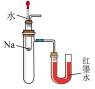 | 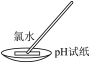 | 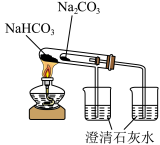 | 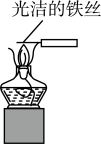 |
| 实验目的 | 验证Na与水反应放热 | 测定氯水的pH | 比较Na2CO3、NaHCO3的热稳定性 | 观察K2CO3的焰色试验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 海洋是一个巨大的化学资源宝库,其中钠元素是海洋中含量较高的元素。
(1)已知在太阳光作用下,绿色植物体内的叶绿素能将水、CO2转化为葡萄糖。海水吸收CO2并进行碳循环的原理示意图如下:
(2)某同学欲用碳酸钠晶体(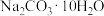 )配制220mL1mol/L的Na2CO3溶液。
)配制220mL1mol/L的Na2CO3溶液。
①所需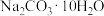 的质量为
的质量为___________ g。
②实验中除需要托盘天平(带砝码)、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器有___________ 。
③配制溶液时正确的操作顺序是:_________ (填字母,下同)
计算→称量→___________→___________→___________→___________→___________→装瓶贴标签。
a.转移 b.定容 c.摇匀 d.洗涤 e.溶解
④下列实验操作会使配制溶液浓度偏高的是___________ 。
A.容量瓶清洗后,未经过干燥处理
B.定容时,俯视刻度线
C.定容后倒转容量瓶几次,发现液面最低点低于刻度线,再补加几滴水至刻度线
D.所用碳酸钠晶体失去结晶水
(1)已知在太阳光作用下,绿色植物体内的叶绿素能将水、CO2转化为葡萄糖。海水吸收CO2并进行碳循环的原理示意图如下:
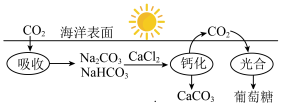
| A.CO2是碱性氧化物 |
| B.等质量的NaHCO3和Na2CO3分别与足量的盐酸反应,前者产生的二氧化碳气体较多 |
C.碳酸氢钠的电离方程式为 |
| D.该循环过程中未涉及氧化还原反应 |
(2)某同学欲用碳酸钠晶体(
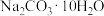 )配制220mL1mol/L的Na2CO3溶液。
)配制220mL1mol/L的Na2CO3溶液。①所需
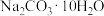 的质量为
的质量为②实验中除需要托盘天平(带砝码)、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要的玻璃仪器有
③配制溶液时正确的操作顺序是:
计算→称量→___________→___________→___________→___________→___________→装瓶贴标签。
a.转移 b.定容 c.摇匀 d.洗涤 e.溶解
④下列实验操作会使配制溶液浓度偏高的是
A.容量瓶清洗后,未经过干燥处理
B.定容时,俯视刻度线
C.定容后倒转容量瓶几次,发现液面最低点低于刻度线,再补加几滴水至刻度线
D.所用碳酸钠晶体失去结晶水
您最近一年使用:0次
2024-01-25更新
|
58次组卷
|
2卷引用:陕西省汉中市汉台区2023-2024学年高一上学期1月期末化学试题



