解题方法
1 . 下列有关 和
和 的叙述中,错误的是
的叙述中,错误的是
 和
和 的叙述中,错误的是
的叙述中,错误的是A.热稳定性: |
B.可以用澄清石灰水来鉴别 和 和 |
C.在一定的条件下, 与 与 之间可以相互转化 之间可以相互转化 |
D.等质量的 和 和 与足量盐酸反应, 与足量盐酸反应, 放出的 放出的 更多 更多 |
您最近一年使用:0次
名校
解题方法
2 . 下列关于Na2CO3、NaHCO3的叙述正确的是
①在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解
②分别向Na2CO3溶液和NaHCO3溶液中滴加少量盐酸,产生CO2气体较快的为NaHCO3溶液
③除去NaHCO3固体中的Na2CO3:将固体加热至恒重
④能用澄清石灰水鉴别Na2CO3、NaHCO3溶液
⑤相同温度下,溶解度:Na2CO3<NaHCO3
⑥物质的量相同时,消耗盐酸的量:Na2CO3>NaHCO3
①在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解
②分别向Na2CO3溶液和NaHCO3溶液中滴加少量盐酸,产生CO2气体较快的为NaHCO3溶液
③除去NaHCO3固体中的Na2CO3:将固体加热至恒重
④能用澄清石灰水鉴别Na2CO3、NaHCO3溶液
⑤相同温度下,溶解度:Na2CO3<NaHCO3
⑥物质的量相同时,消耗盐酸的量:Na2CO3>NaHCO3
| A.①③ | B.②⑥ | C.④⑤ | D.⑥ |
您最近一年使用:0次
2022-11-20更新
|
855次组卷
|
6卷引用:山东省济宁市兖州区2021-2022学年高一上学期期中考试化学试题
名校
解题方法
3 . 某小组研究Na2CO3和NaHCO3的性质,实验如下。
(1)室温下,Na2CO3的溶解度大于NaHCO3的实验证据是_______ 。
(2)根据两试管中的温度变化情况,可得出的结论是_______ 。
(3)该实验不能 说明Na2CO3溶液的碱性强于NaHCO3溶液,理由是_______ 。
| 序号 | 操作 | 现象 | |
| Na2CO3 | NaHCO3 | ||
| ① | 在两支试管中加入1g Na2CO3或1g NaHCO3,再加入5mL水,振荡;将温度计分别插入其中 | 温度由17.6℃变为23.2℃;放置至室温时,试管内无固体 | 温度由17.6℃变为17.2℃;放置至室温时,试管内有少量固体残留 |
| ② | 室温时,分别向①所得溶液中滴入2滴酚酞溶液 | 溶液变红 | 溶液微红 |
(2)根据两试管中的温度变化情况,可得出的结论是
(3)该实验
您最近一年使用:0次
名校
解题方法
4 . 为了验证Na2CO3和NaHCO3的热稳定性,按如图所示装置进行实验。相关说法不合理的是
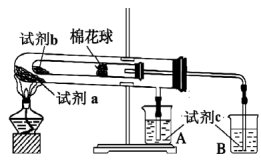

| A.试剂a为NaHCO3 | B.实验中,试剂a比试剂b的受热温度高 |
| C.试剂c为澄清石灰水 | D.一段时间后烧杯B中溶液变浑浊,A中不变浑浊。 |
您最近一年使用:0次
解题方法
5 . 某小组同学为验证NaHCO3受热分解的产物,设计如图实验(部分夹持装置已略去,气密性已检验)。

(1)实验Ⅰ中,澄清石灰水变浑浊,说明NaHCO3受热分解的产物中含有_______ 。
(2)实验Ⅰ中,加热试管a至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为Na2CO3。试剂X是_______ 。
(3)NaHCO3受热分解的化学方程式为_______ 。
(4)依据上述实验,除去Na2CO3固体中的少量NaHCO3,可采用的方法是_______ 。
(5)检验碳酸钠和碳酸氢钠溶液可以加入氯化钡溶液请写出有关化学方程式_______ 。

(1)实验Ⅰ中,澄清石灰水变浑浊,说明NaHCO3受热分解的产物中含有
(2)实验Ⅰ中,加热试管a至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为Na2CO3。试剂X是
(3)NaHCO3受热分解的化学方程式为
(4)依据上述实验,除去Na2CO3固体中的少量NaHCO3,可采用的方法是
(5)检验碳酸钠和碳酸氢钠溶液可以加入氯化钡溶液请写出有关化学方程式
您最近一年使用:0次
名校
6 . 下列方法中不能用于鉴别Na2CO3和NaHCO3的是
| A.取两种固体样品(各约1g)于试管中,分别滴加几滴水、振荡,观察现象 |
| B.配制浓度均为1mol•L-1的两种溶液,分别滴入酚酞试液,观察红色的深浅 |
| C.取固体样品分别滴入相同浓度的稀盐酸,观察产生气泡的剧烈程度 |
| D.取两种样品配成溶液,分别滴加澄清石灰水,观察是否出现白色沉淀 |
您最近一年使用:0次
2022-11-03更新
|
215次组卷
|
2卷引用:广东省广州市海珠区2020-2021学年高一上学期期末考试化学试题
名校
7 . 关于NaHCO3与Na2CO3说法正确的是
① NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火
② NaHCO3粉末中混有Na2CO3,可配置成溶液通入过量的CO2,再低温结晶得到提纯
③ Ca(HCO3)2的溶解度比CaCO3的溶解度大,因此,NaHCO3的溶解度也应该比Na2CO3的大
④Na2CO3固体中混有NaHCO3,高温灼烧即可
⑤区别NaHCO3与Na2CO3溶液,Ca(OH)2溶液和CaCl2溶液均可用
⑥等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下生成的CO2体积Na2CO3多
① NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火
② NaHCO3粉末中混有Na2CO3,可配置成溶液通入过量的CO2,再低温结晶得到提纯
③ Ca(HCO3)2的溶解度比CaCO3的溶解度大,因此,NaHCO3的溶解度也应该比Na2CO3的大
④Na2CO3固体中混有NaHCO3,高温灼烧即可
⑤区别NaHCO3与Na2CO3溶液,Ca(OH)2溶液和CaCl2溶液均可用
⑥等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下生成的CO2体积Na2CO3多
| A.①③ | B.③⑥ | C.②④ | D.②⑤ |
您最近一年使用:0次
名校
解题方法
8 . 下列说法正确的是
| A.燃烧一定要有氧气参与 |
| B.金属钠着火时,可选择用CO2灭火 |
| C.Na2O、Na2O2均属于氧化物,都能与酸性氧化物CO2反应 |
| D.Na2CO3、NaHCO3均属于可溶性盐,可用澄清石灰水鉴别 |
您最近一年使用:0次
2022-10-24更新
|
121次组卷
|
2卷引用:江苏省无锡市锡山高级中学2021-2022学年高一上学期期中考试化学试题
9 . 某小组同学探究碳酸钠的性质,请你与他们一起完成,并填空,回答问题。
(1)预测:从物质类别来看,Na2CO3属于_______ 类,可能与酸、碱、盐等类别的物质发生反应。
(2)设计实验并得出结论:
(3)问题和讨论:某化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图I-IV所示。
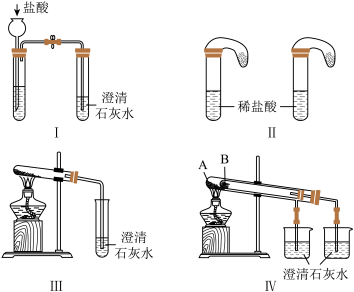
①分析图I、II所示实验,能够达到鉴别碳酸钠和碳酸氢钠目的是(填装置序号)_______ ;请说明做出判断的依据_______ 。
②图III、IV所示实验均能鉴别这两种物质,其反应的化学方程式为_______ 。
③若用实验装置IV验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是_______ 。
A.碳酸钠 B.碳酸氢钠
(1)预测:从物质类别来看,Na2CO3属于
(2)设计实验并得出结论:
| 实验步骤 | 实验现象 | 结论或解释(除④外,其他都用离子方程式表示) |
| ①向盛有Na2CO3溶液的试管中滴加澄清石灰水 | a | b |
| ②向盛有Na2CO3溶液的试管中滴加BaCl2溶液 | 产生白色沉淀 | c |
| ③向盛有Na2CO3溶液的试管中滴加稀盐酸, | 开始时无气泡产生,一段时间后产生气泡 | d、CO +H +=HCO +H +=HCO e、 |
| ④向盛有Na2CO3溶液的试管中滴加酚酞 | f | g、碳酸钠溶液显 |

①分析图I、II所示实验,能够达到鉴别碳酸钠和碳酸氢钠目的是(填装置序号)
②图III、IV所示实验均能鉴别这两种物质,其反应的化学方程式为
③若用实验装置IV验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是
A.碳酸钠 B.碳酸氢钠
您最近一年使用:0次
解题方法
10 . 以不同类别物质间的转化为线索,认识钠及其化合物。
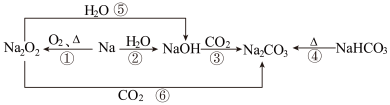
下列分析不正确 的是

下列分析
| A.反应③表明CO2具有酸性氧化物的性质 |
| B.反应④可用于鉴别碳酸钠和碳酸氢钠固体 |
| C.反应⑤、⑥可用于潜水艇中氧气的供给 |
| D.上述转化中涉及的反应类型没有置换反应 |
您最近一年使用:0次
2022-10-23更新
|
165次组卷
|
2卷引用:北京市首师附密云中学2021-2022学年高一上学期期中考试化学试题



