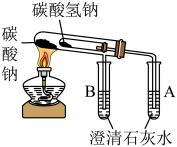
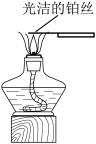
1 . 某化学兴趣小组模拟侯氏制碱法制取Na2CO3产品并回收NH4Cl,设计如下实验方案。
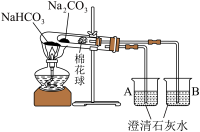
Ⅰ.NaHCO3的制备,实验装置如图甲:
②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是_____ 。
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为_____ 。
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体_____ g(保留1位小数)。
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
(5)①回收NH4Cl时加入氨水的目的是_____ 。
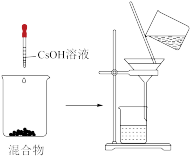
②结合图乙,简单说明操作b的过程_____ 。
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量_____ (填“大于”、“小于”或“等于”)理论上生成Na2CO3的质量。
Ⅰ.NaHCO3的制备,实验装置如图甲:

②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
| A.308K | B.373K | C.421K | D.573K |
(5)①回收NH4Cl时加入氨水的目的是
②结合图乙,简单说明操作b的过程
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量
您最近半年使用:0次
解题方法
2 . 根据下列实验事实能得出相应结论的是
选项 | 实验事实 | 结论 |
A | 向0.1 mol·L  溶液中滴加双氧水,溶液褪色 溶液中滴加双氧水,溶液褪色 |  具有漂白性 具有漂白性 |
B | 分别加热 和 和 固体,试管内壁均有水珠 固体,试管内壁均有水珠 | 两种物质均受热分解 |
C | 向水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色 溶液,呈棕黄色;煮沸,溶液变红褐色 | 升温能促进 水解 水解 |
D | 向0.1 mol·L  溶液中滴加等浓度的醋酸溶液,无明显现象 溶液中滴加等浓度的醋酸溶液,无明显现象 | 酸性: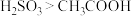 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 下列实验方法不能达到相应实验目的的是
| 选项 | 实验目的 | 实验方法 |
| A | 比较 和 和 的热稳定性 的热稳定性 | 分别加热 和 和 固体,将产生的气体通入澄清石灰水中,观察实验现象 固体,将产生的气体通入澄清石灰水中,观察实验现象 |
| B | 验证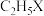 (X代表 (X代表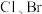 、I)中卤素原子的种类 、I)中卤素原子的种类 | 向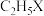 中加入过量的 中加入过量的 溶液,加热一段时间后静置,取少量上层清液于试管中,加入 溶液,加热一段时间后静置,取少量上层清液于试管中,加入 溶液,观察实验现象 溶液,观察实验现象 |
| C | 比较水分子中的氢原子和乙醇羟基中的氢原子的活泼性 | 相同条件下,用金属钠分别与水和乙醇反应,观察实验现象 |
| D | 验证葡萄糖中含有醛基 | 在试管中加入 溶液,滴入5滴 溶液,滴入5滴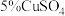 溶液,振荡后加入 溶液,振荡后加入 葡萄糖溶液,加热,观察实验现象 葡萄糖溶液,加热,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 . 下列实验操作不能达到相应实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 提纯 | 将含少量 的 的 固体溶于足量浓氨水中,过滤、洗涤、干燥 固体溶于足量浓氨水中,过滤、洗涤、干燥 |
| B | 向 溶液中滴加几滴KSCN溶液,振荡,再滴加几滴新制氯水,观察溶液颜色的变化 溶液中滴加几滴KSCN溶液,振荡,再滴加几滴新制氯水,观察溶液颜色的变化 |  的还原性比 的还原性比 的强 的强 |
| C | 室温下,向一定量饱和 溶液中通入足量 溶液中通入足量 气体,观察是否有晶体析出 气体,观察是否有晶体析出 | 室温下固体在水中的溶解性: |
| D | 用pH计测量相同温度、相同浓度NaClO溶液、 溶液的pH,比较pH大小 溶液的pH,比较pH大小 | HClO的酸性比 的强 的强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 下列实验操作和现象与所得出的结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向AlCl3溶液中逐滴加入氨水,生成白色沉淀,且沉淀不溶解 | Al(OH)3为强碱 |
| B | 鉴别等物质的量浓度的Na2CO3和NaHCO3溶液 分别滴加几滴无色酚酞溶液,溶液均变红且有一溶液红色更深 | 红色更深的是NaHCO3溶液 |
| C | 用一束光照射NaCl的乙醇溶液,侧面看到光亮通路 | NaCl的乙醇溶液是胶体 |
| D | 向某溶液中滴加BaCl2溶液,生成白色沉淀, 再加入盐酸,沉淀不溶解 | 该溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 下列说法正确的是
①Na2O2投入到紫色石蕊试液中,溶液先变蓝,后褪色;
②足量O2和质量相等的Na在常温和加热条件下反应,转移的电子数相等;
③质量相等的NaHCO3与Na2CO3分别与足量的相同浓度盐酸完全反应时,产生CO2的物质的量相等;
④取a g Al分别与等物质的量的稀盐酸或氢氧化钠溶液充分反应,生成的氢气一样多。
⑤鉴别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液;
⑥NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
⑦制取氧化铝可以向用四羟基合铝酸钠溶液中通入过量的CO2,再过滤得到氢氧化铝固体,灼烧氢氧化铝得到氧化铝。
①Na2O2投入到紫色石蕊试液中,溶液先变蓝,后褪色;
②足量O2和质量相等的Na在常温和加热条件下反应,转移的电子数相等;
③质量相等的NaHCO3与Na2CO3分别与足量的相同浓度盐酸完全反应时,产生CO2的物质的量相等;
④取a g Al分别与等物质的量的稀盐酸或氢氧化钠溶液充分反应,生成的氢气一样多。
⑤鉴别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液;
⑥NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
⑦制取氧化铝可以向用四羟基合铝酸钠溶液中通入过量的CO2,再过滤得到氢氧化铝固体,灼烧氢氧化铝得到氧化铝。
| A.②③④ | B.②⑤⑦ | C.①②⑦ | D.③④⑥ |
您最近半年使用:0次
解题方法
7 . 下列装置或操作一定能达到实验目的的是(已知: )
)
 )
)
|
|
A. 的制备 的制备 | B.验证热稳定性: |
|
|
C.除去铁红中混有的 | D.证明非金属性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 化学是一门以实验为基础的学科,如图所示的实验装置或操作能达到实验目的的是
| 选项 | A | B |
| 实验 |
|
|
| 实验目的 | 制备Fe(OH)3胶体 | 证明非金属性强弱:Cl>C>Si |
| 选项 | C | D |
| 实验 |
|
|
| 实验目的 | 比较碳酸钠和碳酸氢钠的热稳定性 | 观察K2CO3的焰色试验的现象 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
9 . 下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 取少量溶液X,向其中加入适量新制的氯水,再加几滴KSCN溶液 | 溶液颜色变红 | 溶液X含有Fe2+ |
| B | 向饱和的Na2CO3溶液通入CO2 | 产生白色沉淀 | 溶解度:NaHCO3<Na2CO3 |
| C | 向CaCl2溶液中通入适量CO2 | 产生白色沉淀 | 白色沉淀为CaCO3 |
| D | 向FeCl3溶液滴加少量酸性KMnO4溶液以检验FeCl2杂质 | 紫红色褪去 | 混合溶液中有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 碳酸钠和碳酸氢钠在日常生产生活中有着广泛应用。用如图装置探究二者的稳定性。 和
和 位置互换?
位置互换?_______ (填“能”或“不能”)。能证明 的热稳定性强于
的热稳定性强于 的实验现象是:
的实验现象是:_______
(2)除了热稳定性外,请你再设计一个实验用于鉴别 和
和 :
:_______ 。

 和
和 位置互换?
位置互换? 的热稳定性强于
的热稳定性强于 的实验现象是:
的实验现象是:(2)除了热稳定性外,请你再设计一个实验用于鉴别
 和
和 :
:
您最近半年使用:0次