名校
1 . 部分含氮物质的分类与相应氮元素的化合价关系如图所示。下列说法正确的是
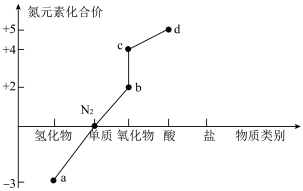
A.实验室可以通过加热固体 来制备a 来制备a |
B.C能使湿润的淀粉— 试纸变蓝 试纸变蓝 |
C.b和c都能与 溶液反应 溶液反应 |
D. 与d的浓溶液常温下不反应,故可以用铝槽车运输d的浓溶液 与d的浓溶液常温下不反应,故可以用铝槽车运输d的浓溶液 |
您最近一年使用:0次
名校
2 .  为短周期主族元素,且原子序数依次增大,A与D可形成使湿润红色石蕊试纸变蓝的气体,A与
为短周期主族元素,且原子序数依次增大,A与D可形成使湿润红色石蕊试纸变蓝的气体,A与 可形成三核
可形成三核 分子,B元素原子
分子,B元素原子 层的电子数是其
层的电子数是其 层电子数的2倍,
层电子数的2倍, 元素的焰色试验中为黄色,
元素的焰色试验中为黄色, 元素的周期数与主族序数相等,下列说法
元素的周期数与主族序数相等,下列说法不正确 的是
 为短周期主族元素,且原子序数依次增大,A与D可形成使湿润红色石蕊试纸变蓝的气体,A与
为短周期主族元素,且原子序数依次增大,A与D可形成使湿润红色石蕊试纸变蓝的气体,A与 可形成三核
可形成三核 分子,B元素原子
分子,B元素原子 层的电子数是其
层的电子数是其 层电子数的2倍,
层电子数的2倍, 元素的焰色试验中为黄色,
元素的焰色试验中为黄色, 元素的周期数与主族序数相等,下列说法
元素的周期数与主族序数相等,下列说法A.简单离子半径: |
B.最高价氧化物对应水化物的酸性: |
C.元素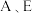 组成的化合物比例一定为 组成的化合物比例一定为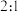 |
D. 的单质在D的最高价含氧酸的冷的浓溶液中会钝化 的单质在D的最高价含氧酸的冷的浓溶液中会钝化 |
您最近一年使用:0次
名校
解题方法
3 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计与结论都正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 检验固体样品中是否含有NH | 将固体样品加水溶解,滴入浓NaOH溶液并加热,试管口放一张湿润的红色石蕊试纸 | 湿润的红色石蕊试纸变蓝 | 样品中含有NH |
| B | 探究铝与浓硫酸的钝化现象 | 室温下,将铝片直接放入浓硫酸中,一段时间后取出并用水洗净,放入CuSO4溶液 | 铝片表面未见紫红色固体生成 | 室温下浓硫酸能将铝片钝化 |
| C | 探究Si、Cl元素非金属性的强弱 | 向Na2SiO3溶液中滴加1滴酚酞,然后逐滴加入盐酸至红色褪去 | 混合液逐渐变成白色凝胶 | 非金属性:Si<Cl |
| D | 探究浓度与反应速率的关系 | 两支试管各盛4mL 0.01mol/L酸性高锰酸钾溶液,分别加入2mL 0.1mol/L草酸溶液和2mL 0.2mol/L草酸溶液 | 加入0.2mol/L草酸溶液的试管中,高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 以下是有关铝的实验探究,请回答相关问题:
(1)用铝粉和 Fe2O3做铝热反应实验,需要的试剂还有___________。
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 Fe2O3反应的化学方程式___________ 。
(3)向集满CO2的铝制易拉罐中加入过量 NaOH 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪; 再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:___________ 。
(4)向铝粉中添加少量 NH4Cl固体并充分混合,将其加热到1000℃时可与 N₂反应制备 AlN,下列说法正确的是___________
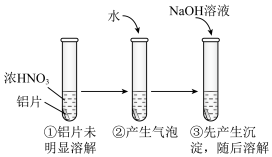
(5)用打磨过的铝片进行如下实验, 下列分析不合理的是___________
(6)为探究铝片(未打磨)与Na2CO3溶液的反应,实验如下:
下列说法不正确的是___________
(7)某铝土矿的主要成分为Al2O3·xH2O,还含有Fe2O3和 SiO2杂质。称取 17.50g铝土矿样品,加入 200mL1.65mol/L 的稀硫酸,恰好完全反应,过滤得沉淀0.30g,然后在滤液中加入足量的 NaOH 溶液,得到沉淀 2.14g。
①该试样中Fe2O3的物质的量为___________ mol。
② 样品中Al2O3·xH2O的x=__________ 。
(1)用铝粉和 Fe2O3做铝热反应实验,需要的试剂还有___________。
| A.KCl | B.KClO3 | C.MnO2 | D.Mg |
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 Fe2O3反应的化学方程式
(3)向集满CO2的铝制易拉罐中加入过量 NaOH 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪; 再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
(4)向铝粉中添加少量 NH4Cl固体并充分混合,将其加热到1000℃时可与 N₂反应制备 AlN,下列说法正确的是___________
| A.AlN是一种金属材料 |
| B.AlN与足量氢氧化钠溶液共热时生成氢氧化铝和氨气 |
| C.少量 NH4Cl能够破坏 Al表面的 Al2O3薄膜 |
| D.AlN与足量盐酸反应的离子方程式为AlN+3H+=Al3++NH3↑ |
(5)用打磨过的铝片进行如下实验, 下列分析不合理的是___________

| A.①中铝片发生了钝化 |
| B.②中产生的气泡是氮氧化合物,不是氢气 |
| C.③中沉淀溶解的离子方程式是Al(OH)3+OH-=[Al(OH)4]- |
| D.②中加水稀释过程中,仅发生了氧化还原反应 |
(6)为探究铝片(未打磨)与Na2CO3溶液的反应,实验如下:
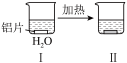 |  | |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色沉淀,产生大量气泡(经检验为H2和CO2) |
A.Na2CO3溶液中存在水解平衡:  |
| B.对比Ⅰ 、Ⅲ,推测 Na2CO3溶液能破坏铝表面的氧化膜 |
| C.Ⅳ溶液中可能存在大量 Al3+ |
D.推测出现白色浑浊的可能原因:[Al(OH)4]-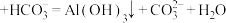 |
(7)某铝土矿的主要成分为Al2O3·xH2O,还含有Fe2O3和 SiO2杂质。称取 17.50g铝土矿样品,加入 200mL1.65mol/L 的稀硫酸,恰好完全反应,过滤得沉淀0.30g,然后在滤液中加入足量的 NaOH 溶液,得到沉淀 2.14g。
①该试样中Fe2O3的物质的量为
② 样品中Al2O3·xH2O的x=
您最近一年使用:0次
5 . 下列措施不合理 的是
| A.水泥制备时需加入石膏调节水泥硬化速率 |
| B.用硫酸清洗锅炉中的水垢 |
| C.高温下用焦炭还原SiO2制取粗硅 |
| D.常温下,用铁制或铝制容器储运浓硝酸、浓硫酸 |
您最近一年使用:0次
6 . 下列陈述Ⅰ和Ⅱ均正确但不具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 用焦炭和石英砂制取粗硅 | 石英砂硬度高 |
| B | 干冰可用在舞台上制造“云雾” | 干冰升华吸热,空气中的水蒸气迅速冷凝 |
| C | 用石英器皿盛放氢氟酸 | 二氧化硅不与强酸反应 |
| D | 用铁或铝槽车运输浓硫酸 | 冷浓硫酸与铁和铝不反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-05更新
|
278次组卷
|
3卷引用:广州市第七十五中学2023-2024学年高一下学期第一次阶段考试化学试题
7 . 对下列事实的解释错误的是
| A.在蔗糖中加入浓硫酸后出现黑色物质,说明浓硫酸具有脱水性 |
| B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 |
| C.将一块打磨过的铝片投入浓硝酸中,铝片未见溶解,铝与浓硝酸不反应 |
| D.浓硫酸露置于空气中,溶液浓度降低,是由于浓硫酸具有吸水性 |
您最近一年使用:0次
名校
8 . 根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 将一块用砂纸打磨过的铝条放入试管,再加入98%浓硫酸3mL,铝条表面无明显现象 | 铝与浓硫酸常温下不反应 |
B | 向试管中加入3mL溴水,再通入 气体,溶液橙黄色褪去 气体,溶液橙黄色褪去 |  具有漂白性 具有漂白性 |
C | 用玻璃棒蘸取浓 点到蓝色石蕊试纸上,试纸先变红色后褪色 点到蓝色石蕊试纸上,试纸先变红色后褪色 | 浓 具有酸性和强氧化性 具有酸性和强氧化性 |
D | 将溶液X与盐酸反应产生的气体通入品红溶液中,品红溶液褪色 | 溶液X中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
22-23高一下·上海浦东新·期中
名校
9 . 下列关于铝及其化合物的说法正确的是
| A.铝制餐具可长时间存放酸性或碱性食物 |
| B.铝在空气中耐腐蚀,所以铝是不活泼金属 |
| C.铝箔在空气中受热可以熔化,剧烈燃烧,产生大量的热 |
| D.常温下,可以用铝或铁制容器来盛装冷的浓硫酸或冷的浓硝酸 |
您最近一年使用:0次
10 . 下列实验操作和现象及所得到的结论均正确的是
| 实验操作和现象 | 结论 | |
| A | 向淀粉碘化钾溶液中滴加氯水后溶液变蓝 | 非金属性Cl>I |
| B | 向某溶液中加入NaOH溶液共热,产生能使湿润的蓝色石蕊试纸变红的气体 | 原溶液中有NH |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝会滴落下来 | 金属铝的熔点较低 |
| D | 将打磨的铝丝放入浓硝酸浸泡后插入CuSO4溶液中 | 铝丝上析出红色固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



