1 . 下列说法中正确的是
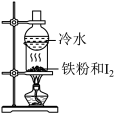

A.利用如图装置可以分离铁粉与 |
B.某物质焰色试验中,火焰呈黄色,该物质一定不含 元素 元素 |
C.室温下,实验室利用浓盐酸与 制取 制取 |
D.工业上用钠制钾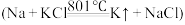 ,不能说明钠的金属性比钾强 ,不能说明钠的金属性比钾强 |
您最近一年使用:0次
2023-09-04更新
|
99次组卷
|
2卷引用:山西省部分学校2023-2024学年高三第一联考(月考)化学试题
2 . 类比法是化学研究的重要方法之一。下列类比合理的是
A. 难溶于水,则 难溶于水,则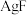 也难溶于水 也难溶于水 |
B. 与 与 反应生成 反应生成 和 和 ,则 ,则 与 与 反应生成 反应生成 和 和 |
C.工业上通过电解熔融的 冶炼 冶炼 ,则可以通过电解熔融的 ,则可以通过电解熔融的 冶炼 冶炼 |
D. 溶液与 溶液与 反应生成 反应生成 和 和 ,则 ,则 溶液与 溶液与 反应生成 反应生成 和 和 |
您最近一年使用:0次
2023-09-04更新
|
89次组卷
|
2卷引用:山西省部分学校2023-2024学年高三第一联考(月考)化学试题
名校
解题方法
3 . 分类法是化学学习和研究的重要思想方法。下列有关物质的分类正确的是
A.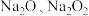 均为碱性氧化物 均为碱性氧化物 |
| B.氢氧化铁胶体为混合物 |
C. 属于钠盐、碳酸盐、正盐 属于钠盐、碳酸盐、正盐 |
| D.“蛟龙”号潜水器使用的铁合金中不含非金属元素 |
您最近一年使用:0次
2023-09-04更新
|
133次组卷
|
4卷引用:山西省部分学校2023-2024学年高三第一联考(月考)化学试题
4 . 某化学小组欲测定一份长期放置的补铁药品(有效成分是琥珀酸亚铁,化学式为FeC4H4O4)是否已变质,实验如下:
Ⅰ.取补铁药样品10.00g,碾碎,溶于100.0mL稀盐酸中,过滤,滤液呈浅黄绿色;
Ⅱ.取少量滤液,滴加KSCN溶液,溶液变为浅红色,再滴入3滴H2O2溶液,溶液红色加深;
Ⅲ.准确量取I中滤液20.00mL,加入足量H2O2溶液,再加入足量NaOH溶液,过滤、洗涤、常温晾干,获得Fe(OH)3固体0.642g;
Ⅳ.再准确量取I中滤液20.00mL于大试管中,加入1.00g铜粉,用胶塞塞紧试管口,充分振荡后过滤,最后得到干燥的铜粉0.936g。
(1)I中琥珀酸亚铁与稀盐酸反应生成FeCl2和琥珀酸(分子式为C4H6O4),说明酸性:C4H6O4_______ HCl(填“>”或“<”)。
(2)用离子方程式解释II中实验现象产生的原因:_______ 、Fe3++3SCN-=Fe(SCN)3。
(3)IV中发生反应的离子方程式为_______ 。
(4)该补铁药中琥珀酸亚铁变质程度为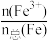 ×100%=
×100%=_______ (保留3位有效数字)。
(5)IV中溶液与铜粉反应时必须使用胶塞塞紧试管口,原因是_______ 。
Ⅰ.取补铁药样品10.00g,碾碎,溶于100.0mL稀盐酸中,过滤,滤液呈浅黄绿色;
Ⅱ.取少量滤液,滴加KSCN溶液,溶液变为浅红色,再滴入3滴H2O2溶液,溶液红色加深;
Ⅲ.准确量取I中滤液20.00mL,加入足量H2O2溶液,再加入足量NaOH溶液,过滤、洗涤、常温晾干,获得Fe(OH)3固体0.642g;
Ⅳ.再准确量取I中滤液20.00mL于大试管中,加入1.00g铜粉,用胶塞塞紧试管口,充分振荡后过滤,最后得到干燥的铜粉0.936g。
(1)I中琥珀酸亚铁与稀盐酸反应生成FeCl2和琥珀酸(分子式为C4H6O4),说明酸性:C4H6O4
(2)用离子方程式解释II中实验现象产生的原因:
(3)IV中发生反应的离子方程式为
(4)该补铁药中琥珀酸亚铁变质程度为
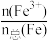 ×100%=
×100%=(5)IV中溶液与铜粉反应时必须使用胶塞塞紧试管口,原因是
您最近一年使用:0次
2023-08-26更新
|
171次组卷
|
5卷引用:山西省2023-2024学年高三上学期10月月考化学试题
名校
5 . 下列各组物质相互反应,生成物不随反应条件或反应物的用量变化而变化的是
| A.Na和O2 | B.NaOH和CO2 | C.Fe和Cl2 | D.Na2CO3和HCl |
您最近一年使用:0次
2023-07-23更新
|
273次组卷
|
4卷引用:山西省2023-2024学年高三上学期10月月考化学试题
名校
6 . 化学与生活、生产、科技、环境等密切相关。下列说法错误的是
| A.医疗上的血液透析利用了胶体的性质,土壤保肥与胶体的性质也有关 |
B.纳米铁粉通过物理吸附去除污水中 、 、 等重金属离子 等重金属离子 |
| C.北斗组网卫星使用的碳纤维是一种新型无机非金属材料 |
D.用 人工合成淀粉,有利于促进“碳中和” 人工合成淀粉,有利于促进“碳中和” |
您最近一年使用:0次
2022-11-18更新
|
142次组卷
|
3卷引用:山西省大同市2023届高三第二次学情调研测试化学试题
名校
解题方法
7 . 对下列现象或事实的解释错误的是
| 选项 | 现象或事实 | 解释 |
| A | 明矾可用于生活用水的净化 | 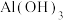 胶体具有杀菌消毒的作用 胶体具有杀菌消毒的作用 |
| B | 用铁罐贮存浓硝酸 | 常温下铁在浓硝酸中钝化 |
| C | 用氯化铁溶液蚀刻覆铜线路板 |  的氧化性比 的氧化性比 的强 的强 |
| D | 漂白粉在空气中久置变质 |  与 与 、 、 反应,生成的 反应,生成的 分解 分解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-10更新
|
230次组卷
|
3卷引用:山西省太原市2022-2023学年高三上学期期中质量监测化学试卷
8 . 向含AgNO3、Cu(NO3)2均为0.02mol的混合溶液中加入常见金属R,充分反应后过滤,得到无色溶液M与滤渣W,向W中加入盐酸得到无色气体单质,下列说法正确的是
| A.M中可能含有两种金属离子 | B.整个过程转移了0.06mol电子 |
| C.R不可能是铁但可能是锌 | D.无色溶液M一定呈中性 |
您最近一年使用:0次
2022-09-12更新
|
95次组卷
|
2卷引用:山西省晋城市第一中学2022-2023学年高三上学期第五次调研考试化学试题
名校
9 . 下列离子方程式正确的是
| A.钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
B.硅酸钠溶液与醋酸溶液混合: +2H+=H2SiO3↓ +2H+=H2SiO3↓ |
| C.室温下用稀NaOH溶液吸收Cl2:Cl2+2OH−=ClO−+Cl−+H2O |
D.浓硝酸中加入过量铁粉并加热:Fe+3 +6H+ +6H+ Fe3++3NO2↑+3H2O Fe3++3NO2↑+3H2O |
您最近一年使用:0次
2022-07-05更新
|
327次组卷
|
3卷引用:山西省长治市2022-2023学年高三上学期9月质量检测试题
山西省长治市2022-2023学年高三上学期9月质量检测试题河北省衡水市武强中学2021-2022学年高二下学期期末考试化学试题(已下线)第14讲 铁的单质、氧化物和氢氧化物(讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )
名校
10 . 设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.5.6g Fe与足量的S反应转移的电子数为0.3NA |
| B.标准状况下,1.12L苯含有C-H键的数目为0.3NA |
C.1L 0.1mol·L-1 K2Cr2O7酸性溶液(pH=4)中,Cr2O 的数目为0.1NA 的数目为0.1NA |
| D.11.2L CH4和22.4L Cl2(均为标准状况)在光照条件下充分反应后,分子总数为1.5NA |
您最近一年使用:0次
2022-03-29更新
|
1685次组卷
|
7卷引用:山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题
山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题山西省太原市2022-2023学年高三上学期期中质量监测化学试卷(已下线)专题02化学计量与化学计算-2022年高考真题+模拟题汇编(全国卷)(已下线)专题02化学计量与化学计算-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题02化学计量与化学计算-五年(2018~2022)高考真题汇编(全国卷)北京市海淀区中关村中学2022届高三下学期三模化学试题进阶训练3



