1 . 奥运会会标是五环旗,假定奥运五环旗中的每一环或每种颜色表示一种物质,相连的环(物质)间在一定条件下能发生常见反应,不相连的环(物质)间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组物质是
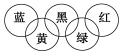

| 选项 | 蓝 | 黄 | 黑 | 绿 | 红 |
| A | SiO2 | NaOH溶液 | CuSO4溶液 | Ag | O2 |
| B | O2 | Fe | 稀硫酸 | NaOH溶液 | CO2 |
| C | Cl2 | NH3 | 稀硫酸 | NaOH溶液 | Al(OH)3 |
| D | N2 | Mg | CO2 | CaO | 稀盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 部分氧化的 Fe-Cu 合金样品(氧化物为 Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是

下列说法正确的是
| A.滤液A中的阳离子为Fe2+、Fe3+、H+ | B.溶解样品消耗的硫酸共为 0.04 mol |
| C.样品中氧元素的质量为 0.48 g | D.V=336 mL |
您最近一年使用:0次
2018-10-30更新
|
966次组卷
|
8卷引用:山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题
山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题天津市武清区杨村第三中学2019届高三上学期第一次月考化学试题黑龙江省大庆铁人中学2021-2022学年高三上学期第二次月考化学试题(已下线)一轮巩固卷5-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)考点08 物质的量在化学方程式计算中的应用(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)【浙江新东方】双师107湖南省邵阳市新邵县2022-2023学年高一上学期期末质量检测化学试题福建省泉州晋江二中、鹏峰中学、广海中学、泉港五中2022-2023学年高一下学期期中考试化学试题
3 . 将 14 g 铁粉溶于 1 L 稀硝酸中恰好完全反应,放出标准状况下 4.48 L NO 气体(假设是惟一还原产物),则原溶液中硝酸的浓度为
| A.1. 0 mol/L | B.0. 4 mol/L | C.0. 6 mol/L | D.0. 8 mol/L |
您最近一年使用:0次
2018-03-26更新
|
1002次组卷
|
4卷引用:山西省太原市2018届高三上学期期末考试化学试题
4 . 下列实验操作对应的实验现象及解释或结论不正确的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 将相同大小的金属钠分别投入乙醇和水中 | 乙醇与钠反应缓慢,水与钠反应剧烈 | 乙醇羟基中的氢原子不如水分子中的氢原子活泼 |
| B | 向 2 mL 1 mol/L NaOH 溶液中先加入3滴 1 mol/L MgCl2,再加入3滴 1 mol/L FeCl3 溶液 | 先生成白色沉淀,后生成红褐色沉淀 | 证明 Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| C | 将水蒸气通过灼热的铁粉 | 生成的气体可以点燃 | 铁与水蒸气在高温下发生反应 |
| D | 将刚摘下的红色花朵放入盛满干燥氯气的集气瓶中,盖上玻璃片 | 花朵褪色 | 因为次氯酸具有漂白作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-03-26更新
|
883次组卷
|
5卷引用:山西省太原市2018届高三上学期期末考试化学试题
名校
解题方法
5 . 某碳素钢锅炉内水垢的主要成分是碳酸钙、硫酸钙、氢氧化镁、铁锈;二氧化硅等。水垢会形成安全隐患,需及时清洗除去。清洗流程如下:
I.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤溶液,清水冲洗锅炉,加入稀盐酸,浸泡;
Ⅲ.向洗液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
已知:20℃时溶解度/g
(1)用NaOH溶解二氧化硅的化学方程式是_________
(2)在步骤Ⅱ中:①加入盐酸可除去CaCO3、Fe2O3和Mg(OH)2.写出盐酸与Mg(OH)2反应的离子方程式:___________ 。
②清洗过程中,溶解的铁锈会加速锅炉腐蚀,用离子方程式解释其原因_________
(3)步骤Ⅲ中,加入Na2SO3的目的是将步骤Ⅱ中生成的Fe3+还原成Fe2+,防止Fe3+腐蚀锅炉。写出Na2SO3和Fe3+反应的高子方程式___________ 。
(4)步骤Ⅳ中,钝化后的锅炉表面会覆盖一层致密的Fe3O4保护膜。
①如果转移的电子有2.4mol,则有________ g铁被钝化。
②钝化效果的检测一般可用滤纸浸渍配好的检测液后贴附于待测样品表面或直接将溶液涂、滴于待测表面。下面检测钝化效果的方法合理的是__________ 。
a.在炉面上滴加浓H2SO4,观察溶液出现棕黄色的时间
b.在炉面上滴加酸性CuSO4溶液,观察蓝色消失的时间
c.在炉面上滴加浓HNO3观察出现红棕色气体的时间
d.在炉面上滴加酸性K3[Fe(CN)6]溶液,观察出现蓝色沉淀的时间
I.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤溶液,清水冲洗锅炉,加入稀盐酸,浸泡;
Ⅲ.向洗液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
已知:20℃时溶解度/g
| CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
| l.4×10-3 | 2.55×10-2 | 9×10-4 | 1.1×10-2 |
(2)在步骤Ⅱ中:①加入盐酸可除去CaCO3、Fe2O3和Mg(OH)2.写出盐酸与Mg(OH)2反应的离子方程式:
②清洗过程中,溶解的铁锈会加速锅炉腐蚀,用离子方程式解释其原因
(3)步骤Ⅲ中,加入Na2SO3的目的是将步骤Ⅱ中生成的Fe3+还原成Fe2+,防止Fe3+腐蚀锅炉。写出Na2SO3和Fe3+反应的高子方程式
(4)步骤Ⅳ中,钝化后的锅炉表面会覆盖一层致密的Fe3O4保护膜。
①如果转移的电子有2.4mol,则有
②钝化效果的检测一般可用滤纸浸渍配好的检测液后贴附于待测样品表面或直接将溶液涂、滴于待测表面。下面检测钝化效果的方法合理的是
a.在炉面上滴加浓H2SO4,观察溶液出现棕黄色的时间
b.在炉面上滴加酸性CuSO4溶液,观察蓝色消失的时间
c.在炉面上滴加浓HNO3观察出现红棕色气体的时间
d.在炉面上滴加酸性K3[Fe(CN)6]溶液,观察出现蓝色沉淀的时间
您最近一年使用:0次
2012·湖北·一模
名校
6 . 已知FeS与某浓度的HNO3反应时生成Fe(NO3)3、H2SO4和某一单一的还原产物,若FeS和参与反应的HNO3的物质的量之比为1︰6,则该反应的还原产物是
| A.NO | B.NO2 | C.N2O | D.NH4NO3 |
您最近一年使用:0次
2017-11-09更新
|
568次组卷
|
6卷引用:2013届山西省平遥中学高三上学期12月质检考试化学试卷
(已下线)2013届山西省平遥中学高三上学期12月质检考试化学试卷(已下线)2012届湖北省普通高等学校招生5月适应性考试化学试卷(已下线)2012届北京市清华附中高三考前适应性训练理综化学试卷黑龙江省哈尔滨市第三中学2018届高三上学期(10月)第二次验收考试化学试题广东省清远市第一中学实验学校2020届高三第四次月考理综化学试题(已下线)上海市虹口区2014届高三三模化学试题
2012·上海普陀·二模
名校
7 . 下列解释实验过程或事实的反应方程式不正确的是
A.熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOH Na2SiO3+H2O Na2SiO3+H2O |
| B.在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+ H2O2+2H+= I2+O2↑+2H2O |
C.红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层:3Fe+ 4H2O(g) Fe3O4+4H2 Fe3O4+4H2 |
| D.“84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:ClO-+ Cl-+ 2H+= Cl2↑+H2O |
您最近一年使用:0次
2017-06-05更新
|
548次组卷
|
10卷引用:山西省实验中学2020届高三化学复习针对性试题集(六)
8 . 铁、铜混合粉末20.0g加入到100mL 5.0 mol·L-1FeCl3溶液中,剩余固体质量为5.2g(忽略反应前后溶液体积变化)。求:
(1)反应后溶液中FeCl2的物质的量浓度_____________ mol·L-1
(2)原固体混合物中铜的质量分数是_____________
(1)反应后溶液中FeCl2的物质的量浓度
(2)原固体混合物中铜的质量分数是
您最近一年使用:0次
2017-02-23更新
|
338次组卷
|
3卷引用:山西省晋中市祁县中学校2020届高三上学期10月月考化学试题
9 . 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
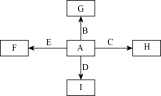
(1)① 中反应的化学方程式为________________________ ;
(2)化合物Ⅰ的电子式为____________ ,它的空间构型是______________ ;
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量_____________ (写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为___________________ ,反应后溶液与过量化合物Ⅰ反应的离子方程式为__________________ ;
(5)E在I中燃烧观察到的现象是_____________________ 。
 B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:
(1)① 中反应的化学方程式为
(2)化合物Ⅰ的电子式为
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量
(4)C与过量NaOH溶液反应的离子方程式为
(5)E在I中燃烧观察到的现象是
您最近一年使用:0次
2016-12-09更新
|
271次组卷
|
2卷引用:山西省阳高县第一中学2018届高三上学期第二次月考化学试题
10 . 已知A、B、C、D、E、F、G为中学化学中常见的化合物,其中A是淡黄色固体,B是无色液体,G为红褐色沉淀。常温下甲、乙、丙为气态非金属单质,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如下图所示(有的反应部分产物已经略去)。请根据以上信息回答下列问题:
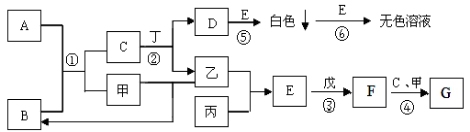
(1)写出下列物质的化学式:A____________ ,E___________ 。
(2)写出丁所含元素在周期表中的位置_______________________ 。
(3)在实验室中,欲检验F溶液中的金属阳离子,先向溶液中滴加几滴_________ 溶液,再加入几滴氯水,观察到溶液变为__________ 色,证明原溶液中的金属阳离子为___________ 。
(4)F转化为G的化学方程式:_______________________________ 。
(5)写出②中反应的离子方程式:_____________________________ 。

(1)写出下列物质的化学式:A
(2)写出丁所含元素在周期表中的位置
(3)在实验室中,欲检验F溶液中的金属阳离子,先向溶液中滴加几滴
(4)F转化为G的化学方程式:
(5)写出②中反应的离子方程式:
您最近一年使用:0次



