1 . 某企业排放的废水中含有 和
和 。为了变废为宝,技术人员计划从该废水中回收
。为了变废为宝,技术人员计划从该废水中回收 和金属Cu,工艺流程如图所示。回答下列问题:
和金属Cu,工艺流程如图所示。回答下列问题:
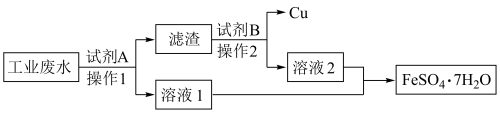
(1)“操作2”的名称为__________ ,在实验室中进行该操作时,所需要的玻璃仪器除烧杯外,还有__________ 。
(2)加入试剂A的目的是将 全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
全部转化为Cu,以便回收铜单质,发生反应的离子方程式为__________ 。
(3)合并溶液1、溶液2后,使溶液析出 晶体的实验操作是
晶体的实验操作是__________ 。
(4)A小组同学要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是__________ 。
(5)B小组同学设计如下实验,研究亚铁盐与 溶液的反应。
溶液的反应。
试剂:酸化的 溶液1和5%
溶液1和5% 溶液
溶液
①上述实验中 溶液与溶液1反应的离子方程式是
溶液与溶液1反应的离子方程式是__________ 。
②请结合相关反应解释“稍后,产生气泡”的原因是__________ 。
 和
和 。为了变废为宝,技术人员计划从该废水中回收
。为了变废为宝,技术人员计划从该废水中回收 和金属Cu,工艺流程如图所示。回答下列问题:
和金属Cu,工艺流程如图所示。回答下列问题:
(1)“操作2”的名称为
(2)加入试剂A的目的是将
 全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
全部转化为Cu,以便回收铜单质,发生反应的离子方程式为(3)合并溶液1、溶液2后,使溶液析出
 晶体的实验操作是
晶体的实验操作是(4)A小组同学要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是
(5)B小组同学设计如下实验,研究亚铁盐与
 溶液的反应。
溶液的反应。试剂:酸化的
 溶液1和5%
溶液1和5% 溶液
溶液操作 | 现象 |
取 酸化的溶液1于试管中,加入5滴5% 酸化的溶液1于试管中,加入5滴5% 溶液 溶液 | 溶液立即变为棕黄色,稍后,产生气泡 |
向反应后的溶液中加入 溶液 溶液 | 溶液变红 |
 溶液与溶液1反应的离子方程式是
溶液与溶液1反应的离子方程式是②请结合相关反应解释“稍后,产生气泡”的原因是
您最近一年使用:0次
解题方法
2 . 硫酸亚铁晶体( )在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
请回答下列问题:

(1)向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含________ (填离子符号),检验滤液中还存在 的方法为
的方法为________ (说明试剂、现象)。
(2)步骤②加入过量 的目的是
的目的是________ 。
(3)步骤③中反应的离子方程式________ 。
(4)步骤④中一系列处理的操作步骤包括:过滤、________ 、灼烧、________ 、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为________ g。
 )在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:请回答下列问题:

(1)向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含
 的方法为
的方法为(2)步骤②加入过量
 的目的是
的目的是(3)步骤③中反应的离子方程式
(4)步骤④中一系列处理的操作步骤包括:过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近一年使用:0次
3 . 高纯碳酸锰是人工合成脂肪酸时的催化剂,也可用作分析试剂、媒染剂、添加剂、药用辅料等。工业上可由软锰矿(主要成分为MnO2,含少量的Fe3O4、Al2O3、SiO2)与硫化锰(MnS)矿石制备高纯碳酸锰(MnCO3),其工艺流程如图所示:

25℃时相关物质的Ksp数据见下表:
回答下列问题:
(1)软锰矿、MnS矿石预先粉碎的目的是___________ 。H2SO4中含有的化学键的类型为___________ (填标号)。
a.离子键 b.非极性共价键 c.极性共价键
(2)“滤渣1”中含有S和___________ (填化学式),“溶浸”时二氧化锰与硫化锰反应的化学方程式为___________ 。
(3)“氧化”时加入试剂X的目的是___________ 。
(4)“调pH”的目的是___________ 。
(5)“操作1”的名称为___________ ;“操作2”为水洗,其具体操作为___________ 。
(6)“沉锰”时发生反应的离子方程式为___________ 。

25℃时相关物质的Ksp数据见下表:
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 |
(1)软锰矿、MnS矿石预先粉碎的目的是
a.离子键 b.非极性共价键 c.极性共价键
(2)“滤渣1”中含有S和
(3)“氧化”时加入试剂X的目的是
(4)“调pH”的目的是
(5)“操作1”的名称为
(6)“沉锰”时发生反应的离子方程式为
您最近一年使用:0次
4 . 某班同学用以下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁、溴化亚铁固体,均配制成 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是_____________________________________ 。
(2)甲组同学取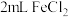 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为____________________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在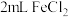 溶液中先加入
溶液中先加入 煤油,再向下层溶液中依次加入几滴氯水和1滴
煤油,再向下层溶液中依次加入几滴氯水和1滴 溶液,溶液变红。煤油的作用是
溶液,溶液变红。煤油的作用是_________________________ 。
(4)丙组同学取 上述
上述 溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1: 被
被 氧化成
氧化成 溶解在溶液中;
溶解在溶液中;
假设2: 被
被 氧化成
氧化成 。
。
请你完成下表,验证假设
(5)已知: 。若在
。若在 上述
上述 溶液中通入标准状况
溶液中通入标准状况 ,反应的离子方程式为
,反应的离子方程式为________________________________ 。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)分别取一定量氯化铁、氯化亚铁、溴化亚铁固体,均配制成
 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是(2)甲组同学取
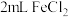 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为(3)乙组同学认为甲组的实验不够严谨,该组同学在
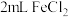 溶液中先加入
溶液中先加入 煤油,再向下层溶液中依次加入几滴氯水和1滴
煤油,再向下层溶液中依次加入几滴氯水和1滴 溶液,溶液变红。煤油的作用是
溶液,溶液变红。煤油的作用是(4)丙组同学取
 上述
上述 溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:假设1:
 被
被 氧化成
氧化成 溶解在溶液中;
溶解在溶液中;假设2:
 被
被 氧化成
氧化成 。
。请你完成下表,验证假设
| 实验步骤、预期现象 | 结论 |
| ①向溶液中加入 | 假设1正确 |
| ②向溶液中加入 | 假设2正确 |
 。若在
。若在 上述
上述 溶液中通入标准状况
溶液中通入标准状况 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次



