1 . 利用“价类二维图”可以从不同角度研究含铁物质的性质及其转化关系,图中甲~己均含铁元素。回答下列问题:

(1)甲在高温下与水蒸气反应,若生成的H2在标准状况下的体积为22.4L,则参加反应的甲的物质的量为____ 。
(2)写出检验某红色氧化物固体是否含有乙的操作____ 。
(3)K2FeO4常用作杀菌消毒剂,从化合价的角度分析是K2FeO4具有____ 性(氧化性或还原性)。用FeCl3与KClO在强碱性条件下制取K2FeO4时,该反应中氧化剂与还原剂的物质的量之比为____ 。
(4)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e-=Cu2+;还原反应为:2Fe3++2e-=2Fe2+。请据此将图中甲与盐酸反应的离子方程式拆写成两个“半反应式”,其中还原反应为____ 。

(1)甲在高温下与水蒸气反应,若生成的H2在标准状况下的体积为22.4L,则参加反应的甲的物质的量为
(2)写出检验某红色氧化物固体是否含有乙的操作
(3)K2FeO4常用作杀菌消毒剂,从化合价的角度分析是K2FeO4具有
(4)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e-=Cu2+;还原反应为:2Fe3++2e-=2Fe2+。请据此将图中甲与盐酸反应的离子方程式拆写成两个“半反应式”,其中还原反应为
您最近一年使用:0次
名校
2 . 下列操作能达到相应实验目的的是
| 实验目的 | 操作 | |
| A | 检验 溶液是否变质 溶液是否变质 | 取少量加入到酸性 溶液中 溶液中 |
| B | 测定家用84消毒液的 | 用洁净的玻璃棒蘸取少许消毒液滴在 试纸上 试纸上 |
| C | 除去 中的少量 中的少量 | 将混合气体通过盛有饱和 溶液的洗气瓶 溶液的洗气瓶 |
| D | 实验室制备 胶体 胶体 | 向沸水中逐滴加入饱和 溶液,边加边搅拌 溶液,边加边搅拌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-25更新
|
276次组卷
|
2卷引用:山东省威海市2021-2022学年高一上学期期末考试化学试题
解题方法
3 . 除去下列物质中含有的少量杂质,所选试剂错误的是
A. 溶液 溶液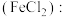 氯水 氯水 |
B. 溶液 溶液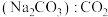 气体 气体 |
C. 溶液 溶液 粉 粉 |
D.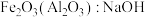 溶液 溶液 |
您最近一年使用:0次
4 . FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断正确的是
| A.溶液中一定含Cu2+ | B.溶液中不一定含Fe2+ |
| C.剩余固体一定含Cu和Fe | D.加入KSCN溶液一定不变红色 |
您最近一年使用:0次



