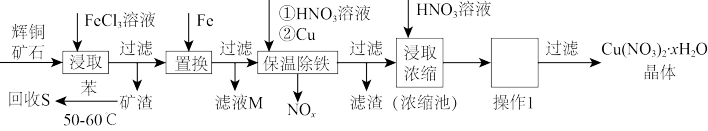
1 . 一种以辉铜矿(主要成分为Cu2S,含少量SiO2)为原料制备硝酸铜晶体的工艺流程如图所示;请回答下列问题:
(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:_______ 。
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl2是该反应的催化剂,该过程的反应原理可用化学方程式表示为:①Cu2S+2CuCl2=4CuCl+S;②_______ 。
(3)“回收S”的过程中,温度控制在50-60℃,不宜过高,原因是_______ 。
(4)向滤液M中加入(或通入)_______ (填字母),所得物质可循环利用。
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(5)“保温除铁”过程中,加入CuO的目的是____ ;向浓缩池中加入适量HNO3的作用是____ 。操作I是____ 。

(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl2是该反应的催化剂,该过程的反应原理可用化学方程式表示为:①Cu2S+2CuCl2=4CuCl+S;②
(3)“回收S”的过程中,温度控制在50-60℃,不宜过高,原因是
(4)向滤液M中加入(或通入)
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(5)“保温除铁”过程中,加入CuO的目的是
您最近一年使用:0次
2020-12-29更新
|
275次组卷
|
3卷引用:四川省凉山州西昌天立学校2022届高三上学期入学考试理综化学试题



