1 . 化合物X在一定条件下可发生如图转化,有关叙述错误的是


A.溶液C到溶液D中发生的离子方程式为:Fe3++3SCN— Fe(SCN)3 Fe(SCN)3 |
| B.E为CO,物质的量为0.05mol |
| C.X为Fe(CO)4 |
| D.过量的稀硫酸若换成盐酸,会造成环境污染 |
您最近一年使用:0次
2021-06-30更新
|
2098次组卷
|
7卷引用:辽宁省实验中学2022届高三第一次阶段性考试化学试题
辽宁省实验中学2022届高三第一次阶段性考试化学试题安徽省淮北市2021届高三第一次模拟考试化学试题(已下线)专题三 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题06 常见金属及其化合物-备战2022年高考化学学霸纠错(全国通用)(已下线)专题14物质的反应和转化-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题13物质的反应和转化-2022年高考真题+模拟题汇编(全国卷)(已下线)专题14物质的反应和转化-五年(2018~2022)高考真题汇编(全国卷)
名校
解题方法
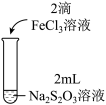
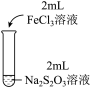
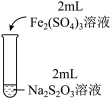
2 . 某实验小组对Na2S2O3分别与FeCl3、Fe2(SO4)3的反应进行实验探究。
实验药品:0.1mol/LNa2S2O3溶液(pH=7);0.1mol/LFeCl3溶液(pH=1);0.05mol/LFe2(SO4)3溶液(pH=1)。
实验过程
资料:ⅰ.Na2S2O3在酸性条件下不稳定,发生自身氧化还原反应;
ⅱ.Fe3++ ⇌Fe(S2O3)+(暗紫色),Fe2+遇
⇌Fe(S2O3)+(暗紫色),Fe2+遇 无明显现象
无明显现象
(1)配制FeCl3溶液时,需要用盐酸酸化,结合离子方程式解释原因:_______ 。
(2)对实验Ⅰ中现象产生的原因探究如下:
①证明有Fe2+生成:取实验Ⅰ中褪色后溶液,加入1~2滴K3[Fe(CN)6]溶液,观察到_______ 。
②实验I中紫色褪去时 被氧化成
被氧化成 ,相关反应的离子方程式是
,相关反应的离子方程式是_______ 。
③实验I和Ⅱ对比,Ⅰ中出现淡黄色浑浊,而Ⅱ中不出现淡黄色浑浊的原因是_______ 。
(3)为探究实验Ⅱ和Ⅲ中紫色褪去快慢不同的原因,设计实验如下:
①试剂X是_______ 。
②由实验Ⅳ和实验Ⅴ得出的结论是_______ 。
实验药品:0.1mol/LNa2S2O3溶液(pH=7);0.1mol/LFeCl3溶液(pH=1);0.05mol/LFe2(SO4)3溶液(pH=1)。
实验过程
| 实验编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验操作 |
|
|
|
| 实验现象 | 溶液呈紫色, 静置后紫色迅速褪去, 久置后出现淡黄色浑浊 | 溶液呈紫色, 静置后紫色褪去, 久置后不出现淡黄色浑浊 | 溶液呈紫色, 静置后紫色缓慢褪去, 久置后不出现淡黄色浑浊 |
ⅱ.Fe3++
 ⇌Fe(S2O3)+(暗紫色),Fe2+遇
⇌Fe(S2O3)+(暗紫色),Fe2+遇 无明显现象
无明显现象(1)配制FeCl3溶液时,需要用盐酸酸化,结合离子方程式解释原因:
(2)对实验Ⅰ中现象产生的原因探究如下:
①证明有Fe2+生成:取实验Ⅰ中褪色后溶液,加入1~2滴K3[Fe(CN)6]溶液,观察到
②实验I中紫色褪去时
 被氧化成
被氧化成 ,相关反应的离子方程式是
,相关反应的离子方程式是③实验I和Ⅱ对比,Ⅰ中出现淡黄色浑浊,而Ⅱ中不出现淡黄色浑浊的原因是
(3)为探究实验Ⅱ和Ⅲ中紫色褪去快慢不同的原因,设计实验如下:
| 实验编号 | Ⅳ | Ⅴ |
| 实验操作 | 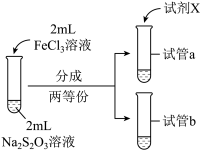 |  |
| 实验现象 | 紫色褪去时间a>b | 紫色褪去时间c<d |
②由实验Ⅳ和实验Ⅴ得出的结论是
您最近一年使用:0次
2021-01-20更新
|
1043次组卷
|
7卷引用:辽宁省葫芦岛市2021届高考第一次模拟考试化学试题
辽宁省葫芦岛市2021届高考第一次模拟考试化学试题北京市东城区2021届高三上学期期末教学统一检测化学试题(已下线)大题04 无机定量与探究实验-【考前抓大题】备战2021年高考化学(全国通用)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练北京市清华大学附属中学2022-2023学年高二上学期期末化学试题北京理工大学附属中学2023-2024学年高三上学期10月月考化学试题
名校
解题方法
3 . 电子工业上使用的印刷电路板,是在敷有铜膜的塑料板上以涂层保护所要的线路,然后用三氯化铁浓溶液作用掉(腐蚀)未受保护的铜膜后形成的。某工程师为了从使用过的腐蚀废液(含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费)中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用,准备采用下列步骤:
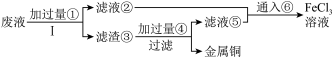
(1)写出FeCl3溶液与铜箔发生反应的离子方程式:____________ 。
(2)检验废腐蚀液中是否含有Fe3+所需试剂名称:________ ,实验现象:______________ 。
(3)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:___________ ,此转化的化学方程式为:______________ 。
(4)写出③中所含物质:________ ,⑥发生反应的离子方程式:_______ 。

(1)写出FeCl3溶液与铜箔发生反应的离子方程式:
(2)检验废腐蚀液中是否含有Fe3+所需试剂名称:
(3)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:
(4)写出③中所含物质:
您最近一年使用:0次
2020-09-04更新
|
244次组卷
|
2卷引用:辽宁省辽河油田第二高级中学2020-2021学年高一3月开学考试化学试题
11-12高一上·黑龙江绥化·期末
名校
解题方法
4 . 向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液变成红色,则下列结论错误 的是
| A.该溶液中一定含有SCN- | B.氧化性:Fe3+>Cl2 |
| C.Fe2+与SCN-不能形成红色物质 | D.Fe2+被氧化为Fe3+ |
您最近一年使用:0次
2020-08-23更新
|
983次组卷
|
25卷引用:辽宁省大石桥市第三高级中学2021-2022学年高一12月月考化学试题
辽宁省大石桥市第三高级中学2021-2022学年高一12月月考化学试题专题9 第二单元 探究铁及其化合物的转化-高中化学必修第二册苏教版20192019版鲁科化学必修第一册第3章第1节 铁的多样性课后习题山东省单县第二中学2021-2022学年高一上学期11月段考化学试题(已下线)2010-2011学年黑龙江省庆安县第三中学高一上学期期末考试化学试卷(已下线)2010—2011学江苏省扬州中学高二学业水平测试考前练习化学试卷(已下线)2011-2012学年云南省玉溪一中高一下学期期中考试化学试卷2014-2015学年山东省菏泽市高一下学期期终考试化学试卷2016-2017学年江西省南昌市第十中学高一下学期分班考试化学试卷云南省景谷一中2018-2019学年高一下学期期末考试化学试题(已下线)2019年8月5日《每日一题》2020年高考一轮复习—— Fe2+、Fe3+的检验黑龙江省安达市第七中学2019-2020学年高一上学期月考化学试题山西省应县第一中学校2019-2020学年高一上学期第四次月考化学试题广西河池市都安县第二高级中学2019-2020学年高一上学期期末考试化学试题(已下线)第03章 铁 金属材料(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)鲁科版(2019)高一必修第一册高效手册——第3章 物质的性质与转化四川省自贡市田家炳中学2020-2021学年高一12月月考化学试题(已下线)专题03 铁 金属材料-2023年高考化学一轮复习小题多维练(全国通用)天津市咸水沽第一中学2022-2023学年高三上学期学开学考试化学试题山东省枣庄市滕州市2022-2023学年高一下学期开学考试化学试题广东省韶关市武江区北江实验中学2022-2023学年高三上学期第一次月考化学试题(已下线)专题九 铁及其化合物内蒙古自治区通辽市科尔沁左翼中旗实验高级中学2023-2024学年高一上学期1月期末化学试题山东省滨州市惠民县第二中学2023-2024学年高一上学期12月月考化学试题云南省祥华教育集团2023-2024学年高一下学期5月联考化学试题