名校
1 . 下列实验设计及其对应的离子方程式均正确的是
A.将少量酸性KMnO4溶液滴入双氧水中,紫色褪去:2 +5 +5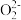 +16H+=2Mn2++5O2↑+8H2O +16H+=2Mn2++5O2↑+8H2O |
| B.Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
| C.用漂白粉溶液脱除废气中的SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
D.泡沫灭火器的工作原理:2Al3++3 +3H2O==2Al(OH)3↓+3CO2↑ +3H2O==2Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
2023-05-28更新
|
284次组卷
|
2卷引用:2024届四川省泸县第四中学高三上学期一诊模拟考试理综试题
名校
2 . 取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式为________________ ,反应后得到的溶液呈________ 色。用此溶液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为____________________________________ ,此反应属于________________ 。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈________ 色,即制得Fe(OH)3胶体。
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到__________ 烧杯中的液体产生丁达尔效应,这个实验可以用来区别________________________ 。
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
a.先出现红褐色沉淀,原因是__________________________________________ 。
b.随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:________________ 。
c.最后溶液颜色加深,原因是_________________________ (用离子方程式表示)。
d.用稀盐酸代替稀HI溶液,能出现上述哪些相同的变化现象?________ (填序号)。
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
a.先出现红褐色沉淀,原因是
b.随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:
c.最后溶液颜色加深,原因是
d.用稀盐酸代替稀HI溶液,能出现上述哪些相同的变化现象?
您最近一年使用:0次
名校
3 . 某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某化学兴趣小组对其组成进行探究。完成下列空格。
①提出假设:
假设1:只存在Fe2O3;假设2:_________ ;假设3:既存在Fe2O3也存在Cu2O。
②查找资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O。
③实验方案设计与分析:
方案一:步骤一:取少量样品于烧杯中,加入过量浓硝酸,产生一种红棕色的气体。由此可得出假设____ 不成立,写出产生上述气体的化学方程式___________________ 。
步骤二:取少量步骤一溶液置于试管中滴加_______ ,振荡,若________ ,则说明假设3成立。
方案二:
取少量样品于烧杯中,加入过量稀硫酸,若固体全部溶解,说明假设_______ 不成立。
方案三:
同学们设计了如下实验方案测定该样品中Fe2O3的质量分数(装置气密性良好,假设样品完全反应):
步骤一:取样品并称量该样品的质量为m1;
步骤二:测出反应前广口瓶和瓶内物质总质量m2;
步骤三:测出反应后广口瓶和瓶内物质总质量m3;
步骤四:计算得出矿物样品中Fe2O3的质量分数。
讨论分析:该实验方案________ (填“能”或“不能”)测出矿物中Fe2O3的质量分数。不改变装置和药品,通过计算得出矿物中Fe2O3的质量分数,你还可以通过测定_______ 。若测得m1为3.04g,m3=m2+1.76g,则原样品中Fe2O3的质量分数为_____ (结果保留四位有效数字)。
①提出假设:
假设1:只存在Fe2O3;假设2:
②查找资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O。
③实验方案设计与分析:
方案一:步骤一:取少量样品于烧杯中,加入过量浓硝酸,产生一种红棕色的气体。由此可得出假设
步骤二:取少量步骤一溶液置于试管中滴加
方案二:
取少量样品于烧杯中,加入过量稀硫酸,若固体全部溶解,说明假设
方案三:

同学们设计了如下实验方案测定该样品中Fe2O3的质量分数(装置气密性良好,假设样品完全反应):
步骤一:取样品并称量该样品的质量为m1;
步骤二:测出反应前广口瓶和瓶内物质总质量m2;
步骤三:测出反应后广口瓶和瓶内物质总质量m3;
步骤四:计算得出矿物样品中Fe2O3的质量分数。
讨论分析:该实验方案
您最近一年使用:0次
2017-03-11更新
|
696次组卷
|
2卷引用:四川省泸县第四中学2020届高三上学期期末考试理综化学试题



