解题方法
1 . 下列离子方程式的书写及评价均合理的是
| 选项 | 离子方程式 | 评价 |
| A | Fe3O4和氢碘酸反应:Fe3O4+8H+=2Fe3++Fe2++4H2O | 正确;金属氧化物和酸反应生成盐和水 |
| B | 已知Kal(H2CO3)>Ka(HClO)>Ka2(H2CO3),少量CO2 通入NaClO溶液中:  | 正确;CO2少量时生成正盐 |
| C | Mg(HCO3)2溶液与足量的NaOH溶液反应: | 正确;酸式盐与碱反应生成正盐和水 |
| D | 28 g Fe加到含1.6 mol HNO3的稀硝酸中: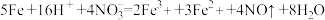 | 正确;Fe被氧化生成的Fe3+、Fe2+的物质的量之比为2:3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列实验设计及其对应的离子方程式均正确的是
A.将少量酸性KMnO4溶液滴入双氧水中,紫色褪去:2 +5 +5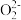 +16H+=2Mn2++5O2↑+8H2O +16H+=2Mn2++5O2↑+8H2O |
| B.Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
| C.用漂白粉溶液脱除废气中的SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
D.泡沫灭火器的工作原理:2Al3++3 +3H2O==2Al(OH)3↓+3CO2↑ +3H2O==2Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
2023-05-28更新
|
283次组卷
|
2卷引用:四川省内江市2023届高三下学期第三次模拟考试理综化学试题
名校
解题方法
3 . 下列离子方程式中,书写正确的是
A.Na2S2O3溶液中加入稀盐酸:2S2O +2H+=SO +2H+=SO +3S↓+H2O +3S↓+H2O |
| B.氯化铁溶液与适量铜粉混合:Cu+Fe3+=Cu2++Fe2+ |
C.磁性氧化铁溶于足量稀硝酸:3Fe3O4+28H++NO =9Fe3++NO↑+14H2O =9Fe3++NO↑+14H2O |
D.碳酸氢铵溶液与足量NaOH 溶液混合:HCO +OH-=CO +OH-=CO +H2O +H2O |
您最近一年使用:0次
2022-09-10更新
|
284次组卷
|
2卷引用:四川省成都市双流中学2022-2023学年高三上学期9月月考理科综合化学试题
名校
4 . 某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示。下列推断不合理的是
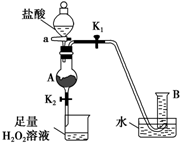

| A.烧杯中H2O2溶液的作用是将Fe2+氧化为Fe3+ |
| B.A中存在氧化铁与盐酸生成氯化铁的反应 |
| C.B中收集到的气体是氢气 |
| D.将反应后的溶液放入烧杯中再通入少量SO2, 则溶液颜色立即由棕黄色变为浅绿色 |
您最近一年使用:0次
2021-04-02更新
|
438次组卷
|
13卷引用:四川省成都市实验中学2020届高三下学期第二次周考理科综合化学试题
四川省成都市实验中学2020届高三下学期第二次周考理科综合化学试题2017届广东省深圳市三校高三上学期第一次联考化学卷(已下线)2019年4月21日 《每日一题》 三轮复习-每周一测(已下线)【南昌新东方】江西省南昌市第三中学2019-2020学年度高三上学期11月月考化学试题陕西省汉中市2022届高三第一次校际联考化学试题吉林省实验中学2017-2018学年高一上学期期末考试化学试题广东省揭阳市揭东县2020-2021学年高一上学期期末考试化学试题(已下线)【浙江新东方】双师155高一下.江苏省昆山市陆家高级中学、柏庐高级中学、周市高级中学2020-2021学年高一下学期6月联合考试化学试题安徽省涡阳一中2020-2021年高一上学期期末考试化学试题(已下线)专题六 铁及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)甘肃省会宁县第一中学2021-2022学年高一上学期期末考试化学试题山东省济宁市第一中学2022-2023学年高一上学期期末教学质量线上测试化学试题
名校
解题方法
5 . 硫化铋在光电、催化及储能方面有着广泛应用,还可用作新型锂离子电池的电极材料。以浮选过的辉铋矿(主要成分是Bi2S3,还含少量Fe2O3、SiO2等杂质)为原料制备高纯 Bi2S3的工艺流程如下:

已知:铋单质不溶于盐酸,可溶于硝酸,BiCl3极易水解生成BiOCl沉淀。
回答下列问题:
(1)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3溶液反应的离子方程式:___________ 。
(2)“浸出”时加入盐酸,既可提高铋的浸出率,又可_____ ;滤渣1的主要成分是S和______ 。
(3) “还原”过程中发生置换反应的离子是___________ ,过量的铁粉可用___________ 除去。检验过滤后的铋粉是否洗净的方法是___________ 。
(4)如把铋粉空气氧化后“酸溶”改为直接用浓硝酸氧化铋粉,不足之处是___________ 。
(5)用Bi2S3/石墨烯复合材料、高纯锂作电极,LiPF6+EC/EMC作电解液制成的电池如图所示。放电时电池的总反应为:Bi2S3+6Li=3Li2S+2Bi,电极材料中石墨烯的作用是___________ 。放电时负极的电极反应为___________ 充电时阳极的电极反应为___________ 。


已知:铋单质不溶于盐酸,可溶于硝酸,BiCl3极易水解生成BiOCl沉淀。
回答下列问题:
(1)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3溶液反应的离子方程式:
(2)“浸出”时加入盐酸,既可提高铋的浸出率,又可
(3) “还原”过程中发生置换反应的离子是
(4)如把铋粉空气氧化后“酸溶”改为直接用浓硝酸氧化铋粉,不足之处是
(5)用Bi2S3/石墨烯复合材料、高纯锂作电极,LiPF6+EC/EMC作电解液制成的电池如图所示。放电时电池的总反应为:Bi2S3+6Li=3Li2S+2Bi,电极材料中石墨烯的作用是

您最近一年使用:0次
2021-01-16更新
|
889次组卷
|
3卷引用:四川省绵阳市2021届高三第二次诊断性测试理综化学试题
四川省绵阳市2021届高三第二次诊断性测试理综化学试题 四川省眉山市彭山区第一中学2023-2024学年高三上学期开学考试理综化学试题(已下线)大题02 化学工艺流程题(二)-【考前抓大题】备战2021年高考化学(全国通用)
6 . 中国景德镇瓷器精美绝伦,瓷器表面的兔毫釉主要成分为SiO2,还含有少量Al2O3和Fe2O3。下列说法错误的是
| A.SiO2属于酸性氧化物 |
| B.景德镇瓷器不宜保存酸性或碱性太强物质 |
| C.兔毫釉极易被空气氧化,瓷器不能在空气中久置 |
| D.Al2O3中氧的质量分数高于Fe2O3 |
您最近一年使用:0次
名校
解题方法
7 . 磁性纳米Fe3O4颗粒具有超顺磁性,做固相萃取剂时能很好从水体中分离。我国科学家利用这一特性,研究出在纳米Fe3O4外包覆多巴胺聚合层,除去水体污染物多环芳烃的方法,模拟过程如下,下列有关说法正确的是
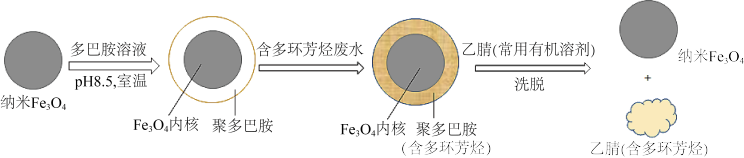

| A.Fe3O4是一种碱性氧化物 |
| B.Fe3O4纳米颗粒粒径越小、水体pH越小除污效果越好 |
| C.多环芳烃在乙腈中的溶解度小于在聚多巴胺中的溶解度 |
| D.处理完成后,Fe3O4纳米颗粒可利用磁铁回收,经加热活化可重复使用 |
您最近一年使用:0次
2020-12-27更新
|
838次组卷
|
8卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川省乐山市2021届高三12月第一次调研考试理综化学试题(已下线)热点10 新信息反应机理分析-2021年高考化学专练【热点·重点·难点】(已下线)解密01 物质的组成、分类和转化(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密01 物质的组成、分类和转化(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)【一飞冲天】8.宝坻一中三模(已下线)专题03 物质的分类和性质(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)课时03 物质的组成、分类和性质-2022年高考化学一轮复习小题多维练(全国通用)河南省鹤壁市高中2020-2021学年高二上学期第四次段考化学试题
解题方法
8 . 粉煤灰是燃煤产生的重要污染物,主要成分有Al2O3、Fe2O3、Fe3O4和SiO2等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米Fe2O3等重要物质。
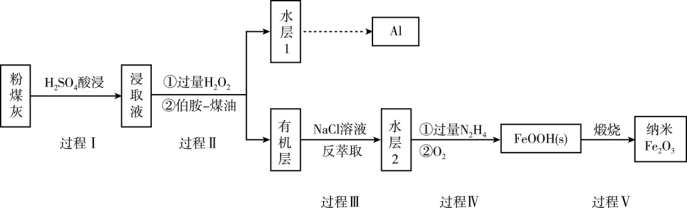
已知:
i)伯胺R-NH2能与Fe3+反应;3R-NH2+Fe3++SO42-+H2O Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物。
Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物。
ii)Fe3+在水溶液中能与Cl-反应:Fe3++6Cl- [FeCl6]3-,回答下列问题:
[FeCl6]3-,回答下列问题:
(1)过程I对煤粉灰进行酸浸过滤后,滤渣的主要成分是_________ 。
(2)写出过程II加入过量H2O2发生的离子方程式_________ 。加入伯胺-煤油对浸取液进行分离,该操作的名称是_________ 。
(3)从化学平衡角度解释过程III利用NaCl溶液进行反萃取的原理________ 。
(4)过程IV中过量的N2H4将水层2中[FeCl6]3-转化为Fe2+,得到的Fe2+再被O2氧化为FeOOH,其中第一步的离子方程式为4[FeCl6]3-+5N2H4=4Fe2++N2+.4N2H5++24Cl-,该反应中氧化剂与还原剂的物质的量之比为_________ 。
(5)在常压用纳米Fe2O3电化学法合成氨的装置如图所示。
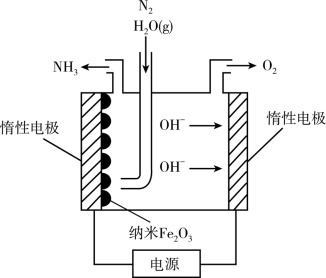
已知电解液为熔融NaOH-KOH,纳米Fe2O3在阴极发生电极反应分两步进行:该电解池第二步:2Fe+N2+3H2O=Fe2O3+2NH3。则该电解池第一步发生反应的方程式为_________ 。纳米Fe2O3在电解过程中所起的作用是_______ 。

已知:
i)伯胺R-NH2能与Fe3+反应;3R-NH2+Fe3++SO42-+H2O
 Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物。
Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物。ii)Fe3+在水溶液中能与Cl-反应:Fe3++6Cl-
 [FeCl6]3-,回答下列问题:
[FeCl6]3-,回答下列问题:(1)过程I对煤粉灰进行酸浸过滤后,滤渣的主要成分是
(2)写出过程II加入过量H2O2发生的离子方程式
(3)从化学平衡角度解释过程III利用NaCl溶液进行反萃取的原理
(4)过程IV中过量的N2H4将水层2中[FeCl6]3-转化为Fe2+,得到的Fe2+再被O2氧化为FeOOH,其中第一步的离子方程式为4[FeCl6]3-+5N2H4=4Fe2++N2+.4N2H5++24Cl-,该反应中氧化剂与还原剂的物质的量之比为
(5)在常压用纳米Fe2O3电化学法合成氨的装置如图所示。

已知电解液为熔融NaOH-KOH,纳米Fe2O3在阴极发生电极反应分两步进行:该电解池第二步:2Fe+N2+3H2O=Fe2O3+2NH3。则该电解池第一步发生反应的方程式为
您最近一年使用:0次
名校
9 . 能与稀盐酸或稀硫酸发生反应的黑色固体是
| A.MnO2 | B.石墨粉 | C.FeO | D.Fe2O3 |
您最近一年使用:0次
名校
10 . 取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式为________________ ,反应后得到的溶液呈________ 色。用此溶液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为____________________________________ ,此反应属于________________ 。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈________ 色,即制得Fe(OH)3胶体。
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到__________ 烧杯中的液体产生丁达尔效应,这个实验可以用来区别________________________ 。
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
a.先出现红褐色沉淀,原因是__________________________________________ 。
b.随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:________________ 。
c.最后溶液颜色加深,原因是_________________________ (用离子方程式表示)。
d.用稀盐酸代替稀HI溶液,能出现上述哪些相同的变化现象?________ (填序号)。
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
a.先出现红褐色沉淀,原因是
b.随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:
c.最后溶液颜色加深,原因是
d.用稀盐酸代替稀HI溶液,能出现上述哪些相同的变化现象?
您最近一年使用:0次



