四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川
高三
一模
2020-12-28
1240次
整体难度:
容易
考查范围:
常见无机物及其应用、化学实验基础、有机化学基础、认识化学科学、物质结构与性质、化学反应原理
四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川
高三
一模
2020-12-28
1240次
整体难度:
容易
考查范围:
常见无机物及其应用、化学实验基础、有机化学基础、认识化学科学、物质结构与性质、化学反应原理
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 《本草图经》在“绿矾”项载:“盖此矾色绿,味酸,烧之则赤……”,下列关于“绿矾”的说法正确的是
| A.绿矾的主要成分为Fe2(SO4)3 ·7H2O |
| B.绿矾在溶液中能电离出H+,所以“味酸” |
| C.“烧之则赤”时,绿矾被氧化 |
| D.可以用K3[Fe(CN)6]溶液检验绿矾是否已经开始变质 |
您最近一年使用:0次
2020-12-27更新
|
448次组卷
|
2卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
2. 维生素C具备抗氧化,抗自由基等作用,广泛存在于西红柿、柚子、猕猴桃等新鲜蔬菜水果中。其结构简式如图所示,下列关于维生素C的说法正确的是


| A.维生素C分子中含有醚键 |
| B.维生素C的分子式为C6H8O6 |
| C.维生素C结构中包含了一个五元碳环 |
| D.1mol维生素C最多能与2mol H2发生反应 |
您最近一年使用:0次
2020-12-27更新
|
704次组卷
|
4卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川省乐山市2021届高三12月第一次调研考试理综化学试题(已下线)热点9 陌生有机物的结构与性质分析-2021年高考化学专练【热点·重点·难点】四川省宜宾市叙州区第一中学校2022届高考三诊模拟考试理科综合化学试题辽宁省鞍山市部分普通高中2022-2023学年高二下学期第二次月考化学(B卷)试题
单选题
|
较易(0.85)
名校
3. 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.8g CH4O分子中含C−H数目为NA |
| B.常温下,36.5g HCl含有的H+ 数为0.5 NA |
| C.标准状况下,2.24LN2和O2的混合气体中分子数为0.2 NA |
| D.1mol Na与足量O2充分反应,转移的电子数为NA |
您最近一年使用:0次
2020-12-27更新
|
683次组卷
|
3卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川省乐山市2021届高三12月第一次调研考试理综化学试题(已下线)热点3 阿伏加德罗常数-2021年高考化学专练【热点·重点·难点】四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题
单选题
|
适中(0.65)
解题方法
4. 1919年,卢瑟福利用α粒子轰击短周期非金属原子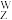 X,发现了质子,使人类对原子核的认识更进一步,其核反应原理如下:
X,发现了质子,使人类对原子核的认识更进一步,其核反应原理如下: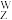 X+
X+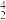 He→
He→ Y+
Y+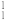 H,其中元素X的最高价氧化物对应水化物与其气态氢化物反应生成盐,下列说法中不正确的是
H,其中元素X的最高价氧化物对应水化物与其气态氢化物反应生成盐,下列说法中不正确的是
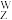 X,发现了质子,使人类对原子核的认识更进一步,其核反应原理如下:
X,发现了质子,使人类对原子核的认识更进一步,其核反应原理如下: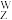 X+
X+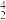 He→
He→ Y+
Y+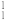 H,其中元素X的最高价氧化物对应水化物与其气态氢化物反应生成盐,下列说法中不正确的是
H,其中元素X的最高价氧化物对应水化物与其气态氢化物反应生成盐,下列说法中不正确的是| A.原子半径:X>Y | B.X的氧化物对应水化物为一元强酸 |
C. Y的中子数为9 Y的中子数为9 | D.元素X、Y能形成多种化合物 |
您最近一年使用:0次
2020-12-27更新
|
572次组卷
|
2卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
单选题
|
适中(0.65)
5. 利用压强传感器测定氨气的喷泉实验中的压强变化的装置如图1。下列说法不正确的是


| A.实验室常用加热NH4Cl与NaOH固体混合物方法制备氨气 |
| B.喷泉实验须使用干燥的NH3,实验室常用碱石灰干燥NH3 |
| C.a处的胶头滴管中装有少量的水或稀硫酸 |
| D.由图2三颈瓶中压强变化曲线可知,C点时打开止水夹b,此时喷泉最剧烈 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
6. 海水中锂资源非常丰富,但是海水中的锂浓度低,很难被提取出来。我国科学家设计了一种太阳能驱动下,利用选择性固体陶瓷膜电解海水提取金属锂的装置(示意图如图),该装置工作时,下列说法不正确的是
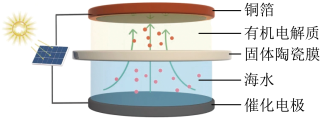

| A.工作时,铜箔作阴极 |
| B.催化电极上的电极反应式:2Cl--2e-= Cl2↑ |
| C.选择性固体陶瓷膜允许H2O通过 |
| D.该装置主要涉及的能量变化:太阳能→电能→化学能 |
【知识点】 电解池电极反应式及化学方程式的书写与判断解读
您最近一年使用:0次
2020-12-27更新
|
510次组卷
|
3卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川省乐山市2021届高三12月第一次调研考试理综化学试题河南省鹤壁市高中2020-2021学年高二上学期第四次段考化学试题(已下线)热点6 电化学及其应用-2021年高考化学专练【热点·重点·难点】
单选题
|
较易(0.85)
名校
解题方法
7. 磁性纳米Fe3O4颗粒具有超顺磁性,做固相萃取剂时能很好从水体中分离。我国科学家利用这一特性,研究出在纳米Fe3O4外包覆多巴胺聚合层,除去水体污染物多环芳烃的方法,模拟过程如下,下列有关说法正确的是
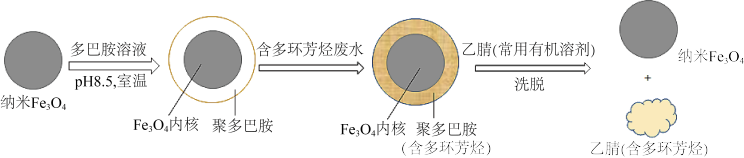

| A.Fe3O4是一种碱性氧化物 |
| B.Fe3O4纳米颗粒粒径越小、水体pH越小除污效果越好 |
| C.多环芳烃在乙腈中的溶解度小于在聚多巴胺中的溶解度 |
| D.处理完成后,Fe3O4纳米颗粒可利用磁铁回收,经加热活化可重复使用 |
您最近一年使用:0次
2020-12-27更新
|
839次组卷
|
8卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川省乐山市2021届高三12月第一次调研考试理综化学试题河南省鹤壁市高中2020-2021学年高二上学期第四次段考化学试题(已下线)热点10 新信息反应机理分析-2021年高考化学专练【热点·重点·难点】(已下线)解密01 物质的组成、分类和转化(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密01 物质的组成、分类和转化(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)【一飞冲天】8.宝坻一中三模(已下线)专题03 物质的分类和性质(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)课时03 物质的组成、分类和性质-2022年高考化学一轮复习小题多维练(全国通用)
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
8. 化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
已知:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中的其它成分与NaOH和盐酸均不反应。
I.摩擦剂中氢氧化铝的定性检验。取适量牙膏样品于烧杯中,加水充分搅拌后过滤,滤渣中加入过量NaOH溶液,过滤,向滤液中通入过量CO2有白色沉淀生成。
(1)在上述操作中,需要用到图中的实验仪器有______ (选填编号)

(2)氢氧化铝与NaOH溶液反应的离子方程式为______ ,有同学认为滤液中通CO2后有白色沉淀生成不能证明摩擦剂中一定含有Al(OH)3,若要进一步证明含Al(OH)3,需要补充的操作是______ (写出操作、现象和结论)。
Ⅱ.牙膏样品中碳酸钙的定量测定。利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
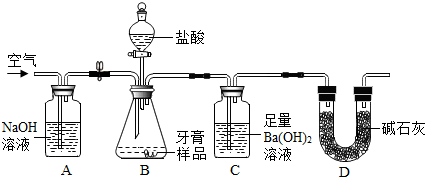
依据实验过程回答下列问题:
(3)装置A中发生反应的离子方程式为______ ,反应结束后,还要持续通一段时间空气的目的是______ 。
(4)下列各项措施中,能提高测定准确度的是______ (选填编号)。
a.把盐酸换成不具有挥发性的硫酸
b.在A~B之间增添盛有浓硫酸的干燥装置
c.滴加盐酸不宜过快
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取8.0 g样品三份,进行三次测定,测得生成BaCO3平均质量为1.97 g。则样品中碳酸钙的质量分数为______ 。
已知:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中的其它成分与NaOH和盐酸均不反应。
I.摩擦剂中氢氧化铝的定性检验。取适量牙膏样品于烧杯中,加水充分搅拌后过滤,滤渣中加入过量NaOH溶液,过滤,向滤液中通入过量CO2有白色沉淀生成。
(1)在上述操作中,需要用到图中的实验仪器有

(2)氢氧化铝与NaOH溶液反应的离子方程式为
Ⅱ.牙膏样品中碳酸钙的定量测定。利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(3)装置A中发生反应的离子方程式为
(4)下列各项措施中,能提高测定准确度的是
a.把盐酸换成不具有挥发性的硫酸
b.在A~B之间增添盛有浓硫酸的干燥装置
c.滴加盐酸不宜过快
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取8.0 g样品三份,进行三次测定,测得生成BaCO3平均质量为1.97 g。则样品中碳酸钙的质量分数为
您最近一年使用:0次
2020-12-27更新
|
552次组卷
|
5卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川省乐山市2021届高三12月第一次调研考试理综化学试题广西桂林市第十八中学2021届高三上学期第八次月考理科综合化学试题(已下线)大题04 无机定量与探究实验-【考前抓大题】备战2021年高考化学(全国通用)四川省邻水实验学校2021-2022学年高三上学期第三阶段考试理综化学试题四川省泸县第一中学2023-2024学年高三上学期10月月考理综化学试题
9. 氢气作为清洁能源有着广泛的应用前景,采用天然气制备氢气主要经历以下反应:
(i)CH4(g)+H2O(g)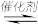 CO(g)+3H2(g) △H1
CO(g)+3H2(g) △H1
(ii)CO(g)+H2O(g)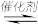 CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2
根据题给信息回答下列问题:

(1)根据图1计算△H1=___________ kJ/mol。
(2)一定温度下,恒容密闭容器中发生反应CH4(g)+H2O(g) CO(g)+3H2(g),下列叙述能说明此反应达到平衡状态的是
CO(g)+3H2(g),下列叙述能说明此反应达到平衡状态的是___________ 。
a.混合气体的密度保持不变 b.CH4和H2O(g)的浓度相等
c.v正(CO)=3v逆(H2) d.容器内气体压强不再改变
(3)通过计算机对反应(i)进行模拟实验,对0.1MPa下,不同温度,不同水碳比[(n(H2O)/n(CH4))]进行了热力学计算,绘得反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图2所示。
①由图2可知,温度一定时,H2的平衡物质的量分数与水碳比的关系是___________ ,产生该结论的原因是___________ 。
②若水碳比为1.0,平衡温度为900℃,平衡时H2的物质的量分数为0.6 [不考虑反应(ii)],则CH4的转化率为___________ %。(结果保留一位小数)
(4)可以利用电解法把反应(ii)产生的CO2和H2分离,过程如下图3,产生O2的一极是电解池的阳极,该极发生的电极反应式为___________ 。

(i)CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1
CO(g)+3H2(g) △H1(ii)CO(g)+H2O(g)
 CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2根据题给信息回答下列问题:

(1)根据图1计算△H1=
(2)一定温度下,恒容密闭容器中发生反应CH4(g)+H2O(g)
 CO(g)+3H2(g),下列叙述能说明此反应达到平衡状态的是
CO(g)+3H2(g),下列叙述能说明此反应达到平衡状态的是a.混合气体的密度保持不变 b.CH4和H2O(g)的浓度相等
c.v正(CO)=3v逆(H2) d.容器内气体压强不再改变
(3)通过计算机对反应(i)进行模拟实验,对0.1MPa下,不同温度,不同水碳比[(n(H2O)/n(CH4))]进行了热力学计算,绘得反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图2所示。

①由图2可知,温度一定时,H2的平衡物质的量分数与水碳比的关系是
②若水碳比为1.0,平衡温度为900℃,平衡时H2的物质的量分数为0.6 [不考虑反应(ii)],则CH4的转化率为
(4)可以利用电解法把反应(ii)产生的CO2和H2分离,过程如下图3,产生O2的一极是电解池的阳极,该极发生的电极反应式为

【知识点】 焓变 化学平衡状态 转化率的相关计算及判断解读 电解原理
您最近一年使用:0次
2021-01-12更新
|
57次组卷
|
3卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
解答题-工业流程题
|
较易(0.85)
解题方法
10. 硝酸铜晶体[Cu(NO3)2·6H2O],是一种重要的化工原料,常用于农药、镀铜、搪瓷等工业。以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备硝酸铜晶体的某工艺如图所示:

回答下列问题:
(1)“浸取”时,为了提高浸取率可采取的措施有______ (任写一点),浸取时在生成S的反应中还原剂与氧化剂的物质的量之比为______ 。
(2)薄层层析法是利用溶液各成分对同一吸附剂吸附能力不同,在溶液流过吸附剂时,使各成分互相分离的方法。某实验小组利用薄层层析法监控滤液1加入铁粉过程中溶液的组成,实验结果如下,则还需继续加入Fe粉的是______ (选填编号)。

(3)滤渣2的主要成分是______ ,滤渣2与稀硝酸反应时,需向装置内通入适量空气,这样做的目的是______ 。
(4)调节溶液pH时选用的物质a可以是______ ,几种金属离子沉淀的pH范围如图所示,“调pH”时应将溶液pH调至______ ~______ 。

(5)操作X主要包括______ 、______ 、过滤、洗涤、干燥。

回答下列问题:
(1)“浸取”时,为了提高浸取率可采取的措施有
(2)薄层层析法是利用溶液各成分对同一吸附剂吸附能力不同,在溶液流过吸附剂时,使各成分互相分离的方法。某实验小组利用薄层层析法监控滤液1加入铁粉过程中溶液的组成,实验结果如下,则还需继续加入Fe粉的是

(3)滤渣2的主要成分是
(4)调节溶液pH时选用的物质a可以是

(5)操作X主要包括
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
解题方法
11. 铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体。
(1)铁、钴、镍均位于元素周期表______ 区, 基态Co的价电子排布式为______ 。
(2)Fe、Co、Ni化学性质相似的原因是______ 。
(3)配位离子[Co(NO3)4]2-中,N的杂化方式为______ ,该配离子中各元素的第一电离能的大小顺序为______ ,1mol该配离子中含键数目为______ 。
(4)Ni(CO)4的结构与相关性质见表,其空间构型为______ ,晶体类型为______ 晶体。
(5)Sm(钐)、Ni、O形成的稀土镍基氧化物具有金属→绝缘体相转变特性,其晶胞结构中Sm和O如图所示,Ni位于O形成正八面体空隙中,则该稀土镍基氧化物的化学式为______ ,设晶胞边长为a pm,该稀土氧化物的摩尔质量为M g/mol,NA为阿伏加德罗常数的值,则该氧化物的密度为______ g/cm3(用含a、M、NA的式子表示)。
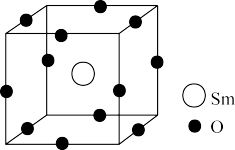
(1)铁、钴、镍均位于元素周期表
(2)Fe、Co、Ni化学性质相似的原因是
(3)配位离子[Co(NO3)4]2-中,N的杂化方式为
(4)Ni(CO)4的结构与相关性质见表,其空间构型为
| 相对分子质量 | 熔点 | 沸点 | 结构 |
| 171 | -19.3℃ | 43℃ |  |

您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
解题方法
12. 中医药是中华民族的宝库,连花清瘟胶囊由13味中药组方而成,研究表明,其中黄酮类物质(如槲皮素、木犀草素等)对COVID−19病毒有明显的抑制作用,某黄酮类化合物G的化学合成路线如图所示:
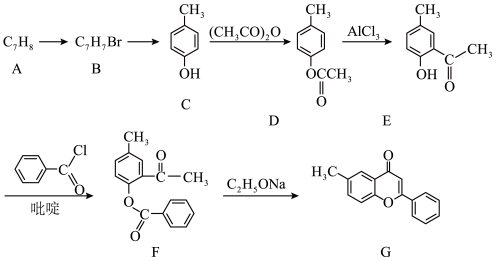
已知: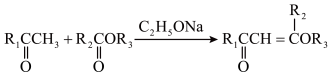 (其中R1、R2为烃基或氢原子,R3为烃基),回答下列问题:
(其中R1、R2为烃基或氢原子,R3为烃基),回答下列问题:
(1)E的分子式为______ ,其官能团的名称是______ 。
(2)A→B的反应条件为______ ,C的名称为______ 。
(3)C→D的化学方程式是______ 。
(4)已知E→F的反应为可逆反应,吡啶是一种有机碱,吡啶的作用是______ 。
(5)同时符合下列条件的E的所有同分异构体的结构共有______ 种,任写出其中一种核磁共振谱具有四组峰的结构简式______ 。
a.苯环上的一氯代物只有两种
b.既能发生银镜反应又能发生水解反应

已知:
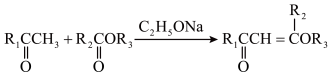 (其中R1、R2为烃基或氢原子,R3为烃基),回答下列问题:
(其中R1、R2为烃基或氢原子,R3为烃基),回答下列问题:(1)E的分子式为
(2)A→B的反应条件为
(3)C→D的化学方程式是
(4)已知E→F的反应为可逆反应,吡啶是一种有机碱,吡啶的作用是
(5)同时符合下列条件的E的所有同分异构体的结构共有
a.苯环上的一氯代物只有两种
b.既能发生银镜反应又能发生水解反应
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学实验基础、有机化学基础、认识化学科学、物质结构与性质、化学反应原理
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 亚铁盐 Fe2+的鉴别及其应用 Fe2+的还原性 物质的检验 | |
| 2 | 0.85 | 根据元素种类、原子个数、有机物类别确定分子式 常见官能团名称、组成及结构 醇类 酯的化学性质 | |
| 3 | 0.85 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 4 | 0.65 | 元素周期律、元素周期表的推断 元素周期律的应用 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | |
| 5 | 0.65 | 氨的物理性质 氨的喷泉实验 氨气的实验室制法 | |
| 6 | 0.65 | 电解池电极反应式及化学方程式的书写与判断 | |
| 7 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 几种铁的氧化物的化学性质 萃取和分液 | |
| 二、解答题 | |||
| 8 | 0.65 | 氢氧化铝 偏铝酸钠与二氧化碳的反应 探究物质组成或测量物质的含量 | 实验探究题 |
| 9 | 0.65 | 焓变 化学平衡状态 转化率的相关计算及判断 电解原理 | 原理综合题 |
| 10 | 0.85 | 氧化还原反应有关计算 沉淀溶解平衡的应用 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 11 | 0.4 | 电离能 利用杂化轨道理论判断化学键杂化类型 配合物的结构与性质 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 有机物的合成 有机合成综合考查 有机推断综合考查 信息给予的有机合成 | 有机推断题 |



