名校
1 . 下列实验设计及其对应的离子方程式均正确的是
A.将少量酸性KMnO4溶液滴入双氧水中,紫色褪去:2 +5 +5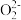 +16H+=2Mn2++5O2↑+8H2O +16H+=2Mn2++5O2↑+8H2O |
| B.Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
| C.用漂白粉溶液脱除废气中的SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
D.泡沫灭火器的工作原理:2Al3++3 +3H2O==2Al(OH)3↓+3CO2↑ +3H2O==2Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
2023-05-28更新
|
285次组卷
|
2卷引用:四川省内江市2023届高三下学期第三次模拟考试理综化学试题
名校
解题方法
2 . 硫化铋在光电、催化及储能方面有着广泛应用,还可用作新型锂离子电池的电极材料。以浮选过的辉铋矿(主要成分是Bi2S3,还含少量Fe2O3、SiO2等杂质)为原料制备高纯 Bi2S3的工艺流程如下:

已知:铋单质不溶于盐酸,可溶于硝酸,BiCl3极易水解生成BiOCl沉淀。
回答下列问题:
(1)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3溶液反应的离子方程式:___________ 。
(2)“浸出”时加入盐酸,既可提高铋的浸出率,又可_____ ;滤渣1的主要成分是S和______ 。
(3) “还原”过程中发生置换反应的离子是___________ ,过量的铁粉可用___________ 除去。检验过滤后的铋粉是否洗净的方法是___________ 。
(4)如把铋粉空气氧化后“酸溶”改为直接用浓硝酸氧化铋粉,不足之处是___________ 。
(5)用Bi2S3/石墨烯复合材料、高纯锂作电极,LiPF6+EC/EMC作电解液制成的电池如图所示。放电时电池的总反应为:Bi2S3+6Li=3Li2S+2Bi,电极材料中石墨烯的作用是___________ 。放电时负极的电极反应为___________ 充电时阳极的电极反应为___________ 。


已知:铋单质不溶于盐酸,可溶于硝酸,BiCl3极易水解生成BiOCl沉淀。
回答下列问题:
(1)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3溶液反应的离子方程式:
(2)“浸出”时加入盐酸,既可提高铋的浸出率,又可
(3) “还原”过程中发生置换反应的离子是
(4)如把铋粉空气氧化后“酸溶”改为直接用浓硝酸氧化铋粉,不足之处是
(5)用Bi2S3/石墨烯复合材料、高纯锂作电极,LiPF6+EC/EMC作电解液制成的电池如图所示。放电时电池的总反应为:Bi2S3+6Li=3Li2S+2Bi,电极材料中石墨烯的作用是

您最近一年使用:0次
2021-01-16更新
|
891次组卷
|
3卷引用:四川省绵阳市2021届高三第二次诊断性测试理综化学试题
四川省绵阳市2021届高三第二次诊断性测试理综化学试题 四川省眉山市彭山区第一中学2023-2024学年高三上学期开学考试理综化学试题(已下线)大题02 化学工艺流程题(二)-【考前抓大题】备战2021年高考化学(全国通用)
3 . 中国景德镇瓷器精美绝伦,瓷器表面的兔毫釉主要成分为SiO2,还含有少量Al2O3和Fe2O3。下列说法错误的是
| A.SiO2属于酸性氧化物 |
| B.景德镇瓷器不宜保存酸性或碱性太强物质 |
| C.兔毫釉极易被空气氧化,瓷器不能在空气中久置 |
| D.Al2O3中氧的质量分数高于Fe2O3 |
您最近一年使用:0次
名校
解题方法
4 . 磁性纳米Fe3O4颗粒具有超顺磁性,做固相萃取剂时能很好从水体中分离。我国科学家利用这一特性,研究出在纳米Fe3O4外包覆多巴胺聚合层,除去水体污染物多环芳烃的方法,模拟过程如下,下列有关说法正确的是
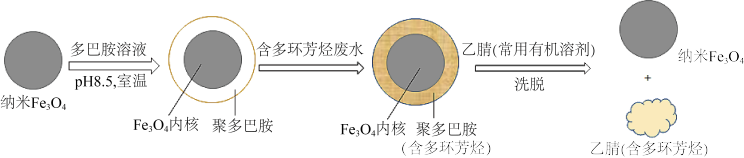

| A.Fe3O4是一种碱性氧化物 |
| B.Fe3O4纳米颗粒粒径越小、水体pH越小除污效果越好 |
| C.多环芳烃在乙腈中的溶解度小于在聚多巴胺中的溶解度 |
| D.处理完成后,Fe3O4纳米颗粒可利用磁铁回收,经加热活化可重复使用 |
您最近一年使用:0次
2020-12-27更新
|
839次组卷
|
8卷引用:四川省乐山市2021届高三12月第一次调研考试理综化学试题
四川省乐山市2021届高三12月第一次调研考试理综化学试题(已下线)【一飞冲天】8.宝坻一中三模(已下线)热点10 新信息反应机理分析-2021年高考化学专练【热点·重点·难点】(已下线)解密01 物质的组成、分类和转化(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密01 物质的组成、分类和转化(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)专题03 物质的分类和性质(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)课时03 物质的组成、分类和性质-2022年高考化学一轮复习小题多维练(全国通用)河南省鹤壁市高中2020-2021学年高二上学期第四次段考化学试题
2010·四川成都·一模
解题方法
5 . 饱和盐溶液W的电解产物发生下列系列反应。图中的每一方格表示有关的一种主要反应物或生成物(反应中加入或生成的水以及生成的其它产物已略去),其中A、B、C、D、E在常温下均为高中化学中常见气态物质,X和K是中学常见的金属单质,氧化物Y是一种比较好的耐火材料。



回答下列问题:


(1)W的名称是_______________ ,G的俗名是________________ 。
(2)A分子的空间构型是____________________ ,键角是_______ 。
(3)反应(3)的化学方程式是______________ 。反应(4)的化学方程式是__________ 。
(4)饱和盐溶液W电解的离子方程式是________________________ 。
(5)已知C的燃烧热为285.8kJ/mol。试写出C完全燃烧生成液态物质的热化学方程式__________________________ 。




回答下列问题:



(1)W的名称是
(2)A分子的空间构型是
(3)反应(3)的化学方程式是
(4)饱和盐溶液W电解的离子方程式是
(5)已知C的燃烧热为285.8kJ/mol。试写出C完全燃烧生成液态物质的热化学方程式
您最近一年使用:0次
2010·四川成都·一模
解题方法
6 . 已知D、M、H是常见的非金属单质,其中M是无色气体,H是有色气体,J是一种金属单质(其同族的某种元素是形成化合物种类最多的元素),A、C是金属氧化物,C和J均是某种常见电池的电极材料,J元素的+2价化合物比+4价化合物稳定,B与C反应时,每生成1molH同时消耗4molB和1molC,K只知含有CO或CO2中的一种或两种。它们关系如图:

(1)写出下列物质的化学式: A______________ D_______________
(2)写出下列反应的化学方程式:
②_________________________________________
⑤___________________________________
(3)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用______ 方法(填序号)
①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为______________________
(4)用C、J作电极,与硫酸构成如图所示电池,正极的电极反应为______________ ,当反应转移1mol电子时,负极质量增加_________ g。


(1)写出下列物质的化学式: A
(2)写出下列反应的化学方程式:
②
⑤
(3)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用
①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为
(4)用C、J作电极,与硫酸构成如图所示电池,正极的电极反应为

您最近一年使用:0次



