名校
解题方法
1 . 印刷电路板废液主要含 、
、 以及少量的
以及少量的 等物质,以废液为原料制备
等物质,以废液为原料制备 ,实现资源回收再利用,流程如图所示。
,实现资源回收再利用,流程如图所示。

(1)粗 溶液的制备
溶液的制备
①上述流程中能加快反应速率的措施有_______ 。
②加入铁屑后,印刷电路板废液中发生的离子反应有_______ 。
(2) 溶液的精制
溶液的精制
ⅰ.经检验,粗 溶液含有
溶液含有
ⅱ.向粗 溶液滴加3%的
溶液滴加3%的 溶液,当溶液中
溶液,当溶液中 完全氧化后,加
完全氧化后,加 粉末调节溶液的
粉末调节溶液的 。
。
ⅲ.将溶液加热至沸,趁热减压过滤,得到精制 溶液。
溶液。
①用离子方程式说明加入 溶液的作用
溶液的作用_______ 。
②已知25℃时, ,
,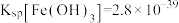 。调节溶液
。调节溶液 ,此时
,此时
_______ mol⋅L ,
, 已沉淀完全。
已沉淀完全。
③ 时判断
时判断 尚未开始沉淀,根据是此时溶液中
尚未开始沉淀,根据是此时溶液中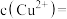
_______ mol⋅L ,与饱和溶液中
,与饱和溶液中 的物质的量浓度相比
的物质的量浓度相比_______ (填“大”“小”或“相等”)(已知25℃时 饱和溶液中
饱和溶液中 的物质的量浓度为1.41 mol⋅L
的物质的量浓度为1.41 mol⋅L )
)
 、
、 以及少量的
以及少量的 等物质,以废液为原料制备
等物质,以废液为原料制备 ,实现资源回收再利用,流程如图所示。
,实现资源回收再利用,流程如图所示。
(1)粗
 溶液的制备
溶液的制备①上述流程中能加快反应速率的措施有
②加入铁屑后,印刷电路板废液中发生的离子反应有
(2)
 溶液的精制
溶液的精制ⅰ.经检验,粗
 溶液含有
溶液含有
ⅱ.向粗
 溶液滴加3%的
溶液滴加3%的 溶液,当溶液中
溶液,当溶液中 完全氧化后,加
完全氧化后,加 粉末调节溶液的
粉末调节溶液的 。
。ⅲ.将溶液加热至沸,趁热减压过滤,得到精制
 溶液。
溶液。①用离子方程式说明加入
 溶液的作用
溶液的作用②已知25℃时,
 ,
,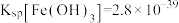 。调节溶液
。调节溶液 ,此时
,此时
 ,
, 已沉淀完全。
已沉淀完全。③
 时判断
时判断 尚未开始沉淀,根据是此时溶液中
尚未开始沉淀,根据是此时溶液中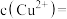
 ,与饱和溶液中
,与饱和溶液中 的物质的量浓度相比
的物质的量浓度相比 饱和溶液中
饱和溶液中 的物质的量浓度为1.41 mol⋅L
的物质的量浓度为1.41 mol⋅L )
)
您最近一年使用:0次
名校
2 . 某废催化剂含SiO2、ZnS、CuS及少量的Fe3O4.某实验小组以该废催化剂为原料,制备锌和铜的硫酸盐的结晶水合物,设计实验流程如下:
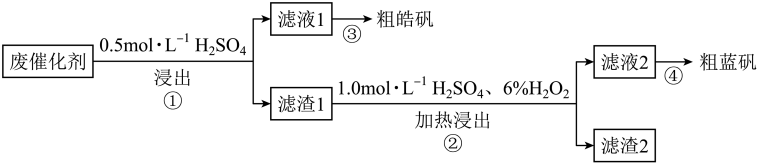
下列说法正确的是

下列说法正确的是
| A.步骤①操作中,生成的气体需用NaOH溶液或CuSO4溶液吸收 |
| B.步骤②操作中,应先加6%H2O2,然后不断搅拌下缓慢加入1.0mol·L-1H2SO4 |
| C.滤渣1成分是SiO2和CuS,滤渣2成分只有SiO2 |
| D.检验滤液1中是否含有Fe2+,可以选用KSCN溶液和新制的氯水 |
您最近一年使用:0次
2021-11-05更新
|
372次组卷
|
5卷引用: 湖南省衡阳市第一中学2021-2022学年高二下学期期末考试化学试题
湖南省衡阳市第一中学2021-2022学年高二下学期期末考试化学试题 宁夏长庆高级中学 2021-2022学年高三上学期第一次月考化学试题湖北省华中师范大学第一附属中学2020-2021学年高一下学期期中检测化学试题(已下线)【2022】【高一下】【杭师大附】【期中考】【高中化学】【洪翔峰收集】辽宁省丹东市五校2023届高三上学期第一次联考化学试题
名校
3 . Fe2(SO4)3溶液可用于腐蚀绝缘板上的铜箔,制造印刷电路板。现设计了一个方案如下,从腐蚀后的废液(主要含Fe3+、Fe2+、Cu2+)中回收铜,并重新获得Fe2(SO4)3溶液。

(1)步骤(I)中分离操作名称为____________________ 。
(2)沉淀B的主要成分有____________________ ,气体D的电子式为__________ 。
(3)写出步骤(III)中发生反应的离子方程式______________________________ 。

(1)步骤(I)中分离操作名称为
(2)沉淀B的主要成分有
(3)写出步骤(III)中发生反应的离子方程式
您最近一年使用:0次



