解题方法
1 . 攀枝花铁矿,探明储量的钒钛磁铁矿达近百亿吨,其中钒、钛储量分别占全国已探明储量的87%和94.3%,分别居世界第三位和第一位,有“世界钒钛之都”之称,是全国四大铁矿区之一,炼铁厂以磁铁矿石、焦炭、空气等为主要原料炼铁,主要反应过程如图所示:

请根据所学知识回答下列问题。
(1)磁铁矿的主要成分是___________ (填化学式),铁元素在元素周期表中位于第___________ 周期第___________ 族。
(2)生铁和钢相比,含碳量更高的是___________ 。
(3)原料中焦炭的作用是___________ 。写出反应③的化学方程式:___________ 。
(4)铁的化合物之一聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m高铁酸盐均可用作水处理剂。以绿矾(FeSO4·7H2O)为原料,可制备聚合硫酸铁和高铁酸盐。
①为检验绿矾是否变质,可采取的操作方法是___________ 。
②取2ml FeSO4溶液于试管中,向其中滴加氢氧化钠溶液,观察到生成的白色沉淀迅速变为灰绿色, 最终变为红褐色,写出此过程中涉及的氧化还原反应的化学方程式:___________ 。已知在浓碱溶液中,NaClO能将Fe(OH)3,氧化为含FeO 的紫红色溶液,请写出该过程中发生反应的离子方程式:
的紫红色溶液,请写出该过程中发生反应的离子方程式:___________ 。

请根据所学知识回答下列问题。
(1)磁铁矿的主要成分是
(2)生铁和钢相比,含碳量更高的是
(3)原料中焦炭的作用是
(4)铁的化合物之一聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m高铁酸盐均可用作水处理剂。以绿矾(FeSO4·7H2O)为原料,可制备聚合硫酸铁和高铁酸盐。
①为检验绿矾是否变质,可采取的操作方法是
②取2ml FeSO4溶液于试管中,向其中滴加氢氧化钠溶液,观察到生成的白色沉淀迅速变为灰绿色, 最终变为红褐色,写出此过程中涉及的氧化还原反应的化学方程式:
 的紫红色溶液,请写出该过程中发生反应的离子方程式:
的紫红色溶液,请写出该过程中发生反应的离子方程式:
您最近一年使用:0次
2 . 软锰矿(主要成分为 ,含有
,含有 、
、 、
、 等杂质)可以作为很多含锰化合物制备的工业原料,以其为原料制备
等杂质)可以作为很多含锰化合物制备的工业原料,以其为原料制备 (可表示为
(可表示为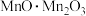 )的工艺流程如下图所示:
)的工艺流程如下图所示:

根据流程回答下列问题:
(1) 中锰元素的价态为
中锰元素的价态为___________ 。
(2)“酸浸、还原”步骤中,为加快浸取速率,可以采取的操作为___________ (至少写两条)。
(3)“氧化1”步骤中,加入 的目的是
的目的是___________ (用离子方程式表示)。
(4)“调节pH”步骤后,经过滤得到的滤渣中X的化学式为___________ 。
(5)请写出“沉锰”步骤的离子方程式:___________ 。
(6)实验表明,“沉锰”步骤中控制温度在50℃左右沉锰效果最好,温度不宜过高的原因是___________ 。
(7)“氧化2”步骤中,理论上消耗的氧化剂与还原剂的物质的量之比为___________ 。
 ,含有
,含有 、
、 、
、 等杂质)可以作为很多含锰化合物制备的工业原料,以其为原料制备
等杂质)可以作为很多含锰化合物制备的工业原料,以其为原料制备 (可表示为
(可表示为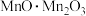 )的工艺流程如下图所示:
)的工艺流程如下图所示:
根据流程回答下列问题:
(1)
 中锰元素的价态为
中锰元素的价态为(2)“酸浸、还原”步骤中,为加快浸取速率,可以采取的操作为
(3)“氧化1”步骤中,加入
 的目的是
的目的是(4)“调节pH”步骤后,经过滤得到的滤渣中X的化学式为
(5)请写出“沉锰”步骤的离子方程式:
(6)实验表明,“沉锰”步骤中控制温度在50℃左右沉锰效果最好,温度不宜过高的原因是
(7)“氧化2”步骤中,理论上消耗的氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
名校
解题方法
3 . I.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是___________ (填化学式)。
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。
、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
②每生成2mol 转移
转移___________ mol电子,若反应过程中转移了0.5mol电子,则还原产物的物质的量为___________ mol。
II.工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
(3)试剂a是___________ ,操作I用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(4)滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________ 。
(5)上述流程中操作III包括___________ 、___________ 、过滤、洗涤。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。
、Cl-、H2O。①请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
②每生成2mol
 转移
转移II.工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
(3)试剂a是
(4)滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为
(5)上述流程中操作III包括
您最近一年使用:0次
2023-07-15更新
|
367次组卷
|
2卷引用:湖南省衡阳市2022-2023学年高一下学期期末检测化学试题
解题方法
4 . 以废铁屑(含 及少量
及少量 )为原料制备
)为原料制备 溶液的流程如下:
溶液的流程如下:
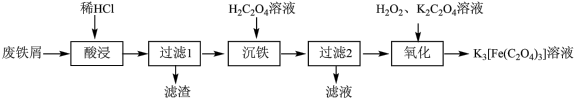
已知:①草酸 为二元弱酸
为二元弱酸
②常温下, 难溶于水。请回答相关问题:
难溶于水。请回答相关问题:
(1) 中
中 元素的化合价为
元素的化合价为_______ 。
(2)为了加快“酸浸”速率,可以采取的措施为_______ (任填一点)。
(3)“滤渣”的主要成分是_______ (填化学式)。
(4)“沉铁”时,生成 的离子方程式是
的离子方程式是_______ 。
(5)“氧化”时发生的反应为: 。该反应中氧化剂与还原剂的物质的量之比为
。该反应中氧化剂与还原剂的物质的量之比为_______ 。“氧化”结束后需要再加入适量草酸,其原因是_______ 。
(6)“过滤1”得到的滤液中的含铁盐与 反应可制备
反应可制备 ,同时可产生的气体为
,同时可产生的气体为_______ 。
 及少量
及少量 )为原料制备
)为原料制备 溶液的流程如下:
溶液的流程如下:
已知:①草酸
 为二元弱酸
为二元弱酸②常温下,
 难溶于水。请回答相关问题:
难溶于水。请回答相关问题:(1)
 中
中 元素的化合价为
元素的化合价为(2)为了加快“酸浸”速率,可以采取的措施为
(3)“滤渣”的主要成分是
(4)“沉铁”时,生成
 的离子方程式是
的离子方程式是(5)“氧化”时发生的反应为:
 。该反应中氧化剂与还原剂的物质的量之比为
。该反应中氧化剂与还原剂的物质的量之比为(6)“过滤1”得到的滤液中的含铁盐与
 反应可制备
反应可制备 ,同时可产生的气体为
,同时可产生的气体为
您最近一年使用:0次
名校
解题方法
5 . 部分氧化的Fe—Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如图处理:

下列说法不正确的是

下列说法不正确的是
| A.样品中Fe元素的质量为2.24 g |
| B.V<896 |
| C.参与反应的n(H2SO4) = 0.04 mol |
| D.滤液A中的阳离子为Fe2+、Cu2+、H+ |
您最近一年使用:0次
名校
6 . 氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2(难溶于稀硫酸)、Al2O3等,用硫酸渣制备铁红(Fe2O3)的过程如图,回答下列问题: 还有
还有___________ (填离子符号),写出Fe2O3与稀硫酸反应的离子方程式:___________ 。
(2)“还原”过程中加入FeS2粉的目的是将溶液中的Fe3+还原为Fe2+,而FeS2自身被氧化为H2SO4,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(3)“滤渣A”是SiO2,SiO2是一种常见的酸性氧化物,与CO2类似,都可与强碱反应,写出SiO2与NaOH溶液反应的化学方程式:___________ 。
(4)“氧化”时,可观察到的实验现象为___________ 。若加入的NaOH溶液过量,则“滤液B”中的溶质除了NaOH外,还含有___________ ;若加入的NaOH溶液不足,则制得的铁红中含有的杂质为___________ (填化学式)。

 还有
还有(2)“还原”过程中加入FeS2粉的目的是将溶液中的Fe3+还原为Fe2+,而FeS2自身被氧化为H2SO4,该反应中氧化剂和还原剂的物质的量之比为
(3)“滤渣A”是SiO2,SiO2是一种常见的酸性氧化物,与CO2类似,都可与强碱反应,写出SiO2与NaOH溶液反应的化学方程式:
(4)“氧化”时,可观察到的实验现象为
您最近一年使用:0次
2022-05-06更新
|
808次组卷
|
15卷引用:湖南省衡阳市祁东县2021-2022学年高一上学期期末考试化学试题
湖南省衡阳市祁东县2021-2022学年高一上学期期末考试化学试题山西省吕梁市2021-2022学年高一上学期期末考试化学试题河北省秦皇岛市2021-2022学年高一上学期期末统一考试化学试题河北省廊坊市2021-2022学年高一上学期期末统一考试化学试题湖南省怀化市沅陵县第一中学2021-2022学年高一下学期期中考试化学试题安徽省宣城中学2021-2022学年高一下学期期中考试化学试题湖南省长沙市实验中学2021-2022学年高一下学期入学考试化学试题安徽省滁州市定远县育才学校2021-2022学年高一下学期5月月考化学试题湖北省襄阳市第四中学2021-2022学年高一下学期2月考试化学试题云南省楚雄州2021-2022学年高一上学期期末教育学业质量监测化学试题湖南省长沙市实验中学2022-2023学年高一上学期期末考试化学试题河北省秦皇岛市青龙满族自治县实验中学2022-2023学年高一上学期期末考试化学试题广东省阳江市江城区部分学校2023-2024学年高一上学期期末联考化学试题(已下线)第05练 以简单工业流程突破金属及其化合物-2022年【暑假分层作业】高二化学(2023届一轮复习通用)湖南省株洲市九方中学2022-2023学年高三上学期第四次月考化学试题
7 . 高铁酸钾( )为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备
)为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备 ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
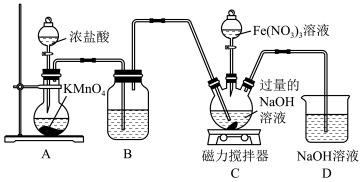
(1)装置A为 的发生装置,写出发生反应的离子方程式:
的发生装置,写出发生反应的离子方程式:_______ 。
(2)装置B中盛装的液体是_______ ,其作用为_______ 。
(3)先向装置C的三口烧瓶中通入一段时间的 制备NaClO,再滴加
制备NaClO,再滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_______ 。
(4)向装置C中通入的 不能过量,原因是
不能过量,原因是_______ 。
(5)若无装置D,可能产生的危害是_______ 。
(6)装置C中反应结束后,过滤,然后向滤液中加入饱和KOH溶液,低温析出 晶体。由此可知低温时溶解度:
晶体。由此可知低温时溶解度:
_______ (填“大于”、“小于”或“等于”) 。
。
(7)高铁酸钾( )是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成
)是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成 胶体,高铁酸钾用作水处理剂的理由是
胶体,高铁酸钾用作水处理剂的理由是_______ 。
 )为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备
)为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备 ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
(1)装置A为
 的发生装置,写出发生反应的离子方程式:
的发生装置,写出发生反应的离子方程式:(2)装置B中盛装的液体是
(3)先向装置C的三口烧瓶中通入一段时间的
 制备NaClO,再滴加
制备NaClO,再滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(4)向装置C中通入的
 不能过量,原因是
不能过量,原因是(5)若无装置D,可能产生的危害是
(6)装置C中反应结束后,过滤,然后向滤液中加入饱和KOH溶液,低温析出
 晶体。由此可知低温时溶解度:
晶体。由此可知低温时溶解度:
 。
。(7)高铁酸钾(
 )是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成
)是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成 胶体,高铁酸钾用作水处理剂的理由是
胶体,高铁酸钾用作水处理剂的理由是
您最近一年使用:0次
2022-01-19更新
|
201次组卷
|
6卷引用:湖南省衡阳市祁东县2021-2022学年高一上学期期末考试化学试题



