2020高三·全国·专题练习
1 . (1)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为________ 。(计算结果保留两位小数)
(2)为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(铁主要以Fe2O3存在)转变成重要的化工原料FeSO4(反应条件略)。

活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应。假如烧渣中的铁全部视为Fe2O3,其含量为50%。将a kg质量分数为b%的硫酸加入到c kg烧渣中浸取,铁的浸取率为96%,其它杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的硫酸忽略不计。按上述流程,第Ⅲ步应加入FeCO3________ kg。
(3)NaCN超标的电镀废水可用两段氧化法处理:NaCN与NaClO反应,生成NaOCN和NaCl,NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2。已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。处理100m3含NaCN 10.3mg/L的废水,实际至少需NaClO________ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5mg/L,达到排放标准。
(2)为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(铁主要以Fe2O3存在)转变成重要的化工原料FeSO4(反应条件略)。

活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应。假如烧渣中的铁全部视为Fe2O3,其含量为50%。将a kg质量分数为b%的硫酸加入到c kg烧渣中浸取,铁的浸取率为96%,其它杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的硫酸忽略不计。按上述流程,第Ⅲ步应加入FeCO3
(3)NaCN超标的电镀废水可用两段氧化法处理:NaCN与NaClO反应,生成NaOCN和NaCl,NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2。已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。处理100m3含NaCN 10.3mg/L的废水,实际至少需NaClO
您最近一年使用:0次
12-13高三上·上海虹口·阶段练习
2 . 钢铁工业是国家工业的基础。我国粗钢产量居世界首位。某中学社会实践活动小组利用假期对当地钢铁厂进行了调研。请对社会实践活动小组感兴趣的问题进行计算:
(1)将6.62 g铁矿石样品投入足量的盐酸中充分反应,过滤,然后在滤液中加过量的NaOH溶液反应,过滤、洗涤、灼烧得4.80 g Fe2O3。则这种铁矿石样品含铁的量为________ 克。
(2)现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00 t生铁(含铁96%),至少需要这种铁矿石___________ 吨(保留两位小数)?
(3)取某钢样粉末28.12 g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况)。
①则此钢样中铁和碳的物质的量之比________ 。
②再取三份不同质量的钢样粉末,分别加到100 mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
计算硫酸溶液的物质的量浓度_______ (要求计算过程)。
(3)若在实验Ⅱ中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少(用含m的代数式表示)_______ ?
(1)将6.62 g铁矿石样品投入足量的盐酸中充分反应,过滤,然后在滤液中加过量的NaOH溶液反应,过滤、洗涤、灼烧得4.80 g Fe2O3。则这种铁矿石样品含铁的量为
(2)现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00 t生铁(含铁96%),至少需要这种铁矿石
(3)取某钢样粉末28.12 g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况)。
①则此钢样中铁和碳的物质的量之比
②再取三份不同质量的钢样粉末,分别加到100 mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | I | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
(3)若在实验Ⅱ中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少(用含m的代数式表示)
您最近一年使用:0次
3 . 硫铁矿石(主要成分FeS2)用于工业制硫酸,其排出的矿渣在一定条件下以磁性氧化铁为主。经磁选获得精矿,可直接用于高炉炼铁。已知某精矿的主要成分是磁性氧化铁( Fe3O4)和Fe2O3及杂质(杂质不含铁、硫、氧元素,且杂质不耗氧)。请回答下列问题:
(1)某硫铁矿石中(杂质不含铁、硫)含硫的质量分数是0.360,则该硫铁矿石中含铁元素的质量分数是________ (答案用小数表示,保留3位小数)。
(2)如用上述硫铁矿石制硫酸,矿渣经磁选获得精矿,直接用于高炉炼铁,当制得98.0%的硫酸1.92吨时(不考虑硫的损失),则炼铁厂(不计选矿及炼铁时铁的损耗)最多可生产含碳4.00%的生铁____ 吨(答案保留3位小数)。
(3)煅烧硫铁矿常用富氧空气。从沸腾炉排出的气体成分如下表。如果精矿中铁、氧的物质的量之比为n (Fe):n(O)=5:7,则富氧空气中O2和N2的体积比(最简单的整数比)为_________ 。
(4)炼铁厂生产的生铁常用于炼钢。取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况下)。
①计算此钢样粉末中铁和碳的物质的量之比为________ (最简单的整数比)。
②再取三份不同质量的上述钢样粉末分别加到100mL相同浓度的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
则该硫酸溶液的物质的量浓度为________________ 。
③若在上述实验II中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少?(写出必要的步骤,答案保留3位小数)_______________ 。
(1)某硫铁矿石中(杂质不含铁、硫)含硫的质量分数是0.360,则该硫铁矿石中含铁元素的质量分数是
(2)如用上述硫铁矿石制硫酸,矿渣经磁选获得精矿,直接用于高炉炼铁,当制得98.0%的硫酸1.92吨时(不考虑硫的损失),则炼铁厂(不计选矿及炼铁时铁的损耗)最多可生产含碳4.00%的生铁
(3)煅烧硫铁矿常用富氧空气。从沸腾炉排出的气体成分如下表。如果精矿中铁、氧的物质的量之比为n (Fe):n(O)=5:7,则富氧空气中O2和N2的体积比(最简单的整数比)为
| 气体 | SO2 | N2 | O2 |
| 物质的量 | 10 | 58 | 6 |
(4)炼铁厂生产的生铁常用于炼钢。取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况下)。
①计算此钢样粉末中铁和碳的物质的量之比为
②再取三份不同质量的上述钢样粉末分别加到100mL相同浓度的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | I | II | III |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
则该硫酸溶液的物质的量浓度为
③若在上述实验II中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少?(写出必要的步骤,答案保留3位小数)
您最近一年使用:0次
13-14高二·上海金山·阶段练习
4 . 铁是一种典型的过渡元素,铁和铁的化合物在生产和生活中有广泛的应用。完成下列计算:
(1)28g铁粉与足量稀硫酸完全反应,生成氢气_________ mol。
(2)将5.72 g钢样粉末(只含铁和碳)高温下置于足量的纯氧中完全反应,生成二氧化碳224 mL(标准状况),则钢样中铁的质量分数为________ 。
(3)若将28.12 g还原铁粉(含少量FexC)在氧气流中加热,得到标准状况下的CO2 224 mL;将相同质量的还原铁粉与足量硫酸反应,得到标准状况下的H2 10.752 L,计算FexC的化学式。_____
(1)28g铁粉与足量稀硫酸完全反应,生成氢气
(2)将5.72 g钢样粉末(只含铁和碳)高温下置于足量的纯氧中完全反应,生成二氧化碳224 mL(标准状况),则钢样中铁的质量分数为
(3)若将28.12 g还原铁粉(含少量FexC)在氧气流中加热,得到标准状况下的CO2 224 mL;将相同质量的还原铁粉与足量硫酸反应,得到标准状况下的H2 10.752 L,计算FexC的化学式。
您最近一年使用:0次
18-19高二·浙江·期中
5 . 化合物甲(由Fe、Mg、H组成)是一种抗磁性的的储氢材料,M=110gmol-1,取5.5g甲在隔绝空气下加热得到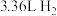 (标准状况下)和由两种金属单质组成的固体X,将固体X溶于足量盐酸,再加入足量
(标准状况下)和由两种金属单质组成的固体X,将固体X溶于足量盐酸,再加入足量 液,过滤、洗涤、干燥、灼烧得到化合物乙4.0g和化合物丙,化合物乙可用作红色的颜料,化合物丙可用作耐高温材料,请计算
液,过滤、洗涤、干燥、灼烧得到化合物乙4.0g和化合物丙,化合物乙可用作红色的颜料,化合物丙可用作耐高温材料,请计算
(1)固体X的质量为_______ g
(2)该化合物甲中Fe和Mg的原子个数比为_______ .
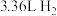 (标准状况下)和由两种金属单质组成的固体X,将固体X溶于足量盐酸,再加入足量
(标准状况下)和由两种金属单质组成的固体X,将固体X溶于足量盐酸,再加入足量 液,过滤、洗涤、干燥、灼烧得到化合物乙4.0g和化合物丙,化合物乙可用作红色的颜料,化合物丙可用作耐高温材料,请计算
液,过滤、洗涤、干燥、灼烧得到化合物乙4.0g和化合物丙,化合物乙可用作红色的颜料,化合物丙可用作耐高温材料,请计算(1)固体X的质量为
(2)该化合物甲中Fe和Mg的原子个数比为
您最近一年使用:0次
真题
6 . 钢铁工业是国家工业的基础。2006年我国粗钢产量突破4亿t,居世界首位。某中学社会实践活动小组利用假期对当地钢铁厂进行了调研,对从矿石开始到钢铁产出的工艺流程有了全面的感性认识。请您对社会实践活动小组感兴趣的问题进行计算:
(1)将6.62g铁矿石样品投入适量的盐酸中(充分反应),过滤,然后在滤液中加过量的NaOH溶液,充分反应后,过滤、洗涤、灼烧得4.80g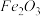 。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
(2)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到 气体224mL。(标准状况)。
气体224mL。(标准状况)。
①计算此钢样粉末中铁和碳的物质的量之比。
②再取三份不同质量的钢样粉末分别加到l00mL相同浓度的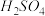 溶液中,充分反应后,测得的实验数据如下表所示:
溶液中,充分反应后,测得的实验数据如下表所示:
计算硫酸溶液的物质的量浓度。
③若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
(1)将6.62g铁矿石样品投入适量的盐酸中(充分反应),过滤,然后在滤液中加过量的NaOH溶液,充分反应后,过滤、洗涤、灼烧得4.80g
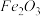 。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)(2)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到
 气体224mL。(标准状况)。
气体224mL。(标准状况)。①计算此钢样粉末中铁和碳的物质的量之比。
②再取三份不同质量的钢样粉末分别加到l00mL相同浓度的
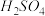 溶液中,充分反应后,测得的实验数据如下表所示:
溶液中,充分反应后,测得的实验数据如下表所示:实验序号 | I | Ⅱ | Ⅲ |
加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
计算硫酸溶液的物质的量浓度。
③若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
您最近一年使用:0次



