解题方法
1 . 钠、铁及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
① 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是___________ 。
② 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是___________ (填“还原产物”或“氧化产物”)。
(2)铁及其重要化合物之间的部分转化关系如图所示。___________ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的___________ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为___________ 。
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为___________ ,此过程中发生的氧化还原反应为(用化学方程式表达)___________ 。
(1)某汽车安全气囊的产气药剂主要含有
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。①
 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是②
 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是(2)铁及其重要化合物之间的部分转化关系如图所示。
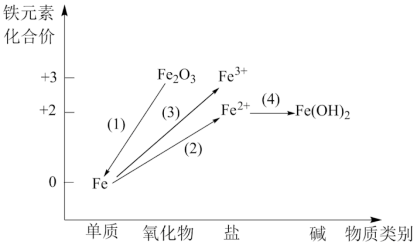
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
您最近一年使用:0次
2 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近一年使用:0次
3 . 将下列有关铁及其化合物的性质或用途的字母序号与所对应的物质对应起来:
A.具有磁性的黑色固体;B.用于治疗缺铁性贫血;C.涂料中的红色颜料;D.用于保存亚铁盐溶液;E.在空气中很不稳定;F.遇KSCN溶液变色
(1)铁单质
(2)三氧化二铁
(3)四氧化三铁
(4)氢氧化亚铁
(5)亚铁盐
(6)铁盐
您最近一年使用:0次
4 . 将下列有关铁及其化合物的性质或用途与所对应的物质连接起来________ 。
具有磁性的黑色固体 铁单质
用于治疗缺铁性贫血 三氧化二铁
涂料中的红色颜料 四氧化三铁
用于保存亚铁盐溶液 氢氧化亚铁
在空气中很不稳定 亚铁盐
遇KSCN溶液变色 铁盐
具有磁性的黑色固体 铁单质
用于治疗缺铁性贫血 三氧化二铁
涂料中的红色颜料 四氧化三铁
用于保存亚铁盐溶液 氢氧化亚铁
在空气中很不稳定 亚铁盐
遇KSCN溶液变色 铁盐
您最近一年使用:0次
名校
5 . 氮元素的单质和化合物在生活生产中有广泛用途。
(1)氮分子中化学键名称是_______ ;氮分子的电子式为:_______ ;已知 分子与
分子与 分子结构相似,
分子结构相似, 熔点高于
熔点高于 ,其原因是(从化学键和晶体的角度用文字表述原因)
,其原因是(从化学键和晶体的角度用文字表述原因)_______ 。
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
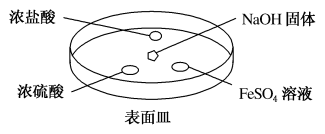
浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_______ ;浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,其中所含的正盐作为一种化肥俗称:_______ ,长期施用容易造成土壤酸化板结; 液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是
液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是_______ 和_______ 。
(3)将氨通入水中溶液呈碱性的原因(用方程式表示)_______ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),写出反应的化学方程式并用单线桥标出电子转移方向和数目_______ ,该反应中被氧化的元素是_______ ,还原产物是_______ 。若反应中有3mol电子发生转移,参与反应的氨的质量为_______ g。
(1)氮分子中化学键名称是
 分子与
分子与 分子结构相似,
分子结构相似, 熔点高于
熔点高于 ,其原因是(从化学键和晶体的角度用文字表述原因)
,其原因是(从化学键和晶体的角度用文字表述原因)(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
 液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是
液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是(3)将氨通入水中溶液呈碱性的原因(用方程式表示)
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),写出反应的化学方程式并用单线桥标出电子转移方向和数目
您最近一年使用:0次
名校
6 . 已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现血红色。

(1)物质A的化学式为___________ ,F化学式为___________ ;
(2)B和R在溶液中反应生成F的离子方程式为___________ ;
(3)H在潮湿空气中变成M的实验现象是___________ ;
(4)A和水反应生成B和C的化学方程式为_____ ,由此反应可知A有作为____ 的用途;

(1)物质A的化学式为
(2)B和R在溶液中反应生成F的离子方程式为
(3)H在潮湿空气中变成M的实验现象是
(4)A和水反应生成B和C的化学方程式为
您最近一年使用:0次



