22-23高二上·浙江·期中
1 . 为了探究某不溶性固体化合物X (仅含两种元素)。的组成和性质,设计并完成如下实验(假设各步反应均完全,反应中气体完全逸出)。已知甲是密度最小的气体,乙能使湿润的红色石蕊试纸变蓝。
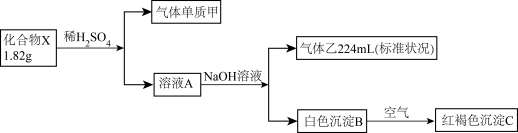
(1)组成X的元素是_______ 。
(2)写出B →C的化学反应方程式_______ 。
(3)写出化合物X与稀硫酸反应的离子方程式_______ 。
(4)请设计实验方案,检验溶液A中的金属阳离子_______ 。

(1)组成X的元素是
(2)写出B →C的化学反应方程式
(3)写出化合物X与稀硫酸反应的离子方程式
(4)请设计实验方案,检验溶液A中的金属阳离子
您最近一年使用:0次
解题方法
2 . 工业上用FeCl3溶液作印刷电路铜板的腐蚀液。化学小组设计如下流程对腐蚀废液(阳离子主要有Fe2+、Cu2+、Fe3+和H+)进行处理,实现FeCl3溶液再生并回收Cu。
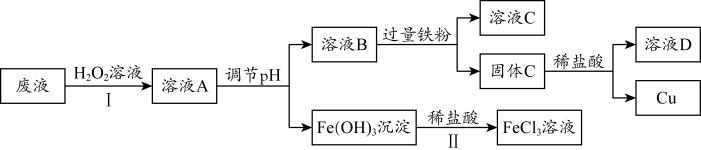
(1)步骤Ⅰ中加入H2O2溶液的目的是将Fe2+_______ (填“氧化”或“还原”)为Fe3+。
(2)步骤Ⅱ中发生反应的离子方程式为_______ 。
(3)溶液C中含有大量Fe2+。取少量溶液C于试管中,滴加_______ 溶液,有白色沉淀生成,白色沉淀迅速变为灰绿色,最终变为红褐色。
(4)下列说法合理的是_______ (填字母)。
a.溶液A、溶液B和固体C中都含有铜元素
b.溶液C和溶液D可回收利用,体现“绿色化学”理念

(1)步骤Ⅰ中加入H2O2溶液的目的是将Fe2+
(2)步骤Ⅱ中发生反应的离子方程式为
(3)溶液C中含有大量Fe2+。取少量溶液C于试管中,滴加
(4)下列说法合理的是
a.溶液A、溶液B和固体C中都含有铜元素
b.溶液C和溶液D可回收利用,体现“绿色化学”理念
您最近一年使用:0次
3 . 铁及其化合物之间的转化关系如图所示。
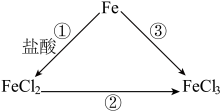
回答下列问题:
(1)反应①的离子方程式为_______ 。
(2)完成反应②还需加入_______ (填“氧化剂”或“还原剂”)。
(3)完成反应③还需用到的试剂为_______ (填化学式),检验 的试剂为
的试剂为_______ 。
(4)向 溶液中加入
溶液中加入 溶液的现象为
溶液的现象为_______ 。

回答下列问题:
(1)反应①的离子方程式为
(2)完成反应②还需加入
(3)完成反应③还需用到的试剂为
 的试剂为
的试剂为(4)向
 溶液中加入
溶液中加入 溶液的现象为
溶液的现象为
您最近一年使用:0次
4 . 回答下列问题
(1)向少量新制的氯化亚铁溶液中,加入几滴硫氰化钾溶液,溶液_______ 色;再加几滴氯水,溶液呈_______ 色,该实验体现了Fe2+的_______ 性。已知Fe(SCN)3中N为−3价,可推测S元素的化合价为_______ 价。
(2)FeCl2溶液与Cl2反应的化学方程式为_______ ,上述生成Fe(SCN)3反应的离子方程式为_______ 。
(3)除去FeCl2溶液中的少量FeCl3,可采用的试剂是_______ (填写化学式),该反应的离子方程式为_______ 。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为_______ ,反应的化学方程式为_______ 。
(1)向少量新制的氯化亚铁溶液中,加入几滴硫氰化钾溶液,溶液
(2)FeCl2溶液与Cl2反应的化学方程式为
(3)除去FeCl2溶液中的少量FeCl3,可采用的试剂是
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
您最近一年使用:0次
名校
解题方法
5 . 下列离子的检验方法合理的是
| A.向某溶液中滴入硫氰化钾溶液呈红色,说明不含Fe2+ |
| B.向某溶液中通入氯气,然后再加入硫氰化钾溶液变红色,说明原溶液中含有Fe2+ |
| C.向某溶液中加入氢氧化钠溶液,得红褐色沉淀,说明溶液中含有Fe3+ |
| D.向某溶液中加入氢氧化钠溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+ |
您最近一年使用:0次
2022-12-20更新
|
488次组卷
|
41卷引用:湖北省咸丰春晖学校2022-2023学年高二上学期9月月考化学试题
湖北省咸丰春晖学校2022-2023学年高二上学期9月月考化学试题2015-2016学年山西省晋城市高平市特立高中高二下期中文科化学试卷河北省邢台市第一中学2016-2017学年高二下学期第三次月考化学试题辽宁省本溪满族自治县高级中学2019-2020学年高二下学期期末考试化学试题陕西省汉中市洋县第二高级中学2020-2021学年高二上学期11月月考化学试题黑龙江省牡丹江市第三中学2021-2022学年高二上学期第一次月考化学(文)试题浙江省丽水外国语学校高中部2021-2022学年高一下学期第一次阶段性考试(3月)化学试题山东省济南九中2022-2023学年高一第二次线上质量评估(12月份)化学试题(已下线)2012-2013学年辽宁省实验中学分校高一上学期期末考试化学试卷(已下线)2012-2013年黑龙江哈尔滨第十二中学高一上学期期末考试化学试卷2015-2016学年广东省汕头金山中学高一上期末化学试卷2016-2017学年宁夏育才中学高一上月考二化学卷22016-2017学年江西省景德镇一中高一12月月考化学卷青海省西宁市第四高级中学2017-2018学年高一上学期第二次月考化学试题1宁夏育才中学孔德校区2017-2018学年高一12月月考化学试题青海省西宁二十一中2017-2018学年高一上学期12月月考化学试题(已下线)解密05 金属及其化合物(教师版)——备战2018年高考化学之高频考点解密安徽省滁州市民办高中2018-2019学年高一上学期第三次月考化学试题【市级联考】吉林省公主岭市2018-2019学年高一上学期期末考试化学试题甘肃省武威第十八中学2018-2019学年高一上学期期末考试化学试题贵州省剑河县第二中学2018-2019学年高一上学期12月份考试化学试题(已下线)专题3.3 铁及其重要化合物(讲)——2020年高考化学一轮复习讲练测(已下线)3.1.1 铁及其化合物练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)第11讲 铁及其重要化合物(精讲)——2021年高考化学一轮复习讲练测湖北省宜昌市葛洲坝中学2021届高三9月月考化学试题高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 教材帮人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物 教材帮(已下线)练习13 铁铜的获取和应用-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)江西省南昌市新建一中2020-2021学年高一上学期第二次月考化学试题(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练(已下线)【浙江新东方】双师107专题9 第二单元 探究铁及其化合物的转化-高中化学必修第二册苏教版2019(已下线)【浙江新东方】高中化学20210304-019陕西省武功县普集高级中学2021-2022学年高一上学期第二次月考化学试题吉林江城中学2021-2022学年高三上学期9月月考化学试题9.2.1反应的合理选择(课中)-2019苏教版必修2课前课中课后第2课时 铁盐和亚铁盐作业(十七) 亚铁盐和铁盐(已下线)【精品卷】3.1.2 铁的重要化合物课堂例题-人教版2023-2024学年必修第一册河北省高碑店市崇德实验中学2022-2023学年高一下学期期末考试化学试题化学江苏省扬州市宝应区2023-2024学年曹甸高级中学高三上学期9月化学试卷
6 . 部分含铁物质的物质类别与相应化合价的关系如图所示,下列相关说法错误的是
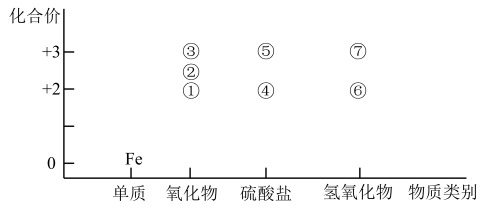

| A.Fe高温下可与水蒸气反应生成② |
| B.③用于生产红色涂料,可长久不变色 |
| C.在空气中加热⑥,不易得到纯净的FeO,易生成红棕色的Fe2O3 |
| D.向盛有少量酸性KMnO4溶液的试管中加入足量④溶液,紫色褪去,说明④溶液未变质 |
您最近一年使用:0次
名校
7 . 某同学设计如图装置制备一定量的Fe(OH)2,并使其能在较长时间内存在。

(1)X为稀盐酸,写出装置2中反应的离子方程式_______ 。
(2)实验开始时,打开分液漏斗塞子,打开K1,_______ (填“打开”成“关闭”)K2;这样操作的目的是_______ 。一段时间后_______ (填“打开”成“关闭”)K2,装置2中的现象是_______ ;装置3中反应的离子方程式_______ 。
(3)装置4的作用是_______ 。
(4)制得的Fe(OH)2暴露在空气中最终会变为红褐色,反应的化学方程式为_______ 。

(1)X为稀盐酸,写出装置2中反应的离子方程式
(2)实验开始时,打开分液漏斗塞子,打开K1,
(3)装置4的作用是
(4)制得的Fe(OH)2暴露在空气中最终会变为红褐色,反应的化学方程式为
您最近一年使用:0次
2022-10-22更新
|
157次组卷
|
2卷引用:上海市财经大学附属北郊高级中学2022-2023学年高二上学期等级班阶段性检测化学试题
名校
8 . 氮元素单质及其化合物在工农业生产中有重要应用。
(1)氮原子结构示意图为____ ;氮气分子的电子式为:____ 。
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

浓盐酸液滴附近会出现白烟,发生反应的化学方程式为____ ;浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,其中所含的正盐作为一种化肥俗称____ ,长期施用容易造成土壤酸化板结。
(3)FeSO4液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生反应的方程式为Fe2++2NH3•H2O=Fe(OH)2+2NH 和
和____ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方式为____ 。若反应中有0.6mol电子发生转移,生成亚硝酸的质量为____ g。
(1)氮原子结构示意图为
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
(3)FeSO4液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生反应的方程式为Fe2++2NH3•H2O=Fe(OH)2+2NH
 和
和(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方式为
您最近一年使用:0次
9 . 下列有关金属及其化合物的说法错误的是
| A.铁丝在氯气中剧烈燃烧,生成FeCl2 | B.配制FeSO4溶液时加入少量的铁粉 |
| C.Fe(OH)2在空气中易被氧化成红褐色的Fe(OH)3 | D. 可用于制作红色油漆或涂料 可用于制作红色油漆或涂料 |
您最近一年使用:0次
2022-10-05更新
|
622次组卷
|
3卷引用:上海市顾村中学2022-2023学年高二上学期期中考试化学试题
10 . 元素及其化合物与人类有密切关系。
(1)氮的固定有利于生物吸收氮。下列属于氮的固定的是________ (填序号)。
①工业上 和
和 合成
合成
② 和
和 放电条件下生成
放电条件下生成
③ 催化氧化生成
催化氧化生成
写出反应③的化学方程式
(2)治理 通常是在氧化剂作用下,将
通常是在氧化剂作用下,将 氧化成溶解度高的
氧化成溶解度高的 ,然后用水或碱液吸收脱氮。下列物质可以用作氧化
,然后用水或碱液吸收脱氮。下列物质可以用作氧化 的是
的是________ 填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C.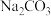 溶液 D.
溶液 D. 溶液
溶液
若以 溶液氧化
溶液氧化 ,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目
,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目________ 。
(3)如图所示,此装置可用来制取较纯 沉淀,然后观察它在空气中被氧化时的颜色变化,实验时使用铁屑和
沉淀,然后观察它在空气中被氧化时的颜色变化,实验时使用铁屑和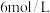 的硫酸,其他试剂任选。填写下列空白:
的硫酸,其他试剂任选。填写下列空白:
①B中盛有一定量的 溶液,A中应预先加入试剂是
溶液,A中应预先加入试剂是________ ;
②A中反应的离子方程式是________ ;
③实验开始时应先将活塞a________ (填“打开”、“关闭”),目的是________ ;
④实验完毕,打开b处活塞,放入一部分空气,此时B瓶中发生的反应现象________ ,化学方程式为________ 。

(1)氮的固定有利于生物吸收氮。下列属于氮的固定的是
①工业上
 和
和 合成
合成
②
 和
和 放电条件下生成
放电条件下生成
③
 催化氧化生成
催化氧化生成
写出反应③的化学方程式
(2)治理
 通常是在氧化剂作用下,将
通常是在氧化剂作用下,将 氧化成溶解度高的
氧化成溶解度高的 ,然后用水或碱液吸收脱氮。下列物质可以用作氧化
,然后用水或碱液吸收脱氮。下列物质可以用作氧化 的是
的是A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C.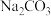 溶液 D.
溶液 D. 溶液
溶液若以
 溶液氧化
溶液氧化 ,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目
,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目(3)如图所示,此装置可用来制取较纯
 沉淀,然后观察它在空气中被氧化时的颜色变化,实验时使用铁屑和
沉淀,然后观察它在空气中被氧化时的颜色变化,实验时使用铁屑和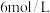 的硫酸,其他试剂任选。填写下列空白:
的硫酸,其他试剂任选。填写下列空白:①B中盛有一定量的
 溶液,A中应预先加入试剂是
溶液,A中应预先加入试剂是②A中反应的离子方程式是
③实验开始时应先将活塞a
④实验完毕,打开b处活塞,放入一部分空气,此时B瓶中发生的反应现象

您最近一年使用:0次



