名校
1 . 在混合体系中,确认化学反应先后顺序有利于问题的解决,下列反应先后顺序判断正确的是
A.在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2: 、 、 、 、 |
B.在含等物质的量的 、 、 、 、 的溶液中加入Zn: 的溶液中加入Zn: 、 、 、 、  |
C.在含等物质的量的 、KOH的溶液中通入 、KOH的溶液中通入 : : 、KOH、BaCO3、 、KOH、BaCO3、 |
D.在含等物质的量的 、 、 、 、 溶液中,逐滴加入盐酸: 溶液中,逐滴加入盐酸: 、 、 、 、 、 、 |
您最近一年使用:0次
2020-02-23更新
|
126次组卷
|
2卷引用:2020届高三化学化学二轮复习——高考常考题:氧化还原反应的实际应用【精编选择25题】
解题方法
2 . 下列叙述I和II均正确且具有因果关系的是
| 编号 | 叙述I | 叙述II |
| A | Fe3+的氧化性比Cu2+强 | FeCl3溶液可用于溶解回收旧电路板中的铜 |
| B | NH4Cl受热分解 | 加热可将Ca(OH)2和NH4Cl固体混合物分离 |
| C | 金属活动性铜比铁弱 | 镀铜铁制品表层划损后仍然受到保护 |
| D | Cl2具有漂白性 | 用氯气制盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 二氧化硫是形成酸雨的罪魁祸首之一,含硫煤燃烧的尾气处理一直是化学研究的重要课题。某工厂设计了新的治污方法,该工艺流程如图所示,下列叙述不正确的是( )
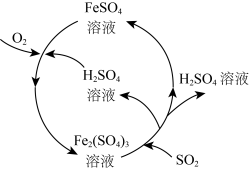

A.该过程中可得到化工产品 |
B.该工艺流程中 可以循环利用 可以循环利用 |
C.若处理含 的尾气,理论上需要通入相同条件下的空气约 的尾气,理论上需要通入相同条件下的空气约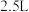 |
| D.可用澄清石灰水检验最终排出的气体是否含有二氧化硫 |
您最近一年使用:0次
2020-02-16更新
|
264次组卷
|
3卷引用:2020届高三化学无机化学二轮专题复习——铁盐及亚铁盐的性质2【精编25题】
名校
解题方法
4 . 下列实验现象与氧化还原反应有关的是
| A.SO2通入品红溶液中,溶液褪色,加热后又恢复红色 |
| B.向FeCl3溶液中滴加淀粉KI溶液,溶液变蓝 |
| C.向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
| D.二氧化碳通入石灰水中变浑浊,继续通入又变澄清 |
您最近一年使用:0次
2020-02-11更新
|
205次组卷
|
3卷引用:2019-2020学年高一上学期期末复习《新题速递·化学》12月(考点07-10)
解题方法
5 . 下列有关叙述正确的是
A.Fe与S混合加热生成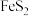 |
B. 有氧化性,因此 有氧化性,因此 溶液可用于回收废旧电路板中的Cu 溶液可用于回收废旧电路板中的Cu |
C.Fe在足量 中燃烧生成 中燃烧生成 和 和 |
D. 、 、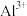 、 、 、 、 在水溶液中一定能大量共存 在水溶液中一定能大量共存 |
您最近一年使用:0次
解题方法
6 . 下列中学常见实验的现象或表述正确的是
| A.饱和碳酸钠溶液和饱和碳酸氢钠溶液中滴入酚酞溶液,溶液均显红色 |
B.含4molHCl的浓盐酸与足量的 共热,得到 共热,得到 |
| C.铝箔在空气中用酒精灯加热可以熔化滴落,且发生剧烈燃烧 |
D. 和 和 的混合溶液中加入铁屑,反应结束后滤出固体物质,滤液中的阳离子可能是 的混合溶液中加入铁屑,反应结束后滤出固体物质,滤液中的阳离子可能是 和 和 |
您最近一年使用:0次
解题方法
7 . 下列说法正确的有( )
①FeO投入稀H2SO4和稀HNO3中均得到浅绿色溶液
②向红砖粉末中加入盐酸,充分振荡反应后取上层清液于试管中,滴加KSCN溶液2〜3滴,溶液呈红色,但不一定说明红砖中含有氧化铁
③Fe2O3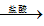 FeCl3(aq)
FeCl3(aq)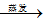 无水FeCl3
无水FeCl3
④磁性氧化铁溶于稀硝酸的离子方程式为3Fe2++4H++NO3-=Fe3++NO↑+3H2O
⑤氢氧化铁与HI溶液反应的离子方程式为Fe(OH)3+H+=Fe3++3H2O
⑥Fe(OH)3不可用Fe2O3与水反应得到,但能通过其它化合反应制取
①FeO投入稀H2SO4和稀HNO3中均得到浅绿色溶液
②向红砖粉末中加入盐酸,充分振荡反应后取上层清液于试管中,滴加KSCN溶液2〜3滴,溶液呈红色,但不一定说明红砖中含有氧化铁
③Fe2O3
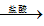 FeCl3(aq)
FeCl3(aq)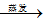 无水FeCl3
无水FeCl3④磁性氧化铁溶于稀硝酸的离子方程式为3Fe2++4H++NO3-=Fe3++NO↑+3H2O
⑤氢氧化铁与HI溶液反应的离子方程式为Fe(OH)3+H+=Fe3++3H2O
⑥Fe(OH)3不可用Fe2O3与水反应得到,但能通过其它化合反应制取
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
名校
解题方法
8 . 常温下,铝土矿 含有
含有 、FeO、
、FeO、 、
、 等物质
等物质 用硫酸浸。下列说法中错误的是
用硫酸浸。下列说法中错误的是

 含有
含有 、FeO、
、FeO、 、
、 等物质
等物质 用硫酸浸。下列说法中错误的是
用硫酸浸。下列说法中错误的是

A.向浸出后的溶液加入过量NaOH溶液后存在: 、 、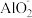 、 、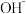 、 、 |
B.向浸出后的溶液加入过量氨水后存在: 、 、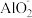 、 、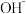 、 、 |
C.向浸出后的溶液通入过量HI后存在: 、 、 、 、 、 、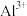 、 、 |
D.若铝土矿改用NaOH溶液浸,浸出后的溶液中存在: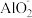 、 、 、 、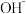 、 、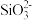 |
您最近一年使用:0次
2020-02-06更新
|
241次组卷
|
6卷引用:夯基提能2020届高三化学选择题对题专练——氧化还原反应的实际应用(提升练)
9 . 工业上常通过高温分解FeSO4的方法制备Fe2O3,为检验FeSO4高温分解的产物,并进行有关探究实验,回答下列问题:
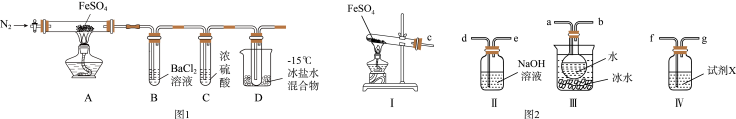
实验一:高温分解FeSO4,利用如图1所示的实验装置进行实验。
已知:①SO2熔点为-72℃,沸点为-10℃;②SO3熔点为-16.8℃,沸点为44.8℃。
(1)连接装置,检验气密性良好,放入药品,通入一段时间N2然后加热,通入N2的目的是___ 。
(2)隔绝空气加热至650℃,看到B中有白色沉淀,D试管中有无色液体,硬质玻璃管中的固体变为___ ,同时有两种无色气体生成,写出该反应的化学方程式___ 。
(3)反应完毕后,停止加热冷却后,取硬质玻璃管中固体,加盐酸,反应的离子方程式是___ ,将反应后所得溶液滴入D试管中,溶液变为浅绿色,该反应的离子方程式是___ 。
实验二:探究高温分解FeSO4生成的气体
(4)用如图2所示装置设计实验,验证高温分解FeSO4生成的气态物质
①按气流方向连接各仪器,用字母表示接口的连接顺序:c-___ 。
②试剂X的名称是___ 。
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的FeSO4的质量,向圆底烧瓶中逐渐滴入氯化钡溶液,直到沉淀完全;然后过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重.若最终得到沉淀的质量为Wg,则已分解的FeSO4的质量__ g。

实验一:高温分解FeSO4,利用如图1所示的实验装置进行实验。
已知:①SO2熔点为-72℃,沸点为-10℃;②SO3熔点为-16.8℃,沸点为44.8℃。
(1)连接装置,检验气密性良好,放入药品,通入一段时间N2然后加热,通入N2的目的是
(2)隔绝空气加热至650℃,看到B中有白色沉淀,D试管中有无色液体,硬质玻璃管中的固体变为
(3)反应完毕后,停止加热冷却后,取硬质玻璃管中固体,加盐酸,反应的离子方程式是
实验二:探究高温分解FeSO4生成的气体
(4)用如图2所示装置设计实验,验证高温分解FeSO4生成的气态物质
①按气流方向连接各仪器,用字母表示接口的连接顺序:c-
②试剂X的名称是
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的FeSO4的质量,向圆底烧瓶中逐渐滴入氯化钡溶液,直到沉淀完全;然后过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重.若最终得到沉淀的质量为Wg,则已分解的FeSO4的质量
您最近一年使用:0次
10 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是

| 选项 | 实验 | 现象 | 结论 |
| A | 向2mL  的 的 溶液中加足量铁粉,振荡,加1滴KSCN溶液 溶液中加足量铁粉,振荡,加1滴KSCN溶液 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性: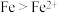 |
| B | 往 溶液中通入足量 溶液中通入足量 气体 气体 | 产生白色胶状沉淀 | 酸性: |
| C | 常温下将铝片加入浓硝酸中 | 无明显现象 | 铝与浓硝酸不反应 |
| D | 将 溶液滴加到酸性 溶液滴加到酸性 溶液中 溶液中 | 紫色溶液褪色 |  具有氧化性 具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



