1 . 甲、乙、丙三种物质间通过一步反应能实现如图转化,下列选项中符合转化关系的是


A.甲为 ,乙为 ,乙为 ,丙为 ,丙为 |
B.甲为 ,乙为 ,乙为 ,丙为 ,丙为 |
C.甲为 ,乙为 ,乙为 ,丙为 ,丙为 |
D.甲为 ,乙为 ,乙为 ,丙为 ,丙为 |
您最近一年使用:0次
解题方法
2 . X、Y、Z、W四种物质的转化关系如图所示(“ ”表示反应一步实现,部分物质和反应条件已略去),则符合要求的X、Y、Z、W依次是
”表示反应一步实现,部分物质和反应条件已略去),则符合要求的X、Y、Z、W依次是

 ”表示反应一步实现,部分物质和反应条件已略去),则符合要求的X、Y、Z、W依次是
”表示反应一步实现,部分物质和反应条件已略去),则符合要求的X、Y、Z、W依次是
| 选项 | X | Y | Z | W |
| A |  |  |  |  |
| B |  |  |  |  |
| C | Fe |  |  | Fe2O3 |
| D |  |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-13更新
|
361次组卷
|
2卷引用:辽宁省重点高中沈阳市郊联体2023-2024学年高一上学期10月月考化学试题
名校
解题方法
3 . 下列离子能大量共存的是
A.在含大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.无色澄清透明的溶液中: 、 、 、 、 、 、 、 、 |
C.使无色酚酞试液呈红色的溶液中: 、 、 、 、 、 、 |
D.使石蕊试液变红的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2023-10-13更新
|
337次组卷
|
6卷引用:辽宁省重点高中沈阳市郊联体2023-2024学年高一上学期10月月考化学试题
名校
解题方法
4 . 黄铜渣中约含Zn7%、ZnO31%、Cu50%、CuO5%,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如下图(杂质不溶于水、不参与反应):
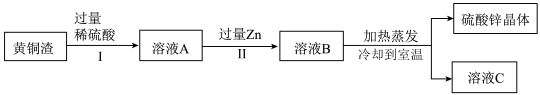
下列说法正确的是

下列说法正确的是
| A.溶液A中的溶质有2种 |
| B.Ⅰ、Ⅱ中的操作均包含过滤 |
| C.溶液A的质量大于溶液B |
| D.溶液C中溶质的质量分数小于溶液B |
您最近一年使用:0次
名校
解题方法
5 . 关于物质分类的正确组合是
| 分类组合 | 碱 | 酸 | 碱性氧化物 | 酸性氧化物 | 纯净物 |
| A |  |  |  |  | 合金 |
| B | 纯碱 |  |  |  | 硫酸 |
| C |  |  |  |  | 盐酸 |
| D |  |  |  | 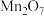 | 胆矾 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 云南省博物馆收藏的“四牛鎏金骑士铜贮贝器”,是滇青铜文明的代表性文物之一。下列有关该文物的说法正确的是

四牛鎏金骑士铜贮贝器

四牛鎏金骑士铜贮贝器
| A.青铜是合金 | B.青铜是铜单质 |
| C.表面的铜绿是CuO | D.在青铜器上鎏金是化学变化 |
您最近一年使用:0次
解题方法
7 . 下列是四种实验操作中各量变化关系的图像,能正确反映其对应操作的图像有
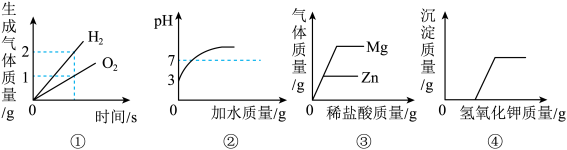
①电解水
②向一定量 的盐酸溶液中不断加水稀释
的盐酸溶液中不断加水稀释
③向等质量的镁和锌中分别加入溶质质量分数相同的稀盐酸至过量
④向盐酸和氯化铜的混合溶液中不断滴加氢氧化钾溶液

①电解水
②向一定量
 的盐酸溶液中不断加水稀释
的盐酸溶液中不断加水稀释③向等质量的镁和锌中分别加入溶质质量分数相同的稀盐酸至过量
④向盐酸和氯化铜的混合溶液中不断滴加氢氧化钾溶液
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次
8 . 在初中化学“金属的性质”中有如下实验:将无锈铁钉浸入CuSO4溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
【提出问题】Al和CuSO4溶液也能发生化学反应吗?
(1)预测Al能和CuSO4溶液反应,理由是_______ 。
【进行实验】将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。
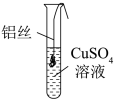
(2)铝丝表面未出现红色物质,原因是_______ (用化学方程式解释)。
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
(3)填写实验报告单:
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为_______ 。
(5)欲加快Al和CuSO4溶液的反应,可加入的物质是_______ (填一种即可)。
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是_______(填序号)。
【提出问题】Al和CuSO4溶液也能发生化学反应吗?
(1)预测Al能和CuSO4溶液反应,理由是
【进行实验】将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。

(2)铝丝表面未出现红色物质,原因是
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
(3)填写实验报告单:
| 序号 | 实验现象 | 结论与解释 |
| ① | 铝丝表面有少量气泡;铝丝周围出现蓝绿色物质 | CuSO4溶液呈弱酸性,与Al反应产生的气体是 |
| ② | 24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质 | 红色物质是 |
| ③ | 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色:两层溶液界面清晰 | 反应生成的Al2(SO4)3为无色;Al2(SO4)3溶液的密度 |
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为
(5)欲加快Al和CuSO4溶液的反应,可加入的物质是
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是_______(填序号)。
| A.食醋 | B.食用油 | C.面粉 | D.咸菜 |
您最近一年使用:0次
名校
9 . 胆矾(CuSO4·5H2O,相对式量为250)受热会先失去结晶水,完全脱水的化学方程式为: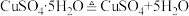 ,且无水硫酸铜固体加热到650℃会分解。现加热25.0g胆矾的过程中,测得固体质量随温度变化曲线如图(图中最后剩余物质为纯净物),请仔细分析如图后判断以下几种说法正确的个数有:
,且无水硫酸铜固体加热到650℃会分解。现加热25.0g胆矾的过程中,测得固体质量随温度变化曲线如图(图中最后剩余物质为纯净物),请仔细分析如图后判断以下几种说法正确的个数有:
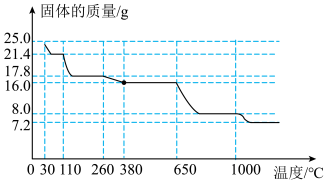
(1)胆矾失水的温度范围为30℃~380C
(2)开始加热至完全脱水,胆矾经历5次脱水过程
(3)650℃后CuSO4分解得到CuO和SO2两种物质
(4)1000℃时,得到固体物质的化学式为CuO
(5)1000℃之后,可能发生了以下的化学变化: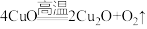
(6)整个变化过程中没有元素化合价发生改变
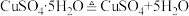 ,且无水硫酸铜固体加热到650℃会分解。现加热25.0g胆矾的过程中,测得固体质量随温度变化曲线如图(图中最后剩余物质为纯净物),请仔细分析如图后判断以下几种说法正确的个数有:
,且无水硫酸铜固体加热到650℃会分解。现加热25.0g胆矾的过程中,测得固体质量随温度变化曲线如图(图中最后剩余物质为纯净物),请仔细分析如图后判断以下几种说法正确的个数有:
(1)胆矾失水的温度范围为30℃~380C
(2)开始加热至完全脱水,胆矾经历5次脱水过程
(3)650℃后CuSO4分解得到CuO和SO2两种物质
(4)1000℃时,得到固体物质的化学式为CuO
(5)1000℃之后,可能发生了以下的化学变化:
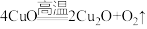
(6)整个变化过程中没有元素化合价发生改变
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次
名校
解题方法
10 . 取一定量胆矾晶体(CuSO4·5H2O)加热分解,固体残留率( ) 随温度的变化如图所示:
) 随温度的变化如图所示:
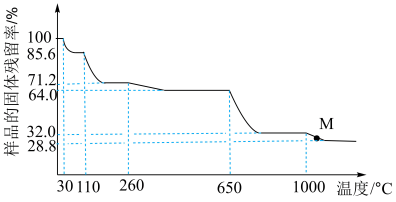
下列说法中不正确的是
 ) 随温度的变化如图所示:
) 随温度的变化如图所示:
下列说法中不正确的是
| A.110°C 时的晶体化学式 CuSO4·3H2O |
B.260°C~ 650°C 过程中的反应方程式为CuSO4·H2O CuSO4+H2O CuSO4+H2O |
| C.已知 650°C 加热至 1000°C ,产物为一种固体与一种气体, 则气体为SO2 |
| D.M 点所得固体是 CuO 与 Cu2O 的混合物 |
您最近一年使用:0次



