名校
解题方法
1 . 下列是两种制备 的方式
的方式
甲: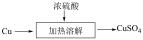
乙: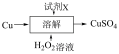
下列说法正确的是
 的方式
的方式甲:

乙:

下列说法正确的是
| A.从环境保护角度分析方案甲更好 |
| B.乙方案中试剂X为稀盐酸 |
C.若用方案甲制备 会产生 会产生 |
D.方案乙“溶解”时发生反应的离子方程式为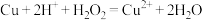 |
您最近一年使用:0次
2023-04-16更新
|
97次组卷
|
2卷引用:湖北省宜昌市协作体2022-2023学年高一下学期期中考试化学试题
名校
解题方法
2 . 学生设计出四种实验方案(如图)用以验证浓硫酸的吸水性,在理论上可行的是


| A.仅①②③ | B.仅①③④ | C.①②③④ | D.仅②③④ |
您最近一年使用:0次
名校
解题方法
3 . CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
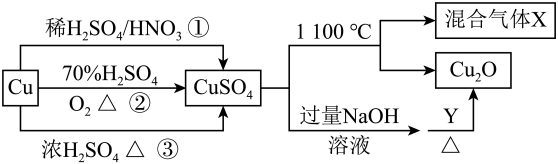

| A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 |
| B.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| C.1mol CuSO4在1100℃所得混合气体X中O2可能为0.75mol |
| D.Y应该是一种还原剂 |
您最近一年使用:0次
名校
4 . 下列硫酸盐性质与用途具有对应关系的是
| A.KAl(SO4)2·12H2O能水解形成胶体,可用作净水剂 |
| B.FeSO4具有还原性,可作治疗贫血药剂 |
| C.CuSO4水溶液呈酸性,可用作杀菌剂 |
| D.BaSO4难溶于水,可用于制取BaS |
您最近一年使用:0次
2023-03-10更新
|
129次组卷
|
2卷引用:江苏省苏州市工业园区星海实验高级中学2023-2024学年高一上学期12月调研化学试题
5 . 经检测某工厂的酸性废水中所含离子及其浓度如表所示:
(1)c(H+)=_______ mol/L。
(2)为了减少污染并变废为宝,工程师们设计了如图流程,回收铜和绿矾(FeSO4·7H2O)。

①工业废水中加入铁粉生成固体C时发生反应的离子方程为:_______ 。
②试剂B的化学式是_______ 。
③上述100L废水经处理,可获得FeSO4·7H2O的物质的量是_______ mol。
④在含有4molFeSO4的溶液中加入4molNa2O2现象是_______ ;已知反应物恰好完全反应且反应转移6mol电子,生成的气体标况下的体积为_______ L。
| 离子 | Fe3+ | Cu2+ | SO | Na+ | H+ |
| 浓度/(mol/L) | 2×10-2 | 1×10-2 | 1×10-1 | 2×10-2 |
(2)为了减少污染并变废为宝,工程师们设计了如图流程,回收铜和绿矾(FeSO4·7H2O)。

①工业废水中加入铁粉生成固体C时发生反应的离子方程为:
②试剂B的化学式是
③上述100L废水经处理,可获得FeSO4·7H2O的物质的量是
④在含有4molFeSO4的溶液中加入4molNa2O2现象是
您最近一年使用:0次
6 . 从价类二维的角度认识化学物质是一种高效的学习方法,铜元素的价类二维图如下,根据要求回答有关问题:
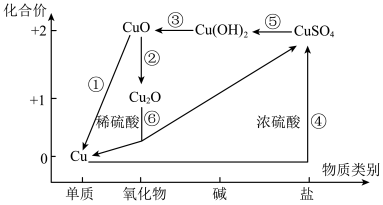
(1)转化②中铜元素被_______ (填“氧化”或“还原”)。
(2)转化④的化学方程式为_______ ,转化⑥的离子方程式为_______ 。
(3)转化⑤生成的 沉淀中混有
沉淀中混有 ,写出生成
,写出生成 的化学方程式
的化学方程式_______ ,用离子反应的实质解释生成 的原因是
的原因是_______ (表述中须指明微粒名称或符号)。
(4)电子工业中,人们常用 溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板。请设计从腐蚀废液中回收金属
溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板。请设计从腐蚀废液中回收金属 的处理方案,用流程图表示
的处理方案,用流程图表示_______ 。
(流程图示例: ……)
……)

(1)转化②中铜元素被
(2)转化④的化学方程式为
(3)转化⑤生成的
 沉淀中混有
沉淀中混有 ,写出生成
,写出生成 的化学方程式
的化学方程式 的原因是
的原因是(4)电子工业中,人们常用
 溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板。请设计从腐蚀废液中回收金属
溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板。请设计从腐蚀废液中回收金属 的处理方案,用流程图表示
的处理方案,用流程图表示(流程图示例:
 ……)
……)
您最近一年使用:0次
解题方法
7 . 下列化学用语对事实的表征正确的是
A.氮气的电子式: |
B. 分子结构模型: 分子结构模型: |
C. (g)通过灼热铁粉: (g)通过灼热铁粉: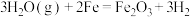 |
D.铜在潮湿空气中易产生铜绿[主要成分为 ]: ]: |
您最近一年使用:0次
解题方法
8 . 能正确表示下列反应的离子方程式的是
A.用稀盐酸除去铜器表面的铜绿: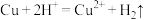 |
B. 溶液与稀 溶液与稀 反应: 反应: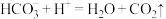 |
C.往 溶液中滴加足量稀硫酸: 溶液中滴加足量稀硫酸: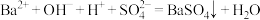 |
D.漂白粉在空气中久置失效: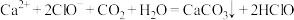 |
您最近一年使用:0次
名校
解题方法
9 . 下列物质在给定条件下的转化均能一步实现的是
A.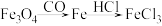 | B.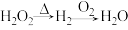 |
C. 溶液 溶液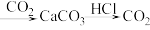 | D. 溶液 溶液 |
您最近一年使用:0次
名校
解题方法
10 . 江南梅雨季节,家用除湿袋内的白色颗粒物吸收水分后将溶解进入集水区,仔细观察可发现集水区有白色晶体析出,那么袋内最有可能的物质是
| A.氯化钙 | B.活性炭 | C.干冰 | D.CuSO4 |
您最近一年使用:0次



