从价类二维的角度认识化学物质是一种高效的学习方法,铜元素的价类二维图如下,根据要求回答有关问题:
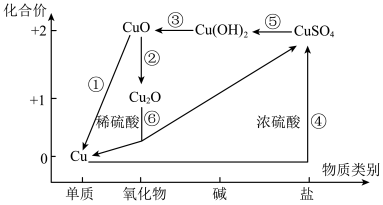
(1)转化②中铜元素被_______ (填“氧化”或“还原”)。
(2)转化④的化学方程式为_______ ,转化⑥的离子方程式为_______ 。
(3)转化⑤生成的 沉淀中混有
沉淀中混有 ,写出生成
,写出生成 的化学方程式
的化学方程式_______ ,用离子反应的实质解释生成 的原因是
的原因是_______ (表述中须指明微粒名称或符号)。
(4)电子工业中,人们常用 溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板。请设计从腐蚀废液中回收金属
溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板。请设计从腐蚀废液中回收金属 的处理方案,用流程图表示
的处理方案,用流程图表示_______ 。
(流程图示例: ……)
……)

(1)转化②中铜元素被
(2)转化④的化学方程式为
(3)转化⑤生成的
 沉淀中混有
沉淀中混有 ,写出生成
,写出生成 的化学方程式
的化学方程式 的原因是
的原因是(4)电子工业中,人们常用
 溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板。请设计从腐蚀废液中回收金属
溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板。请设计从腐蚀废液中回收金属 的处理方案,用流程图表示
的处理方案,用流程图表示(流程图示例:
 ……)
……)
更新时间:2023-02-11 23:31:13
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】已知氢碘酸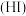 是一种具有强还原性的强酸,
是一种具有强还原性的强酸, 可以与多种物质【如:
可以与多种物质【如: 、
、 、
、 、
、 、
、 、
、 等】发生不同类型的化学反应.请回答下列问题:
等】发生不同类型的化学反应.请回答下列问题:
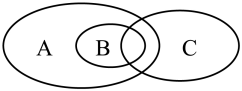
(1)下图可表示离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_________ (填标号).
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为_________________ .
(3)常温下 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,说明还原性
,说明还原性
______  (填“>”、“<”或“=).
(填“>”、“<”或“=).
(4)在反应 ,氧化剂与还原剂的物质的量之比为
,氧化剂与还原剂的物质的量之比为________ .
(5)下列三种氧化剂均可以将 氧化生成
氧化生成 ,自身对应的还原产物情况如下:
,自身对应的还原产物情况如下:
请判断等物质的量的三种氧化剂分别与足量HI作用,得到I2质量最多的是________ (填选项标号).
(6)向 胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
①红褐色沉淀溶解,反应的离子方程式为___________________________ .
②最后溶液颜色加深,反应的离子方程式为______________________________ .
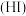 是一种具有强还原性的强酸,
是一种具有强还原性的强酸, 可以与多种物质【如:
可以与多种物质【如: 、
、 、
、 、
、 、
、 、
、 等】发生不同类型的化学反应.请回答下列问题:
等】发生不同类型的化学反应.请回答下列问题:(1)下图可表示离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)常温下
 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,说明还原性
,说明还原性
 (填“>”、“<”或“=).
(填“>”、“<”或“=).(4)在反应
 ,氧化剂与还原剂的物质的量之比为
,氧化剂与还原剂的物质的量之比为(5)下列三种氧化剂均可以将
 氧化生成
氧化生成 ,自身对应的还原产物情况如下:
,自身对应的还原产物情况如下:选项 | A | B | C |
氧化剂 |
|
|
|
还原产物 |
|
|
|
(6)向
 胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.
胶体中逐滴加入HI稀溶液,会出现如下一系列变化:先出现红褐色沉淀;随后沉淀溶解,溶液呈黄色:最后溶液颜色加深.①红褐色沉淀溶解,反应的离子方程式为
②最后溶液颜色加深,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Mg在CO2中燃烧的反应可用于火星电站发电、人员取暖等,反应的化学方程式为2Mg+CO2 2MgO+C。
2MgO+C。
(1)做氧化剂的物质是___________ ,Mg被___________ (填“氧化”或“还原”),碳元素的化合价___________ (填“升高”或“降低”)。
(2)反应中每生成1 mol MgO,消耗Mg的物质的量是___________ mol,转移电子的物质的量是___________ mol。
 2MgO+C。
2MgO+C。(1)做氧化剂的物质是
(2)反应中每生成1 mol MgO,消耗Mg的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.氧化还原反应是一类重要的化学反应,广泛存在于工农业生产、科学技术和日常生活中。氯化铵可除去铜器表面的氧化铜: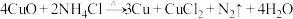 。
。
(1)反应中___________ 元素被还原,氧化产物是___________ 。
(2)该反应中氧化剂和还原剂物质的量之比是___________。
(3)当生成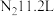 (标准状况)时,转移的电子数及被还原的
(标准状况)时,转移的电子数及被还原的 的物质的量为___________。
的物质的量为___________。
Ⅱ.天宫课堂中,王亚平老师用醋酸钠(化学式: )的过饱和溶液做了一个“太空冰雪”的趣味实验,在微重力环境下,使一颗“水球”瞬间变成了一颗“冰球”,因此对醋酸和醋酸钠的性质进行深入学习。请回答下列问题:
)的过饱和溶液做了一个“太空冰雪”的趣味实验,在微重力环境下,使一颗“水球”瞬间变成了一颗“冰球”,因此对醋酸和醋酸钠的性质进行深入学习。请回答下列问题:
(4)从物质分类上看,醋酸钠属于___________ ,醋酸溶液属于___________ 。
A.酸 B.碱 C.盐 D.非电解质 E.电解质 F.混合物
(5)已知:醋酸(CH3COOH)是一种弱酸,属于弱电解质,在水中不能完全电离。下列不能说明醋酸是弱电解质的是___________。
(6)往盛有 溶液的烧杯中逐滴滴加等浓度的醋酸溶液,直至过量。请写出醋酸溶液与
溶液的烧杯中逐滴滴加等浓度的醋酸溶液,直至过量。请写出醋酸溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(7)随着醋酸的滴入,烧杯中溶液的电导率随滴入醋酸溶液的体积变化趋势与下图一致的是___________。
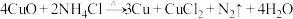 。
。(1)反应中
(2)该反应中氧化剂和还原剂物质的量之比是___________。
A. | B. | C. | D. |
(3)当生成
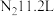 (标准状况)时,转移的电子数及被还原的
(标准状况)时,转移的电子数及被还原的 的物质的量为___________。
的物质的量为___________。A. , , | B. , , | C. , , | D. , , |
Ⅱ.天宫课堂中,王亚平老师用醋酸钠(化学式:
 )的过饱和溶液做了一个“太空冰雪”的趣味实验,在微重力环境下,使一颗“水球”瞬间变成了一颗“冰球”,因此对醋酸和醋酸钠的性质进行深入学习。请回答下列问题:
)的过饱和溶液做了一个“太空冰雪”的趣味实验,在微重力环境下,使一颗“水球”瞬间变成了一颗“冰球”,因此对醋酸和醋酸钠的性质进行深入学习。请回答下列问题:(4)从物质分类上看,醋酸钠属于
A.酸 B.碱 C.盐 D.非电解质 E.电解质 F.混合物
(5)已知:醋酸(CH3COOH)是一种弱酸,属于弱电解质,在水中不能完全电离。下列不能说明醋酸是弱电解质的是___________。
A.醋酸水溶液存在 、 、 、 、 |
| B.同浓度的盐酸和醋酸溶液,盐酸导电能力强 |
C.醋酸可以与碳酸钠反应制 |
| D.醋酸溶液能使石蕊试液变红 |
(6)往盛有
 溶液的烧杯中逐滴滴加等浓度的醋酸溶液,直至过量。请写出醋酸溶液与
溶液的烧杯中逐滴滴加等浓度的醋酸溶液,直至过量。请写出醋酸溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:(7)随着醋酸的滴入,烧杯中溶液的电导率随滴入醋酸溶液的体积变化趋势与下图一致的是___________。
A. | B. |
C.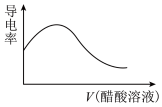 | D.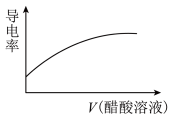 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】人们可以利用氧化还原反应研究物质的性质、实现物质的转化。
(1)过氧化钠可用于呼吸面具和潜水艇里的氧气供给_______ (用一个化学方程式表示)。
(2)实验室利用二氧化锰和浓盐酸反应制备Cl2的离子方程式为_______ ,此反应中浓盐酸体现了_______ 性质。
(3)浓硫酸与蔗糖进行“黑面包”实验时产生大量气体的化学方程式_______ 。
(4)将5%H2O2溶液滴入酸性KMnO4溶液中,观察到_______ ,此反应中H2O2做_______ 剂(填“氧化”或“还原)。若将5%H2O2溶液滴入FeCl2溶液中,则观察到_______ ,此反应中H2O2发生_______ 反应(填“氧化”或“还原”)。
(5)工业高炉炼铁时常以赤铁矿(主要成分为Fe2O3)和焦炭(主要成分为碳)为原料,而炼铁过程中实际起作用的是CO,请写出高炉炼铁的化学方程式_______ 。
(1)过氧化钠可用于呼吸面具和潜水艇里的氧气供给
(2)实验室利用二氧化锰和浓盐酸反应制备Cl2的离子方程式为
(3)浓硫酸与蔗糖进行“黑面包”实验时产生大量气体的化学方程式
(4)将5%H2O2溶液滴入酸性KMnO4溶液中,观察到
(5)工业高炉炼铁时常以赤铁矿(主要成分为Fe2O3)和焦炭(主要成分为碳)为原料,而炼铁过程中实际起作用的是CO,请写出高炉炼铁的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】H2SO4具有多种性质,回答下列问题:
(1)浓H2SO4使蔗糖变黑,体现了浓H2SO4的什么性质_______ 。黑色物质为炭粉,炭粉与浓硫酸继续反应的化学方程式为_______ 。
(2)浓H2SO4是常见的气体干燥剂,但它不能干燥H2S和HI,原因是_______ 。
(1)浓H2SO4使蔗糖变黑,体现了浓H2SO4的什么性质
(2)浓H2SO4是常见的气体干燥剂,但它不能干燥H2S和HI,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】物质类别和核心元素的价态是学习元素及其化合物性质的重要认识视角。下图是硫元素的“价类二维图”。

请回答下列问题:
(1)硫元素在周期表中的位置为_______ ;H2S的电子式为_______ 。
(2)H2S与SO2混合时会产生淡黄色粉末,该反应的化学方程式为_______ 。
(3)实验室可用铜与浓硫酸反应制取SO2气体,该反应的化学方程式为_______ ,其中浓硫酸表现_______ 。性(填“氧化”、“还原”或“酸”)。
(4)工业上制硫酸最后阶段是吸收SO3和硫酸的生成,该阶段在吸收塔中进行,SO3蒸气从吸收塔下口通入,上口加入98.3%的浓硫酸吸收SO3,用浓硫酸吸收SO3而不用水吸收的原因是_______ 。
(5)请设计实验证明K2SO3粉末已被空气中的氧气氧化:_______ 。

请回答下列问题:
(1)硫元素在周期表中的位置为
(2)H2S与SO2混合时会产生淡黄色粉末,该反应的化学方程式为
(3)实验室可用铜与浓硫酸反应制取SO2气体,该反应的化学方程式为
(4)工业上制硫酸最后阶段是吸收SO3和硫酸的生成,该阶段在吸收塔中进行,SO3蒸气从吸收塔下口通入,上口加入98.3%的浓硫酸吸收SO3,用浓硫酸吸收SO3而不用水吸收的原因是
(5)请设计实验证明K2SO3粉末已被空气中的氧气氧化:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即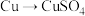 ;
;
方案乙:由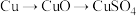 。
。
这两种方案,你认为哪一种方案更合理?_______ ,理由是_______ 。
(2)氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
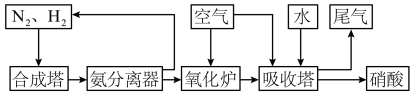
①合成塔中发生反应的化学方程式为_______ 。
②向吸收塔中通入空气的作用是_______ 。
③氧化炉中发生反应的化学方程式为_______ 。标准状况下,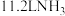 被氧化为
被氧化为 时转移电子的数目为
时转移电子的数目为_______ 。
④吸收塔中出来的尾气 可用具有碱性的
可用具有碱性的 溶液吸收,其中
溶液吸收,其中 既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:_______ 。
(1)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
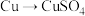 ;
;方案乙:由
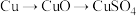 。
。这两种方案,你认为哪一种方案更合理?
(2)氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

①合成塔中发生反应的化学方程式为
②向吸收塔中通入空气的作用是
③氧化炉中发生反应的化学方程式为
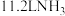 被氧化为
被氧化为 时转移电子的数目为
时转移电子的数目为④吸收塔中出来的尾气
 可用具有碱性的
可用具有碱性的 溶液吸收,其中
溶液吸收,其中 既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
既是氧化剂又是还原剂,且三种产物的物质的量之比为1∶1∶1,写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】从价类二维的角度认识化学物质是一种高效的学习方法,铜元素的价类二维图如下,根据要求回答有关问题:
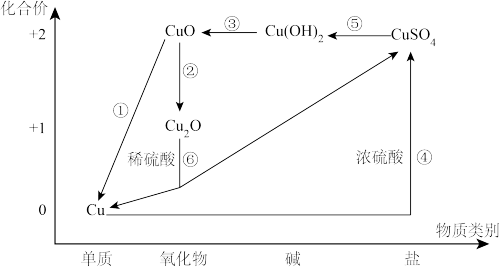
(1)Cu2(OH)2CO3是铜绿的主要成分,其属于_______ (填序号)。
a、碱b、正盐c、碱式盐d、酸式盐e、碳酸盐
(2)转化②中铜元素被_______ (填“氧化”或“还原”)。
(3)转化④的化学方程式为_______ 。
(4)转化⑤的反应类型为_______ (填基本反应类型),Cu(OH)2为_______ (填“强”、“弱”或“非”)电解质。
(5)已知Cu2O为砖红色不溶于水的固体,转化⑥可生成Cu、CuSO4溶液和另一种物质,则转化⑥的离子方程式为_______ 。
(6)Cu2O与稀HNO3可以发生氧化还原反应,完成并配平下列方程式:_______ 。
_______Cu2O+_______HNO3=_______Cu(NO3)2+_______NO↑+_______

(1)Cu2(OH)2CO3是铜绿的主要成分,其属于
a、碱b、正盐c、碱式盐d、酸式盐e、碳酸盐
(2)转化②中铜元素被
(3)转化④的化学方程式为
(4)转化⑤的反应类型为
(5)已知Cu2O为砖红色不溶于水的固体,转化⑥可生成Cu、CuSO4溶液和另一种物质,则转化⑥的离子方程式为
(6)Cu2O与稀HNO3可以发生氧化还原反应,完成并配平下列方程式:
_______Cu2O+_______HNO3=_______Cu(NO3)2+_______NO↑+_______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。工业上用粗氧化铜(含Fe2O3、FeO、Cu2O以及少量不溶性杂质)为原料制取氯化铜晶体 (CuCl2·2H2O)的为生产流程如下:
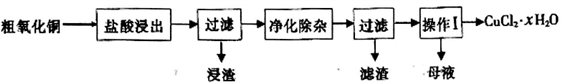
已知:Cu2O在酸性环境中可以生成Cu2+和Cu回答下列问题:
(1)已知“浸渣”中不含铜单质,写出Cu2O在“盐酸浸出”中发生反应的化学方程式:___________________________________________
(2)“盐酸浸出”中,铜的浸出率与浸出时间的关系如下图所示。由图可得出如下变化规律:
①____________________________
②______________________________ 。
(3)“净化除杂”需先加入C1O2,其作用是(用离子方程式表示)______________ 。
然后再调节溶液的pH约为4,可选用的试剂是(填选项字母)______________ 。
A. CuSO4B.CuOC.Cu2(OH)2CO3D.NH3·H2O
(4)“操作I”包含多步实验基本操作,依次是__________ 、洗涤和风干等。工业上常采用无水乙醇代替水进行洗涤的主要原因是______________ 。
(5)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,称取ag晶体,加入足量10%的氢氧化钠溶液,过滤、洗涤后,用酒精灯加热至质量不再减轻为止,冷却、称量所得固体质量为bg。计算得x=______________ 。(用含a、b的代数式表示)。

已知:Cu2O在酸性环境中可以生成Cu2+和Cu回答下列问题:
(1)已知“浸渣”中不含铜单质,写出Cu2O在“盐酸浸出”中发生反应的化学方程式:
(2)“盐酸浸出”中,铜的浸出率与浸出时间的关系如下图所示。由图可得出如下变化规律:
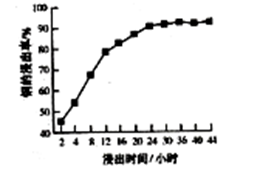
①
②
(3)“净化除杂”需先加入C1O2,其作用是(用离子方程式表示)
然后再调节溶液的pH约为4,可选用的试剂是(填选项字母)
A. CuSO4B.CuOC.Cu2(OH)2CO3D.NH3·H2O
(4)“操作I”包含多步实验基本操作,依次是
(5)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,称取ag晶体,加入足量10%的氢氧化钠溶液,过滤、洗涤后,用酒精灯加热至质量不再减轻为止,冷却、称量所得固体质量为bg。计算得x=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式正确的是________ 。
A.稀硫酸与铁丝制取氢气: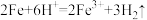
B.Cu片投入到FeCl3溶液中:Cu+2Fe3+=Cu2++2Fe2+
C.将少量Na放入水中:Na+H2O=Na++OH-+H2↑
D.氢氧化钡溶液与硫酸反应:OH-+H+=H2O
E.向澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
F.碳酸氢钠溶液与足量盐酸反应:2H++CO =H2O+CO2↑
=H2O+CO2↑
G.氧化钠与水反应:Na2O+H2O=2OH-+2Na+
H.将氧化钡与稀硫酸混合: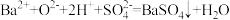
I.碳酸钙与稀盐酸制备二氧化碳:
J.CuSO4溶液中滴加Ba(OH)2溶液:Cu2++2OH-=Cu(OH)2↓
K.将铝片插入硝酸银溶液中: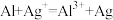
L.铁投入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
A.稀硫酸与铁丝制取氢气:
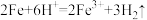
B.Cu片投入到FeCl3溶液中:Cu+2Fe3+=Cu2++2Fe2+
C.将少量Na放入水中:Na+H2O=Na++OH-+H2↑
D.氢氧化钡溶液与硫酸反应:OH-+H+=H2O
E.向澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
F.碳酸氢钠溶液与足量盐酸反应:2H++CO
 =H2O+CO2↑
=H2O+CO2↑G.氧化钠与水反应:Na2O+H2O=2OH-+2Na+
H.将氧化钡与稀硫酸混合:
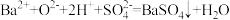
I.碳酸钙与稀盐酸制备二氧化碳:

J.CuSO4溶液中滴加Ba(OH)2溶液:Cu2++2OH-=Cu(OH)2↓
K.将铝片插入硝酸银溶液中:
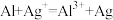
L.铁投入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如下图为铁及其化合物的“价一类”二维图。
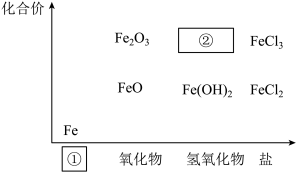
(1)填写二维图缺失的类别①___________ 和化学式②___________ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2②Fe③NaOH④H2SO4⑤AgNO3
i.从物质类别上看,FeCl3属于___________ ,可能与___________ 发生反应(填序号)。
ii.从化合价角度看,Fe3+具有___________ 性,可能与___________ 发生反应(填序号)。
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:Cu+2FeCl3=CuCl2+2FeCl2
①FeCl3在反应中作___________ 剂。
②该反应的离子方程式为___________ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2②Fe③NaOH④H2SO4⑤AgNO3
i.从物质类别上看,FeCl3属于
ii.从化合价角度看,Fe3+具有
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:Cu+2FeCl3=CuCl2+2FeCl2
①FeCl3在反应中作
②该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)简单鉴别Fe(OH)3胶体和FeCl3溶液的方法是_______________ 。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请用双线桥表示出电子转移的方向和数目_____________________
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则可检出待测液中含有的金属阳离子是_____ ;
②验证该溶液中含有Fe2+,正确的实验方法是_______ (用字母代号填)。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
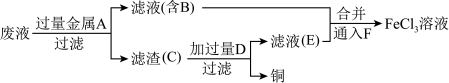
①滤渣C的主要成分的化学式为_______ 、_______ 。
②加过量D发生反应的离子方程式为__________________________________ 。
③通入F发生反应的化学方程式为___________________________________ 。
(1)简单鉴别Fe(OH)3胶体和FeCl3溶液的方法是
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请用双线桥表示出电子转移的方向和数目
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则可检出待测液中含有的金属阳离子是
②验证该溶液中含有Fe2+,正确的实验方法是
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:

①滤渣C的主要成分的化学式为
②加过量D发生反应的离子方程式为
③通入F发生反应的化学方程式为
您最近一年使用:0次





