名校
解题方法
1 . 某小组同学通过实验研究 溶液与Cu粉发生的氧化还原反应。实验记录如下:
溶液与Cu粉发生的氧化还原反应。实验记录如下:
下列说法不正确 的是
 溶液与Cu粉发生的氧化还原反应。实验记录如下:
溶液与Cu粉发生的氧化还原反应。实验记录如下:| 序号 | Ⅰ | Ⅱ | Ⅲ |
| 实验步骤 | 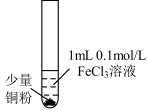 充分振荡,加2mL蒸馏水 | 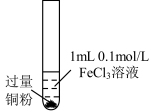 充分振荡,加入2mL蒸馏水 |  充分振荡,加入2mL蒸馏水 |
| 实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
A.实验Ⅰ、Ⅱ、Ⅲ中均涉及 被还原 被还原 |
| B.对比实验Ⅰ、Ⅱ说明白色沉淀的产生与铜粉的量有关 |
C.实验Ⅱ、Ⅲ中加入蒸馏水后 不相同 不相同 |
| D.向实验Ⅲ反应后的溶液中加入饱和NaCl溶液不可能出现白色沉淀 |
您最近一年使用:0次
2021-10-12更新
|
347次组卷
|
3卷引用:广东省深圳外国语学校高中园2023-2024学年高一上学期期末考试 化学试卷
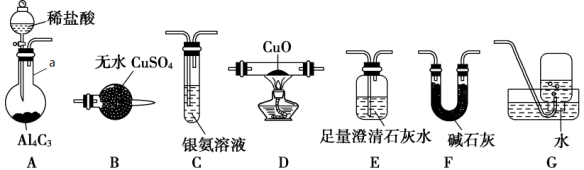
2 . 甲烷在加热条件下可还原氧化铜,某化学小组利用如图装置探究其反应产物。
查阅资料:①CO能与银氨溶液反应:
②Cu2O为红色,能发生反应: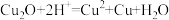
(1)仪器a的名称是___________ ,装置A中反应的化学方程式为___________ 。
(2)按气流方向各装置从左到右的连接顺序为A→F→D→___________→___________→___________→G(填字母编号)。___________
(3)已知气体产物中含有CO,则装置C中可观察到的现象是___________ ;装置F的作用为___________ 。
(4)当反应结束后,装置D处试管中固体全部变为红色。
①设计简单实验证明红色固体中含有 :
:___________ 。
②若红色固体为单质,且产物中含碳氧化物的物质的量之比为 ,则D处发生的反应化学方程式是
,则D处发生的反应化学方程式是___________ 。

查阅资料:①CO能与银氨溶液反应:

②Cu2O为红色,能发生反应:
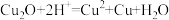
(1)仪器a的名称是
(2)按气流方向各装置从左到右的连接顺序为A→F→D→___________→___________→___________→G(填字母编号)。
(3)已知气体产物中含有CO,则装置C中可观察到的现象是
(4)当反应结束后,装置D处试管中固体全部变为红色。
①设计简单实验证明红色固体中含有
 :
:②若红色固体为单质,且产物中含碳氧化物的物质的量之比为
 ,则D处发生的反应化学方程式是
,则D处发生的反应化学方程式是
您最近一年使用:0次
3 . 铜及其化合物在生产生活中有广泛应用
(1)工业上以黄铜矿(CuFeS2) 为原料,采用火法熔炼工艺生产铜的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑ 该反应的氧化剂是
6Cu+SO2↑ 该反应的氧化剂是________________ ,验证SO2的方法是________________ 。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜。温度控制在50℃~60℃的原因有:①加快反应速率;②___________ 。在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热,可生成CuC1沉淀,写出生成CuCl的离子方程式______________ 。
(3)碱式碳酸铜在有机催化剂、烟火制造和颜料、农药生产中有广泛的应用。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备碱式碳酸铜的流程如下:
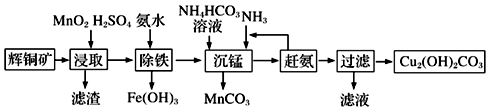
①辉铜矿在浸取前要富集与粉碎,粉碎的好处是___________ 。
②浸取过程中可得到一种黄色单质,写出浸取时主要反应的化学方程式___________ 。
③“除铁”这一步反应在25℃进行,加入氨水调节溶液pH为4后,溶液中铜离子最大浓度不超过_________ mol/L。(已知Ksp[Cu(OH)2]=2.2×10-20)
(1)工业上以黄铜矿(CuFeS2) 为原料,采用火法熔炼工艺生产铜的中间过程会发生反应:2Cu2O+Cu2S
 6Cu+SO2↑ 该反应的氧化剂是
6Cu+SO2↑ 该反应的氧化剂是(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜。温度控制在50℃~60℃的原因有:①加快反应速率;②
(3)碱式碳酸铜在有机催化剂、烟火制造和颜料、农药生产中有广泛的应用。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备碱式碳酸铜的流程如下:

①辉铜矿在浸取前要富集与粉碎,粉碎的好处是
②浸取过程中可得到一种黄色单质,写出浸取时主要反应的化学方程式
③“除铁”这一步反应在25℃进行,加入氨水调节溶液pH为4后,溶液中铜离子最大浓度不超过
您最近一年使用:0次
2018-08-30更新
|
300次组卷
|
2卷引用:【全国省级联考】广东省2017-2018学年高二第二学期期末检测理科综合化学试题



