1 . 某课外研究小组,用杂铜(含有较多杂质的铜粉),通过不同的途径制取胆矾,实验过程如下:

回答下列问题:
(1)杂铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于_______ 上(用所给仪器下方的字母填空,下同),取用坩埚应使用_______ ,灼烧后的坩埚应放在_______ 上,不能直接放在桌面上。
a. 蒸发皿 b.
蒸发皿 b. 石棉网 c.
石棉网 c. 泥三角 d.
泥三角 d. 表面皿 e.
表面皿 e. 坩埚钳 f.
坩埚钳 f. 试管夹
试管夹
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物。灼烧后含有少量铜的原因可能是_______ (填字母)。
a.灼烧过程中部分氧化铜被有机物还原 b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解生成铜 d.该条件下铜无法被氧气氧化
(3)由粗制氧化铜(含单质铜)通过两种途径抽取胆矾,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是:_______ (从环境和反应物的消耗量角度)。
(4)胆矾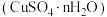 中结晶水n值的测定,步骤如下:ⅰ.称量坩埚的质量,记为
中结晶水n值的测定,步骤如下:ⅰ.称量坩埚的质量,记为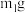 ;ⅱ.称量坩埚和胆矾的质量,记为
;ⅱ.称量坩埚和胆矾的质量,记为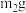 ;ⅲ.加热、冷却、称量坩埚和固体的质量,记为
;ⅲ.加热、冷却、称量坩埚和固体的质量,记为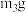 ;ⅳ.再次加热、冷却、称量坩埚和固体的质量,记为
;ⅳ.再次加热、冷却、称量坩埚和固体的质量,记为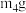 (注:上述过程无
(注:上述过程无 分解)。
分解)。
①胆矾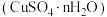 中结晶水n=
中结晶水n=_______ 。
②下列不规范操作会导致测宗结果“偏大”或“偏小”,请将结果填在每种情况后面的横线上:
加热温度过高_______ ;胆矾晶体的颗粒较大_______ ;加热后放在空气中冷却_______ ;粉末未完全变白就停止加热_______ 。

回答下列问题:
(1)杂铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于
a.
 蒸发皿 b.
蒸发皿 b. 石棉网 c.
石棉网 c. 泥三角 d.
泥三角 d. 表面皿 e.
表面皿 e. 坩埚钳 f.
坩埚钳 f. 试管夹
试管夹(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物。灼烧后含有少量铜的原因可能是
a.灼烧过程中部分氧化铜被有机物还原 b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解生成铜 d.该条件下铜无法被氧气氧化
(3)由粗制氧化铜(含单质铜)通过两种途径抽取胆矾,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是:
(4)胆矾
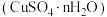 中结晶水n值的测定,步骤如下:ⅰ.称量坩埚的质量,记为
中结晶水n值的测定,步骤如下:ⅰ.称量坩埚的质量,记为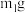 ;ⅱ.称量坩埚和胆矾的质量,记为
;ⅱ.称量坩埚和胆矾的质量,记为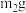 ;ⅲ.加热、冷却、称量坩埚和固体的质量,记为
;ⅲ.加热、冷却、称量坩埚和固体的质量,记为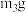 ;ⅳ.再次加热、冷却、称量坩埚和固体的质量,记为
;ⅳ.再次加热、冷却、称量坩埚和固体的质量,记为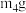 (注:上述过程无
(注:上述过程无 分解)。
分解)。①胆矾
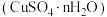 中结晶水n=
中结晶水n=②下列不规范操作会导致测宗结果“偏大”或“偏小”,请将结果填在每种情况后面的横线上:
加热温度过高
您最近一年使用:0次
2022-10-01更新
|
166次组卷
|
3卷引用:江西九师联盟2023届高三9月联考化学试题
名校
解题方法
2 . 查阅资料得知:海绵铜主要成分是Cu,CuCl是一种微溶于乙醇,难溶于水的白色固体,在潮湿的空气中易转化为Cu2(OH)3Cl。
(1)下图是某化工厂制备氯化亚铜的流程:
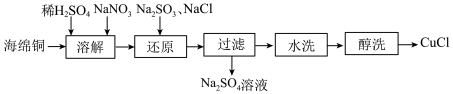
①“溶解”步骤主要反应的离子方程式为_____ ;
②醇洗的目的是______ ;
③已知常温下Cu(OH)2溶度积常数Ksp=2×10-20,要使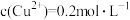 的硫酸铜溶液中的铜离子沉淀比较完全(使铜离子浓度变为原来的
的硫酸铜溶液中的铜离子沉淀比较完全(使铜离子浓度变为原来的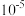 )则应调节溶液pH为
)则应调节溶液pH为______ 以上。
(2)已知次磷酸(H3PO2)是一元中强酸。
①次磷酸钡是一种溶于水的强电解质,向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,写出反应的离子方程式:______ ;
②H3PO2可将溶液中的Ag+还原为银,从而用于化学镀银,反应同时生成P元素最高价氧化物对应的水化物。0.1molH3PO2能还原出金属银______ g;
(1)下图是某化工厂制备氯化亚铜的流程:

①“溶解”步骤主要反应的离子方程式为
②醇洗的目的是
③已知常温下Cu(OH)2溶度积常数Ksp=2×10-20,要使
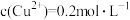 的硫酸铜溶液中的铜离子沉淀比较完全(使铜离子浓度变为原来的
的硫酸铜溶液中的铜离子沉淀比较完全(使铜离子浓度变为原来的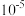 )则应调节溶液pH为
)则应调节溶液pH为(2)已知次磷酸(H3PO2)是一元中强酸。
①次磷酸钡是一种溶于水的强电解质,向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,写出反应的离子方程式:
②H3PO2可将溶液中的Ag+还原为银,从而用于化学镀银,反应同时生成P元素最高价氧化物对应的水化物。0.1molH3PO2能还原出金属银
您最近一年使用:0次
2021-01-21更新
|
184次组卷
|
2卷引用:江西省吉安市第一中学2022-2023学年高一上学期期末考试化学试题
解题方法
3 . 过渡金属的单质及化合物很多有催化性能,氯化铜、氯化亚铜经常用作有机合成催化剂。实验室中用氯气与粗铜(杂质只有Fe)反应,制备铜的氯化物的流程如下。
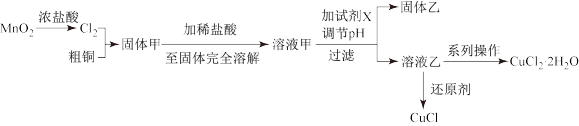
查阅资料:
氯化亚铜:白色微溶于水,在干燥空气中稳定,受潮则易变蓝到棕色,在热水中迅速水解生成氧化铜水合物而呈红色。
氯化铜:从水溶液中结晶时,在26~42℃得到二水物,在15℃以下得到四水物,在15~25.7℃得到三水物,在42℃以上得到一水物,在100℃得到无水物。
(1)现用如图所示的实验仪器及药品制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。
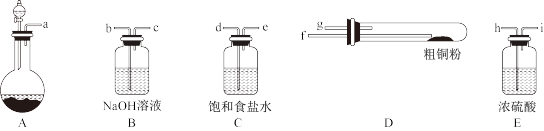
①按气流方向连接各仪器接口顺序是:a→_____ 、_____ →h、i→_____ 、_____ →_____ 。
②本套装置有两个仪器需要加热,加热的顺序为先_____ 后_____ 。
(2)分析流程:
①固体甲需要加稀盐酸溶解,其理由是_____ ;
②溶液甲可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)_____ 。
a Cu(OH)2 b NH3·H2O c CuO d CuSO4
查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________ ,Fe3+完全沉淀时溶液的pH为________ 。(提示:lg2=0.3)
③完成溶液乙到纯净CuCl2·2H2O晶体的系列操作步骤为:加少量盐酸、蒸发浓缩、________ 、_______ 、洗涤、干燥。
(3)向溶液乙中加入适当的还原剂(如SO2、N2H4、SnCl2等),并微热得到CuCl沉淀,写出向乙溶液加入N2H4(氧化产物为无毒气体)的离子方程式:____________ 。
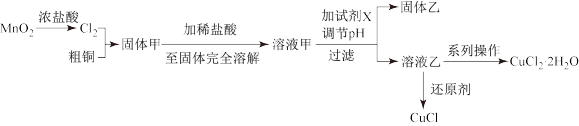
查阅资料:
氯化亚铜:白色微溶于水,在干燥空气中稳定,受潮则易变蓝到棕色,在热水中迅速水解生成氧化铜水合物而呈红色。
氯化铜:从水溶液中结晶时,在26~42℃得到二水物,在15℃以下得到四水物,在15~25.7℃得到三水物,在42℃以上得到一水物,在100℃得到无水物。
(1)现用如图所示的实验仪器及药品制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。

①按气流方向连接各仪器接口顺序是:a→
②本套装置有两个仪器需要加热,加热的顺序为先
(2)分析流程:
①固体甲需要加稀盐酸溶解,其理由是
②溶液甲可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)
a Cu(OH)2 b NH3·H2O c CuO d CuSO4
查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为
③完成溶液乙到纯净CuCl2·2H2O晶体的系列操作步骤为:加少量盐酸、蒸发浓缩、
(3)向溶液乙中加入适当的还原剂(如SO2、N2H4、SnCl2等),并微热得到CuCl沉淀,写出向乙溶液加入N2H4(氧化产物为无毒气体)的离子方程式:
您最近一年使用:0次



