名校
1 . 下列关于化学反应与能量的说法中,不正确 的是
| A.化学反应必然伴随发生能量变化 |
| B.Na与H2O的反应属于放热反应 |
| C.Ba(OH)2·8H2O与NH4Cl的反应属于放热反应 |
| D.化学变化中的能量变化主要是由化学键变化引起的 |
您最近一年使用:0次
2021-05-14更新
|
288次组卷
|
4卷引用:专题1.1.1 反应热与焓变(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)
(已下线)专题1.1.1 反应热与焓变(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)新疆巴楚县第一中学2021-2022学年高二上学期期中考试化学试题北京市第六十六中学2020-2021学年高一下学期期中考试化学试题北京市第四十三中学2021-2022学年高一下学期期中考试化学试题
2 . 下列说法正确的是
| A.水是一次能源,水煤气是二次能源,天然气是可再生能源 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
D.Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3+10H2O  =+80 kJ·mol-1能自发进行,原因是体系有自发向混乱度增大的方向转变的倾向 =+80 kJ·mol-1能自发进行,原因是体系有自发向混乱度增大的方向转变的倾向 |
您最近一年使用:0次
名校
3 . 已知某反应的能量变化如图所示,下列说法正确的是


| A.该反应可用于表示Mg与硫酸反应 |
| B.该反应只有在加热条件下才能进行 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应可以用于表示CaCO3受热分解的反应 |
您最近一年使用:0次
2021-05-12更新
|
1033次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2023-2024学年高二上学期开学考试化学试题
名校
4 . 下列说法正确的是
| A.只有氧化还原反应才是放热反应 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.放热的反应在常温下一定很容易发生 |
| D.反应是放热还是吸热看反应物和生成物所具有的总能量的相对大小 |
您最近一年使用:0次
2021-05-12更新
|
202次组卷
|
3卷引用:第一节 化学反应与能量的变化(第1课时 焓变 反应热)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)
(已下线)第一节 化学反应与能量的变化(第1课时 焓变 反应热)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)吉林省长春外国语学校2020-2021学年高一下学期期中考试化学(理科)试题河北省石家庄市第二十三中学2020-2021学年高一第二学期5月月考化学试题
解题方法
5 . 20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是会在反应物转化为生成物的过程中经过一个高能量的过渡态。下图是NO2与CO反应生成CO2和NO过程中的能量变化示意图。下列说法不正确的是
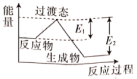

| A.该反应是放热反应 |
| B.该反应中反应物断键吸收的总能量比生成物成键释放的总能量低 |
| C.反应NO2+CO=CO2+NO的能量差为E2-E1 |
| D.反应NO2+CO=CO2+NO中既有共价键形成又有离子键形成 |
您最近一年使用:0次
名校
6 . 碳酸钠晶体(Na2CO3·10H2O)失水可得到Na2CO3·H2O(s)或Na2CO3(s),两个化学反应的能量变化示意图如下:
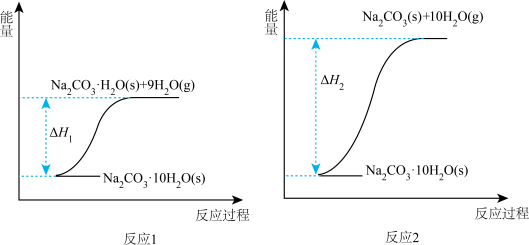
| A.∆H1<0 |
| B.碳酸钠晶体(Na2CO3·10H2O)失水不是化学变化 |
| C.Na2CO3·H2O(s)失水生成Na2CO3(s):∆H=∆H1-∆H2 |
| D.向Na2CO3(s)中滴加几滴水,温度升高 |
您最近一年使用:0次
2021-05-10更新
|
399次组卷
|
3卷引用:北京师范大学附属中学2023-2024学年高二下学期期中考试化学试题
7 . 下列各反应的能量变化分别用如下形式的示意图表示,其中正确的是
| A | B | C | D |
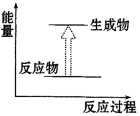 |  | 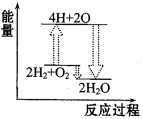 |  |
| 化石燃料的燃烧 | 植物的光合作用 | 氢气与氧气反应 | 氢气与氯气反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列关于化学反应与能量变化说法不正确的是
①在高温、高压条件下发生的反应一定是吸热反应
②H2在Cl2中燃烧、H2与Cl2的混合气体光照发生爆炸,都放出热量,且后者放出热量多
③水汽化需要吸收能量,所以水汽化属于吸热反应
④对于吸热反应,生成物总能量一定低于反应物总能量
⑤X(s)=Y(s)是放热反应,则X比Y稳定
⑥等量的硫蒸气和固态硫分别完全燃烧,后者放出的热量更多
①在高温、高压条件下发生的反应一定是吸热反应
②H2在Cl2中燃烧、H2与Cl2的混合气体光照发生爆炸,都放出热量,且后者放出热量多
③水汽化需要吸收能量,所以水汽化属于吸热反应
④对于吸热反应,生成物总能量一定低于反应物总能量
⑤X(s)=Y(s)是放热反应,则X比Y稳定
⑥等量的硫蒸气和固态硫分别完全燃烧,后者放出的热量更多
| A.①②③④⑤⑥ | B.③④⑤⑥ | C.①②③⑤⑥ | D.②③④ |
您最近一年使用:0次
2021-05-10更新
|
263次组卷
|
2卷引用:河南省原阳县第三高级中学2020-2021学年高二下学期第三次月考化学试题
名校
9 . 下列过程中的能量变化情况符合图示关系的是


| A.酸与碱的中和反应 |
| B.H+Cl→H-Cl |
| C.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
| D.氧化钙与水反应制熟石灰 |
您最近一年使用:0次
2021-05-10更新
|
196次组卷
|
3卷引用:广东仲元中学2021-2022学年高二上学期开学检测 化学试题
广东仲元中学2021-2022学年高二上学期开学检测 化学试题宁夏青铜峡市高级中学2020-2021学年高一下学期期中考试化学试题(已下线)专题04 化学反应与热能【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)
名校
10 . 下列说法中正确的是
| A.伴随能量变化的物质变化一定是化学变化 |
| B.吸热反应必须在加热条件下才能发生,而放热反应则无须加热 |
| C.根据能量守恒,在化学反应中,反应物的总能量与生成物总能量一定相等 |
| D.物质发生化学变化的同时都伴随能量变化 |
您最近一年使用:0次
2021-05-07更新
|
137次组卷
|
3卷引用:江苏省马坝高级中学2020-2021学年高二下学期期中考试化学试题



