溶液,发生反应:
溶液,发生反应: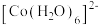 (粉红色)
(粉红色)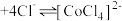 (蓝色)
(蓝色)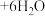 ,溶液颜色由粉红色变为蓝色。下列说法错误的是
,溶液颜色由粉红色变为蓝色。下列说法错误的是A.基态 原子的价电子排布式为 原子的价电子排布式为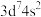 |
| B.该反应为吸热反应 |
C.向冷 溶液中加入 溶液中加入 固体,溶液变蓝 固体,溶液变蓝 |
| D.加水稀释,平衡正移 |
| A.“蒸粮”时可适当鼓风加快燃烧速率 | B.“拌曲”加入的酒曲在酿酒时起到催化作用 |
C.“堆酵”时升温是因为此过程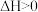 | D.“馏酒”的原理即实验操作中的“蒸馏” |
 经两步反应氧化成
经两步反应氧化成 ,两步反应的能量变化如图。
,两步反应的能量变化如图。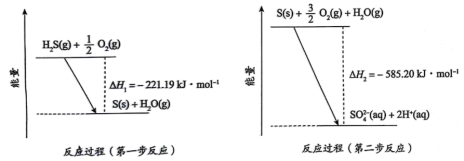
A.O的非金属性大于S,推知热稳定性: |
| B.两步反应中化学键断裂吸收的总能量均小于化学键形成释放的总能量 |
C.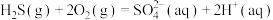 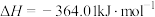 |
D.结合 的燃烧热,可求算 的燃烧热,可求算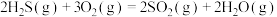 的 的 |
| A.铝片与稀硫酸的反应 | B.红热的焦炭与氧气的反应 |
| C.NaOH溶液与稀盐酸的反应 | D.石灰石高温分解 |
 (过二硫酸根)和
(过二硫酸根)和 的溶液中,发生反应:
的溶液中,发生反应: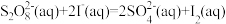 ,其分解机理及反应过程中的能量变化如图所示:
,其分解机理及反应过程中的能量变化如图所示:
| A.步骤②决定总反应的速率 |
| B.步骤①是吸热过程,步骤②是放热过程 |
C.由反应机理可以看出, 是中间产物 是中间产物 |
| D.反应中S元素不参与电子转移 |
 的制备反应如下:
的制备反应如下: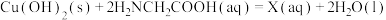
 有两种结构,分别为
有两种结构,分别为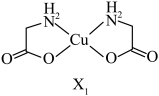 和
和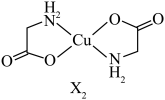
 ,最终转化为
,最终转化为 。下列说法
。下列说法A. 中 中 的配位数为4 的配位数为4 | B. 中 中 与配位原子形成的空间结构与 与配位原子形成的空间结构与 类似 类似 |
C.极性: | D.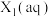 转化为 转化为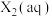 是放热反应 是放热反应 |
|
|
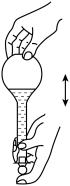
| A.通过注射器活塞移动验证钠与水反应放热 | B.探究浓度对反应速率的影响 |
|
|
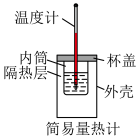
| C.检查容量瓶是否漏液 | D.测定中和热 |
| A.A | B.B | C.C | D.D |
 。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和
。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和 的浓度随时间变化。
的浓度随时间变化。 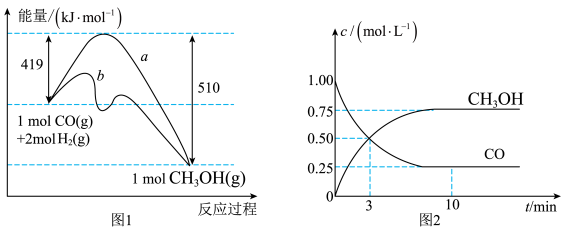
(1)在图1中,曲线
(2)该反应属于
(3)增大反应体系压强,则该反应化学平衡常数
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)图中,A是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在B中实现铁上镀铜:

②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为
|
|
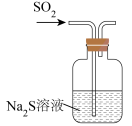
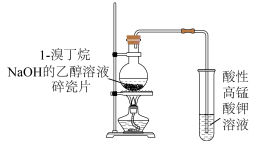
A.验证 氧化性 氧化性 | B.验证1-溴丁烷的消去反应 |
|
|
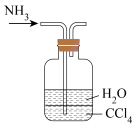
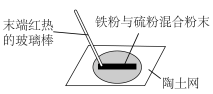
| C.制氨水 | D.证明Fe与S反应放热 |
| A.A | B.B | C.C | D.D |
10 . 水是清洁、可持续的氢能来源。利用太阳能从水中获取氢气符合可持续发展的理念。
“太阳能直接热分解水制氢”通过集中阳光产生2000K以上高温,促使H2O分解为H2和O2;若温度进一步升高至5000K,H2与O2会分解为气态原子。
(1)H2O分解过程中断裂的化学键属于
A.离子键 B.极性共价键 C.非极性共价键
(2)在相同条件下,同时存在如下两个过程:
ⅰ.2H(g)+O(g)=H2O(g)
ⅱ.H2(g)+ O2(g)=H2O(g)
O2(g)=H2O(g)
比较下列量的相对大小(均从选项中选择):①放出热量
A.ⅰ>ⅱ B.ⅰ=ⅱ C.ⅰ<ⅱ