解题方法
1 . 甲醇是重要的化工原料,研究甲醇的制备及用途在工业上有重要的意义。
(1)一种重要的工业制备甲醇的反应为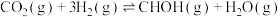 △H
△H
已知:①

②

试计算制备反应的△H=_______ 。
(2)在某恒温恒压容器中进行反应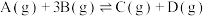 ,达到平衡时容器容积为1 L。A、B、C、D的物质的量依次为3 mol、1 mol、1 mol、1 mol;若往容器中再通入6 mol A,此时平衡
,达到平衡时容器容积为1 L。A、B、C、D的物质的量依次为3 mol、1 mol、1 mol、1 mol;若往容器中再通入6 mol A,此时平衡_______ (填“正向”“逆向”或“不”)移动,该反应的△H _______ (填“大于”或“小于”)0。
(3)对于反应 ,
,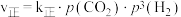 ,
, 。其中
。其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。在540K下,按初始投料比
分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。在540K下,按初始投料比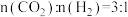 、
、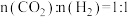 、
、 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:
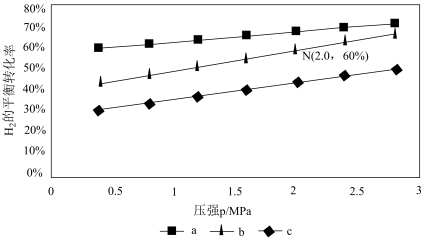
①比较a、b、c各曲线所表示的投料比大小顺序为_______ (用字母表示)。
②点N在线b上,计算540 K的压强平衡常数Kp=_______ (用平衡分压代替平衡浓度计算)。
③540K条件下,某容器测得某时刻 MPa,
MPa, MPa,
MPa,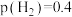 MPa,此时
MPa,此时
_______ 。
(4)甲醇催化可制取丙烯,反应为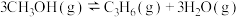 ,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为
,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为 (Ea为活化能,k为速率常数,R和C为常数)。
(Ea为活化能,k为速率常数,R和C为常数)。
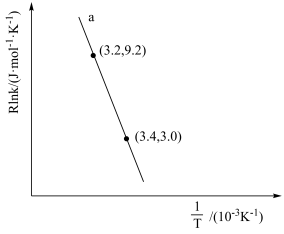
①该反应的活化能Ea=_______  。
。
②当使用更高效催化剂时,在图中画出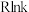 与
与 关系的示意图。
关系的示意图。_______
(1)一种重要的工业制备甲醇的反应为
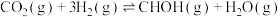 △H
△H已知:①


②


试计算制备反应的△H=
(2)在某恒温恒压容器中进行反应
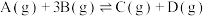 ,达到平衡时容器容积为1 L。A、B、C、D的物质的量依次为3 mol、1 mol、1 mol、1 mol;若往容器中再通入6 mol A,此时平衡
,达到平衡时容器容积为1 L。A、B、C、D的物质的量依次为3 mol、1 mol、1 mol、1 mol;若往容器中再通入6 mol A,此时平衡(3)对于反应
 ,
,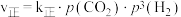 ,
, 。其中
。其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。在540K下,按初始投料比
分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。在540K下,按初始投料比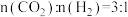 、
、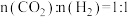 、
、 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:
①比较a、b、c各曲线所表示的投料比大小顺序为
②点N在线b上,计算540 K的压强平衡常数Kp=
③540K条件下,某容器测得某时刻
 MPa,
MPa, MPa,
MPa,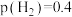 MPa,此时
MPa,此时
(4)甲醇催化可制取丙烯,反应为
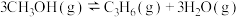 ,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为
,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为 (Ea为活化能,k为速率常数,R和C为常数)。
(Ea为活化能,k为速率常数,R和C为常数)。
①该反应的活化能Ea=
 。
。②当使用更高效催化剂时,在图中画出
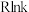 与
与 关系的示意图。
关系的示意图。
您最近一年使用:0次
2022-05-10更新
|
328次组卷
|
4卷引用:湖南省娄底市2022届高三上学期第二次模拟考试化学试题
湖南省娄底市2022届高三上学期第二次模拟考试化学试题(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编湖南省株洲市北附高级中学2022-2023学年高三上学期第五次月考化学试题湖南省株洲市十三中2022-2023学年高三第五次月考化学试题



