名校
解题方法
1 . 周期表中ⅢA族单质及其化合物应用广泛。BF3极易水解,生成HBF4(HBF4在水中完全电离为H+和 )和硼酸(H3BO3)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下Al2O3和焦炭在氯气的氛围中获得AlCl3。GaN的结构与晶体硅类似,是第三代半导体研究的热点。铊(TI)位于元素周期表中第6周期,于1861年发现。下列物质性质与用途具有对应关系的是
)和硼酸(H3BO3)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下Al2O3和焦炭在氯气的氛围中获得AlCl3。GaN的结构与晶体硅类似,是第三代半导体研究的热点。铊(TI)位于元素周期表中第6周期,于1861年发现。下列物质性质与用途具有对应关系的是
 )和硼酸(H3BO3)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下Al2O3和焦炭在氯气的氛围中获得AlCl3。GaN的结构与晶体硅类似,是第三代半导体研究的热点。铊(TI)位于元素周期表中第6周期,于1861年发现。下列物质性质与用途具有对应关系的是
)和硼酸(H3BO3)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下Al2O3和焦炭在氯气的氛围中获得AlCl3。GaN的结构与晶体硅类似,是第三代半导体研究的热点。铊(TI)位于元素周期表中第6周期,于1861年发现。下列物质性质与用途具有对应关系的是| A.BF3极易水解,可用作有机反应的催化剂 |
| B.硼酸甲酯具有挥发性,可用作木材防腐剂 |
| C.GaN硬度大,可用作半导体材料 |
| D.Al(OH)3受热分解,可用作阻燃剂 |
您最近半年使用:0次
名校
解题方法
2 . 如图表示某化学反应在使用催化剂(b曲线)和未使用催化剂(a曲线)时,反应进程和能量的对应关系。下列说法一定正确的是
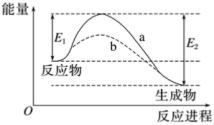

| A.a与b相比,b的活化能更高 |
| B.催化剂的使用,改变了反应的ΔH,因而能大大加快反应速率 |
| C.a与b相比,b中活化分子的百分数更高 |
| D.a与b相比,a的反应速率更快 |
您最近半年使用:0次
2023高三·全国·专题练习
3 . 氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氨气直接合成氨。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
常温下,大气固氮的倾向___________ 工业固氮(填“大于”或“小于”)。
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g)反应制备NH3(l)的热化学方程式为:___________ 。
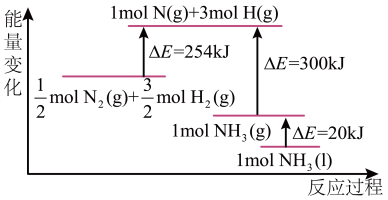
(3)T ℃时,在2 L恒容密闭容器中加入1.2 mol N2和2 mol H2模拟一定条件下工业固氮[N2(g)+3H2(g) 2NH3(g)],体系中n(NH3)随时间的变化如图所示:
2NH3(g)],体系中n(NH3)随时间的变化如图所示:
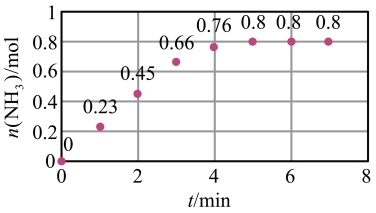
①前2分钟内的平均反应速率v(NH3)=___________ mol·L-1·min-1;
②有关工业固氮的说法正确的是___________ (选填序号)。
A.使用催化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500 ℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
③T ℃时,该反应的平衡常数为___________ ;
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol/min)与催化剂的对应关系如表所示。
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是 ___________ (填化学式)。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
| 反应 | 大气固氮 N2(g)+O2(g)  2NO(g) 2NO(g) | 工业固氮 N2(g)+3H2(g)  2NH3(g) 2NH3(g) | ||||
| 温度/℃ | 25 | 2 000 | 25 | 350 | 400 | 450 |
| 平衡常数K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.504 | 0.152 |
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g)反应制备NH3(l)的热化学方程式为:

(3)T ℃时,在2 L恒容密闭容器中加入1.2 mol N2和2 mol H2模拟一定条件下工业固氮[N2(g)+3H2(g)
 2NH3(g)],体系中n(NH3)随时间的变化如图所示:
2NH3(g)],体系中n(NH3)随时间的变化如图所示:
①前2分钟内的平均反应速率v(NH3)=
②有关工业固氮的说法正确的是
A.使用催化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500 ℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
③T ℃时,该反应的平衡常数为
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol/min)与催化剂的对应关系如表所示。
| 催化剂 | Fe | Pd | Ru | Rh | Pt | Ni |
| 初始速率 | 0.5 | 1.8 | 7.9 | 4.0 | 2.2 | 3.0 |
您最近半年使用:0次
名校
解题方法
4 . 图像可以直观地体现出化学变化中各种变化关系,加深对化学知识的理解。下列图像能够正确表示对应关系的是
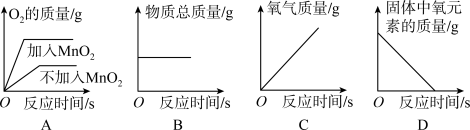

| A.用两份等质量的氯酸钾制取氧气 | B.木炭在盛有氧气的密闭容器中燃烧 |
| C.一定质量的过氧化氢溶液和二氧化锰制取氧气 | D.加热一定质量的高锰酸钾 |
您最近半年使用:0次
名校
5 . 下列实验操作及现象正确,且与解释或结论存在对应关系是
| 选项 | 实验操作及现象 | 解释或结论 |
| A | 向双氧水中滴加酸性 溶液,迅速有气泡生成 溶液,迅速有气泡生成 |  对 对 分解具有催化作用 分解具有催化作用 |
| B | 向 溶液中滴入足量氯水和 溶液中滴入足量氯水和 ,振荡、静置、分层;再向上层溶液中加入KSCN溶液,下层溶液呈紫红色,上层溶液变为血红色。 ,振荡、静置、分层;再向上层溶液中加入KSCN溶液,下层溶液呈紫红色,上层溶液变为血红色。 | 证明还原性: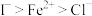 |
| C | 向硫酸酸化的食盐溶液中加入KI溶液和几滴淀粉溶液,溶液未变蓝色 | 该食盐不是含碘盐 |
| D | 向 溶液中滴入稀盐酸,出现白色凝胶 溶液中滴入稀盐酸,出现白色凝胶 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-05-30更新
|
73次组卷
|
2卷引用:山东省滨州市部分学校2022-2023学年高一下学期5月联考化学试题
解题方法
6 . 下列实验的“操作和现象”与“推测或结论”对应关系正确的是
选项 | 操作和现象 | 推测或结论 |
A | 向H2O2溶液中加入几滴FeCl3溶液,溶液中产生气泡 | 发生的离子反应为: |
B | 用铁丝蘸取少量某溶液进行焰色反应,火焰呈黄色 | 该溶液含有钠盐 |
C | 向Al与Fe2O3反应后的固体产物中先加稀硫酸溶解,再加入几滴KSCN溶液,溶液不变红 | 无法证明反应后固体产物中是否含有Fe2O3 |
D | 向无水乙醇中加入浓硫酸,加热至170℃,将产生的气体通入酸性高锰酸钾溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 氨是人科学技术发史上的一项重大突,目前工业上用氢气和氨气直接合成氨。
(1)固氮一直是科学家致力研究的要课题,有关热力学数据如下:
常温下,大气固氮的倾向_______ 工业固氮(填“大于”或“小于”)
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g) 反应制备NH3(g) 的热化学方程式为:_______ ;

(3)T℃时,在2L恒容密闭容器中加入1.2mol N2和2mol H2模拟一定条件下工业固氮[N2(g)+3H2(g) 2NH3(g)],体系中n(NH3)随时间的变化如图所示;
2NH3(g)],体系中n(NH3)随时间的变化如图所示;

①前2分钟内的平均反应速率v(NH3)=_______ mol·L-1·min-1;
②有关工业固氮的说法正确的是_______ (选填序号) 。
A.使用化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500℃左右有利于反应向正方向行
D.增大压强有利于加快反应速率,所以压强大越好
③T℃时,该反应的平衡常数为_______ ;
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位: mmol/min)与化剂的对应关系如表所示。
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是 _______ (填化学式)
(1)固氮一直是科学家致力研究的要课题,有关热力学数据如下:
| 反应 | 大气固氮N2(g)+O2(g)  2NO(g) 2NO(g) | 工业固氮N2(g)+3H2(g)  2NH3(g) 2NH3(g) | ||||
| 温度/℃ | 25 | 2000 | 25 | 350 | 400 | 450 |
| 平衡常数K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.504 | 0.152 |
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g) 反应制备NH3(g) 的热化学方程式为:

(3)T℃时,在2L恒容密闭容器中加入1.2mol N2和2mol H2模拟一定条件下工业固氮[N2(g)+3H2(g)
 2NH3(g)],体系中n(NH3)随时间的变化如图所示;
2NH3(g)],体系中n(NH3)随时间的变化如图所示;
①前2分钟内的平均反应速率v(NH3)=
②有关工业固氮的说法正确的是
A.使用化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500℃左右有利于反应向正方向行
D.增大压强有利于加快反应速率,所以压强大越好
③T℃时,该反应的平衡常数为
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位: mmol/min)与化剂的对应关系如表所示。
| 催化剂 | Fe | Pd | Ru | Rh | Pt | Ni |
| 初始速率 | 0.5 | 1.8 | 7.9 | 4.0 | 2.2 | 3.0 |
您最近半年使用:0次
名校
解题方法
8 . 下列事实与括号中物质的性质对应关系不正确的是
| A.将鲜花至于装满氯气的集气瓶中褪色(氯气具有漂白性) |
| B.蔗糖遇浓硫酸会变黑膨胀(浓硫酸有强氧化性和脱水性) |
| C.双氧水中加入FeCl3溶液有气体快速放出(Fe3+能催化H2O2分解) |
| D.葡萄糖与银氨溶液共热,有银镜现象(葡萄糖有还原性) |
您最近半年使用:0次
名校
9 . 氯、氮、硫等及其化合物性质研究。如图是氮、硫元素的各种价态与物质类别的对应关系:

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的化学方程式为____ 。
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,写出化学方程式____ 。
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl b.NO+NO2+H2O 2HNO2 c.HClO+HNO2=HNO3+HCl
2HNO2 c.HClO+HNO2=HNO3+HCl
下列分析正确的是___ 。
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:
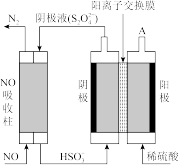
从A口中出来的物质的是____ 。写出电解池阴极的电极反应式____ 。
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
①上述实验中a=____ ,b=____ 。
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是____ (填实验编号)。

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的化学方程式为
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,写出化学方程式
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl b.NO+NO2+H2O
 2HNO2 c.HClO+HNO2=HNO3+HCl
2HNO2 c.HClO+HNO2=HNO3+HCl下列分析正确的是
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:

从A口中出来的物质的是
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO
 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | b | 124 |
| III | 350 | a | 5.80×10-3 | 82 |
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是
您最近半年使用:0次
10 . 下列实验的“操作和现象”与“推测或结论”对应关系一定正确的是
| 操作和现象 | 推测或结论 | |
| A | 常温下,同时向盛有5%和30%双氧水的试管中各加入一粒相同大小的 后,盛有30%双氧水的试管中反应更剧烈 后,盛有30%双氧水的试管中反应更剧烈 | 盛有30%双氧水的试管最先停止冒气泡 |
| B | 用铁丝蘸取少量某溶液进行焰色反应,火焰呈黄色 | 该溶液含有钠盐 |
| C | 某气体能使湿润的红色石蕊试纸变蓝 | 该气体的水溶液显碱性 |
| D | 向无水乙醇中加入浓 ,加热至 ,加热至 ,将产生的气体通入酸性 ,将产生的气体通入酸性 溶液,红色褪去 溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次




