1 . 甲烷是一种重要的化工原料,在生产中有着重要的应用。
I.工业上以CH4和H2O为原料,通过下列反应来制备甲醇:
①CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.0kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H=-129.0kJ•mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为___________ 。
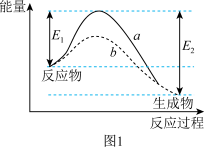
(2)1932年,美国理论化学家亨利·艾琳等人在统计力学和量子力学的基础上建立了过渡态理论,认为催化剂主要是通过改变过渡态物质而降低了活化能。对于反应②,在使用和未使用催化剂时,反应过程和能量的对应关系如图1所示。使用了催化剂的曲线是___________ (填“a”或“b”);断裂反应物中的化学键吸收的总能量___________ (填“>”、“<”或“=”)形成生成物中的化学键释放的总能量。
II.甲烷还可以制作燃料电池。如图2是甲烷燃料电池原理示意图,回答下列问题:
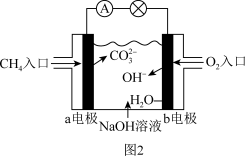
已知:总反应为CH4+2O2+2NaOH=Na2CO3+3H2O
(3)该装置的能量转换形式是___________ 。
(4)电池的负极是___________ (填“a”或“b”),该极的电极反应是 ___________ 。
(5)电池工作一段时间后电解质溶液的碱性___________ (填“增强”、“减弱”或“不变”)。
(6)标准状况下,消耗3.36L甲烷,电路中转移的电子数目为___________ 。
I.工业上以CH4和H2O为原料,通过下列反应来制备甲醇:
①CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.0kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H=-129.0kJ•mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为
(2)1932年,美国理论化学家亨利·艾琳等人在统计力学和量子力学的基础上建立了过渡态理论,认为催化剂主要是通过改变过渡态物质而降低了活化能。对于反应②,在使用和未使用催化剂时,反应过程和能量的对应关系如图1所示。使用了催化剂的曲线是

II.甲烷还可以制作燃料电池。如图2是甲烷燃料电池原理示意图,回答下列问题:

已知:总反应为CH4+2O2+2NaOH=Na2CO3+3H2O
(3)该装置的能量转换形式是
(4)电池的负极是
(5)电池工作一段时间后电解质溶液的碱性
(6)标准状况下,消耗3.36L甲烷,电路中转移的电子数目为
您最近半年使用:0次
名校
2 . 如图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法正确的是
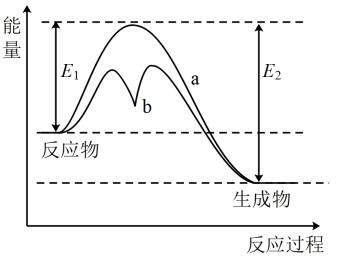

| A.反应为吸热反应 |
| B.a与b相比,a的反应速率更快 |
| C.a与b相比,反应的平衡常数一定不同 |
| D.反应物断键吸收的总能量小于生成物成键释放的总能量 |
您最近半年使用:0次
2022-02-18更新
|
211次组卷
|
2卷引用:广东省广州真光中学2021-2022学年高二上学期12月月考化学试题
名校
解题方法
3 . 下列事实与括号中物质的性质对应关系不正确的是
| A.将鲜花至于装满氯气的集气瓶中褪色(氯气具有漂白性) |
| B.蔗糖遇浓硫酸会变黑膨胀(浓硫酸有强氧化性和脱水性) |
| C.双氧水中加入FeCl3溶液有气体快速放出(Fe3+能催化H2O2分解) |
| D.葡萄糖与银氨溶液共热,有银镜现象(葡萄糖有还原性) |
您最近半年使用:0次
名校
解题方法
4 . 如图,这种具有不同能量的分子百分数和能量的对应关系图,叫做一定温度下分子能量分布曲线图。图中E表示分子平均能量,Ec是活化分子具有的最低能量。下列说法不正确的是
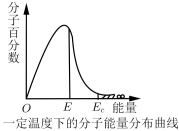

| A.图中Ec与E之差表示活化能 |
| B.升高温度,图中阴影部分面积会增大 |
| C.使用合适的催化剂,E不变,Ec变小 |
| D.能量大于Ec的分子间发生的碰撞一定是有效碰撞 |
您最近半年使用:0次
2020-03-05更新
|
258次组卷
|
3卷引用:湖北省荆州市2020届高三上学期质量检测(一) 化学试题
12-13高二上·河南许昌·期末
5 . 下图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法一定正确的是
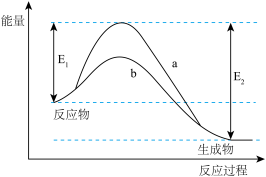

| A.该反应为吸热反应 |
| B.a与b相比,a的反应速率更快 |
| C.a与b相比,反应的平衡常数一定不同 |
| D.反应物吸收的总能量小于生成物释放的总能量 |
您最近半年使用:0次
2019-04-14更新
|
352次组卷
|
3卷引用:2011-2012学年河南省许昌部分学校高二上学期期末联考化学试卷
(已下线)2011-2012学年河南省许昌部分学校高二上学期期末联考化学试卷【区级联考】上海市黄浦区2019届高三下学期等级考二模试卷化学试题2019-2020学年新人教版必修2同步练习题:6.1化学反应与能量变化
名校
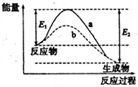
6 . 右图表示某可逆反应:N2(g)+3H2(g) 2NH3(g) △H在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法正确的是
2NH3(g) △H在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法正确的是
 2NH3(g) △H在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法正确的是
2NH3(g) △H在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法正确的是
| A.反应物的总键能小于生成物的总键能 |
| B.如果对上述反应加压,平衡正向移动,△H减小 |
| C.a与b相比,反应的平衡常数一定不同 |
| D.a与b相比,a的反应速率更快 |
您最近半年使用:0次
2017-12-04更新
|
226次组卷
|
2卷引用:山东省青岛市城阳区2018届高三上学期期中学分认定考试化学试题
7 . 右图衰示可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法正确的是


| A.反应物的总能量大于生成物的总能量 | B.反应产生的热效应Q=E1-E2 |
| C.a与b相比,反应的平衡常数一定不同 | D.a与b相比,a的反应速率更快 |
您最近半年使用:0次
10-11高二下·广东广州·期中
8 . 如图表示某可逆反应在使用和未使用催化剂时,反应进程和能量的对应关系。下列说法一定正确的是 ( )
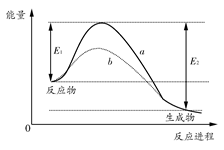

| A.a与b相比,b的活化能更高 |
| B.反应物断键吸收的总能量小于生成物成键释放的总能量 |
| C.a与b相比,反应的平衡常数一定不同 |
| D.a与b相比,a对应的反应速率更快 |
您最近半年使用:0次
2016-12-09更新
|
1405次组卷
|
4卷引用:2010-2011学年广东省白云中学高二下学期期中考试化学试卷
(已下线)2010-2011学年广东省白云中学高二下学期期中考试化学试卷(已下线)2014年高考化学苏教版总复习 7-2 化学反应的方向和限度练习卷2015-2016学年河北省望都中学高二上学期第二次月考化学试卷吉林省松原市乾安县第七中学2020-2021学年高二上学期第一次教学质量检测化学试题
9 . 下列实验“操作和现象”与“结论”对应关系正确的是
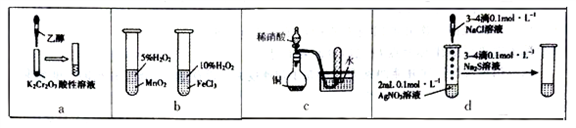

| A.a图,滴加乙醇,试管中橙色溶液变为绿色,乙醇发生取代反应生成乙酸 |
| B.b图,左边试管中产生气泡迅速,说明二氧化锰的催化效果比氯化铁好 |
| C.c图,根据试管中收集到无色气体,能验证铜与稀硝酸的反应产物是NO |
| D.d图,试管中先有白色沉淀,后有黑色沉淀生成,能确定Ksp(AgCl)>Ksp(Ag2S) |
您最近半年使用:0次
解题方法
10 . 苯乙烯是一种很重要的有机化学原料,用途十分广泛。在以水蒸气做稀释剂、存在催化剂的条件下,乙苯催化脱氢可生成苯乙烯。可能发生如下两个反应;
主反应: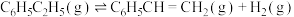
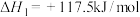 ;
;
副反应: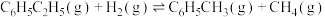
 。
。
回答下列问题:
(1)已知,在 、
、 条件下,
条件下,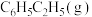 、
、 、
、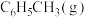 、
、 的燃烧热分别为
的燃烧热分别为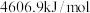 、
、 、
、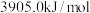 、
、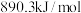 。则
。则
_______  。
。
(2)在某温度、pkPa的条件下,向反应器中充入 气态乙苯发生主反应:
气态乙苯发生主反应: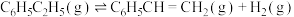 ,其平衡转化率为50%,若向该反应器中充入
,其平衡转化率为50%,若向该反应器中充入 水蒸气作为稀释气(计算时忽略副反应),可将平衡转化率提高至
水蒸气作为稀释气(计算时忽略副反应),可将平衡转化率提高至_______ 。
(3)在不同的温度条件下,以水烃比 投料,在膜反应器中发生乙苯催化脱氢反应
投料,在膜反应器中发生乙苯催化脱氢反应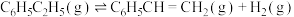 。膜反应器可以通过多孔膜移去
。膜反应器可以通过多孔膜移去 ,提高乙苯的平衡转化率,工作原理如图所示:
,提高乙苯的平衡转化率,工作原理如图所示: 移出率
移出率
 ×100%。
×100%。
①忽略副反应,维持体系总压强p恒定,在温度T时,已知乙苯的平衡转化率为 ,
, 的移出率为b,则在该温度下主反应的平衡常数
的移出率为b,则在该温度下主反应的平衡常数
_______ (用含 、b、p的代数式表示)。
、b、p的代数式表示)。
②乙苯的平衡转化率增长百分数与 的移出率在不同温度条件下的关系如表所示:
的移出率在不同温度条件下的关系如表所示:
高温下副反应程度极小,试说明当温度高于950℃时,乙苯的平衡转化率随 的移出率的变化改变程度不大的原因:
的移出率的变化改变程度不大的原因:_______ 。
③下列说法正确的是_______ (填选项字母)。
A.生成 的总物质的量与苯乙烯相等
的总物质的量与苯乙烯相等
B.因为 被分离至隔离区,故反应器中不发生副反应
被分离至隔离区,故反应器中不发生副反应
C.在恒容的膜反应器中,其他条件不变,增大水烃比,可提高乙苯的转化率
D.当 的分压不再发生变化时,说明主副反应均达到平衡状态
的分压不再发生变化时,说明主副反应均达到平衡状态
(4)有研究者发现,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图所示:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图所示:_______ 。
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应影响较大,如果催化剂表面碱性太强,会降低乙苯的转化率,碱性太强使乙苯转化率降低的原因是_______ (写一点即可)。
③从资源综合利用角度分析, 氧化乙苯脱氢制苯乙烯的优点是
氧化乙苯脱氢制苯乙烯的优点是_______ 。
主反应:
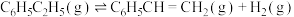
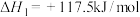 ;
;副反应:
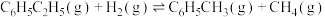
 。
。回答下列问题:
(1)已知,在
 、
、 条件下,
条件下,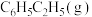 、
、 、
、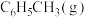 、
、 的燃烧热分别为
的燃烧热分别为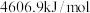 、
、 、
、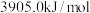 、
、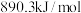 。则
。则
 。
。(2)在某温度、pkPa的条件下,向反应器中充入
 气态乙苯发生主反应:
气态乙苯发生主反应: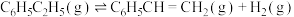 ,其平衡转化率为50%,若向该反应器中充入
,其平衡转化率为50%,若向该反应器中充入 水蒸气作为稀释气(计算时忽略副反应),可将平衡转化率提高至
水蒸气作为稀释气(计算时忽略副反应),可将平衡转化率提高至(3)在不同的温度条件下,以水烃比
 投料,在膜反应器中发生乙苯催化脱氢反应
投料,在膜反应器中发生乙苯催化脱氢反应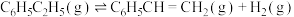 。膜反应器可以通过多孔膜移去
。膜反应器可以通过多孔膜移去 ,提高乙苯的平衡转化率,工作原理如图所示:
,提高乙苯的平衡转化率,工作原理如图所示: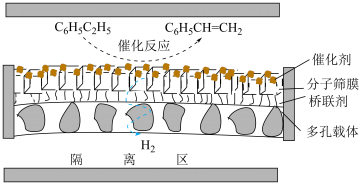
 移出率
移出率
 ×100%。
×100%。①忽略副反应,维持体系总压强p恒定,在温度T时,已知乙苯的平衡转化率为
 ,
, 的移出率为b,则在该温度下主反应的平衡常数
的移出率为b,则在该温度下主反应的平衡常数
 、b、p的代数式表示)。
、b、p的代数式表示)。②乙苯的平衡转化率增长百分数与
 的移出率在不同温度条件下的关系如表所示:
的移出率在不同温度条件下的关系如表所示:| 温度/℃ 增长百分数/%  移出率/% 移出率/% | 700 | 950 | 1000 |
| 60 | 8.43 | 4.38 | 2.77 |
| 80 | 16.8 | 6.1 | 3.8 |
| 90 | 27 | 7.1 | 4.39 |
 的移出率的变化改变程度不大的原因:
的移出率的变化改变程度不大的原因:③下列说法正确的是
A.生成
 的总物质的量与苯乙烯相等
的总物质的量与苯乙烯相等B.因为
 被分离至隔离区,故反应器中不发生副反应
被分离至隔离区,故反应器中不发生副反应C.在恒容的膜反应器中,其他条件不变,增大水烃比,可提高乙苯的转化率
D.当
 的分压不再发生变化时,说明主副反应均达到平衡状态
的分压不再发生变化时,说明主副反应均达到平衡状态(4)有研究者发现,在
 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图所示:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图所示: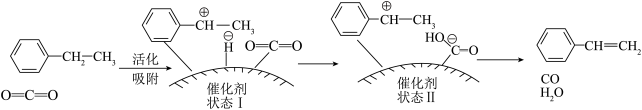
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应影响较大,如果催化剂表面碱性太强,会降低乙苯的转化率,碱性太强使乙苯转化率降低的原因是
③从资源综合利用角度分析,
 氧化乙苯脱氢制苯乙烯的优点是
氧化乙苯脱氢制苯乙烯的优点是
您最近半年使用:0次



