2023高三·全国·专题练习
1 . 氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氨气直接合成氨。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
常温下,大气固氮的倾向___________ 工业固氮(填“大于”或“小于”)。
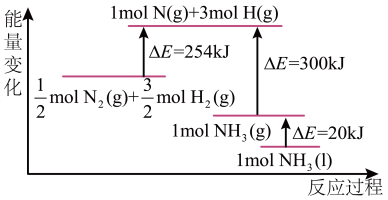
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g)反应制备NH3(l)的热化学方程式为:___________ 。
(3)T ℃时,在2 L恒容密闭容器中加入1.2 mol N2和2 mol H2模拟一定条件下工业固氮[N2(g)+3H2(g) 2NH3(g)],体系中n(NH3)随时间的变化如图所示:
2NH3(g)],体系中n(NH3)随时间的变化如图所示:
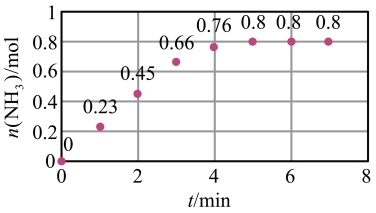
①前2分钟内的平均反应速率v(NH3)=___________ mol·L-1·min-1;
②有关工业固氮的说法正确的是___________ (选填序号)。
A.使用催化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500 ℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
③T ℃时,该反应的平衡常数为___________ ;
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol/min)与催化剂的对应关系如表所示。
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是 ___________ (填化学式)。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如下:
| 反应 | 大气固氮 N2(g)+O2(g)  2NO(g) 2NO(g) | 工业固氮 N2(g)+3H2(g)  2NH3(g) 2NH3(g) | ||||
| 温度/℃ | 25 | 2 000 | 25 | 350 | 400 | 450 |
| 平衡常数K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.504 | 0.152 |
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g)反应制备NH3(l)的热化学方程式为:

(3)T ℃时,在2 L恒容密闭容器中加入1.2 mol N2和2 mol H2模拟一定条件下工业固氮[N2(g)+3H2(g)
 2NH3(g)],体系中n(NH3)随时间的变化如图所示:
2NH3(g)],体系中n(NH3)随时间的变化如图所示:
①前2分钟内的平均反应速率v(NH3)=
②有关工业固氮的说法正确的是
A.使用催化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500 ℃左右有利于反应向正方向进行
D.增大压强有利于加快反应速率,所以压强越大越好
③T ℃时,该反应的平衡常数为
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol/min)与催化剂的对应关系如表所示。
| 催化剂 | Fe | Pd | Ru | Rh | Pt | Ni |
| 初始速率 | 0.5 | 1.8 | 7.9 | 4.0 | 2.2 | 3.0 |
您最近半年使用:0次
名校
2 . 乙醇用途广泛且需求量大,寻求制备乙醇的新方法是研究的热点。
(1) 电催化制备乙醇。电解原理示意图如图1所示。
电催化制备乙醇。电解原理示意图如图1所示。
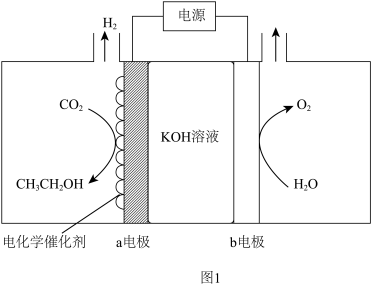
①a电极的电极反应式为_______ 。
②有效抑制a电极发生析氢反应的措施有_______ 。
(2) 催化加氢制备乙醇。
催化加氢制备乙醇。 在催化剂
在催化剂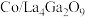 表面加氢制备乙醇的反应为
表面加氢制备乙醇的反应为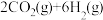

 ,反应机理如图2所示。
,反应机理如图2所示。
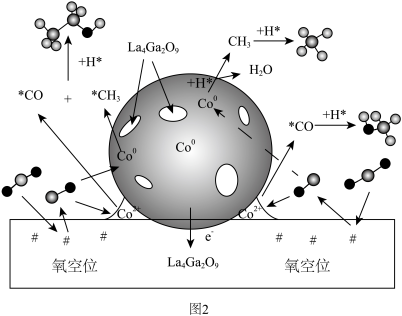
① 在
在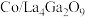 催化剂表面加氢生成
催化剂表面加氢生成 的过程可描述为
的过程可描述为_______ 。
②制取 的过程中可获得的副产物有
的过程中可获得的副产物有_______ 。
③随着反应进行,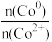 的值
的值_______ (填“增大”、“减小”或“不变”)。
④将 的混合气体置于密闭容器中,在
的混合气体置于密闭容器中,在 和不同温度下反应达到平衡时,
和不同温度下反应达到平衡时, 的转化率和
的转化率和 的选择性[
的选择性[ 的选择性
的选择性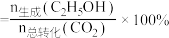 ]如图3所示。温度在时
]如图3所示。温度在时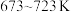 ,CO2的平衡转化率几乎不变,其原因可能为
,CO2的平衡转化率几乎不变,其原因可能为_______ 。
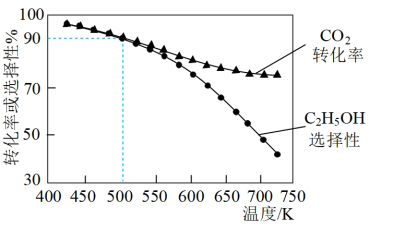
图3
(1)
 电催化制备乙醇。电解原理示意图如图1所示。
电催化制备乙醇。电解原理示意图如图1所示。
①a电极的电极反应式为
②有效抑制a电极发生析氢反应的措施有
(2)
 催化加氢制备乙醇。
催化加氢制备乙醇。 在催化剂
在催化剂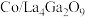 表面加氢制备乙醇的反应为
表面加氢制备乙醇的反应为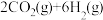

 ,反应机理如图2所示。
,反应机理如图2所示。
①
 在
在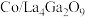 催化剂表面加氢生成
催化剂表面加氢生成 的过程可描述为
的过程可描述为②制取
 的过程中可获得的副产物有
的过程中可获得的副产物有③随着反应进行,
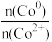 的值
的值④将
 的混合气体置于密闭容器中,在
的混合气体置于密闭容器中,在 和不同温度下反应达到平衡时,
和不同温度下反应达到平衡时, 的转化率和
的转化率和 的选择性[
的选择性[ 的选择性
的选择性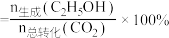 ]如图3所示。温度在时
]如图3所示。温度在时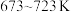 ,CO2的平衡转化率几乎不变,其原因可能为
,CO2的平衡转化率几乎不变,其原因可能为
图3
您最近半年使用:0次
2023-02-15更新
|
579次组卷
|
2卷引用:江苏省无锡市2022-2023学年高三上学期期末调研测试化学试题
解题方法
3 . 放热反应在生产、生活中用途广泛。
(1)已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则1mol甲烷不完全燃烧的热化学方程式为_______ 。
(2)甲烷可以消除氮氧化物污染,发生的反应为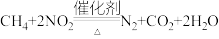 ,在体积固定的密闭容器中,每次实验均加入
,在体积固定的密闭容器中,每次实验均加入 和
和 ,使
,使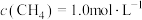 、
、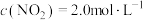 ,在不同条件下进行反应,测得
,在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:
①实验1中,在10~20min内,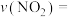
_______ ,40min时v(正)_______ v(逆)(填:“大于”、“小于”、“等于”)。
②0~20min内,实验2比实验1反应速率快的原因可能是_______ 。
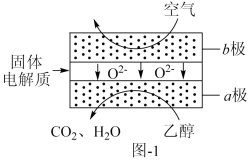
(3)乙醇应用于燃料电池,该电池采用可传导 的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为_______ 。
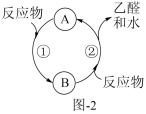
(4)乙醇在Cu作催化剂时与氧气反应的关系如图2,反应②的化学方程式:_______ 。
(5)硝酸铵在高温或猛烈撞击时易爆炸,放出大量的热。 高温分解不可能生成
高温分解不可能生成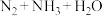 。理由是
。理由是_______ 。
(1)已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则1mol甲烷不完全燃烧的热化学方程式为
(2)甲烷可以消除氮氧化物污染,发生的反应为
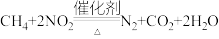 ,在体积固定的密闭容器中,每次实验均加入
,在体积固定的密闭容器中,每次实验均加入 和
和 ,使
,使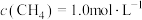 、
、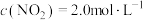 ,在不同条件下进行反应,测得
,在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:| 实验 序号 | 时间/min 浓度  温度/℃ | 10 | 20 | 30 | 40 | 50 |
| 1 | 800 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
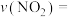
②0~20min内,实验2比实验1反应速率快的原因可能是
(3)乙醇应用于燃料电池,该电池采用可传导
 的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
(4)乙醇在Cu作催化剂时与氧气反应的关系如图2,反应②的化学方程式:

(5)硝酸铵在高温或猛烈撞击时易爆炸,放出大量的热。
 高温分解不可能生成
高温分解不可能生成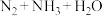 。理由是
。理由是
您最近半年使用:0次
4 . 请阅读下列材料,完成下面小题。
硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸的关键一步是将SO2氧化为SO3,该反应为2SO2+O2 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
1. SO2与O2在一定条件下反应生成SO3,该反应属于( )
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
2. 上述材料中的反应是氧化还原反应,下列有关该反应的说法正确的是( )
A. O2是还原剂 B. SO2被氧化
C. O2失去电子 D. SO2发生还原反应
3. 上述材料中的反应在密闭容器中进行,下列关于该反应的说法正确的是( )
A. 升高温度能减慢反应速率
B. SO2与O2能100%转化为SO3
C. 减小O2的浓度能加快反应速率
D. 使用恰当的催化剂能加快反应速率
4. 上述材料中的反应为放热反应,下列说法正确的是( )
A. 断开化学键放出能量
B. 放热反应都不需要加热
C. 该反应的逆反应是吸热反应
D. 该反应的反应物总能量小于生成物的总能量
硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸的关键一步是将SO2氧化为SO3,该反应为2SO2+O2
 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。1. SO2与O2在一定条件下反应生成SO3,该反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
2. 上述材料中的反应是氧化还原反应,下列有关该反应的说法正确的是
A. O2是还原剂 B. SO2被氧化
C. O2失去电子 D. SO2发生还原反应
3. 上述材料中的反应在密闭容器中进行,下列关于该反应的说法正确的是
A. 升高温度能减慢反应速率
B. SO2与O2能100%转化为SO3
C. 减小O2的浓度能加快反应速率
D. 使用恰当的催化剂能加快反应速率
4. 上述材料中的反应为放热反应,下列说法正确的是
A. 断开化学键放出能量
B. 放热反应都不需要加热
C. 该反应的逆反应是吸热反应
D. 该反应的反应物总能量小于生成物的总能量
您最近半年使用:0次



