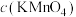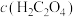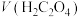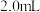名校
1 . 某小组同学探究Cu和H2O2的反应。
[猜想预测]
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
[实验探究]
实验i:向装有0.5gCu的烧杯中加入20mL30%H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:____ 。
[继续探究]
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2++4NH3 [Cu(NH3)4]2+,[Cu(NH3)4]2+为深蓝色;
[Cu(NH3)4]2+,[Cu(NH3)4]2+为深蓝色;
Cu(OH)2可溶于氨水形成深蓝色溶液。
(2)实验ii中:溶液变蓝的原因是____ (用化学用语解释);经检验产生的气体为氧气,产生氧气的原因是____ 。
(3)对比实验i和iii,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。
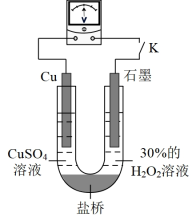
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:____ 。
利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)实验iii有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因可能是____ 。
(5)基于以上实验,影响Cu与H2O2反应速率的因素有____ 和____ 。
[猜想预测]
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
[实验探究]
实验i:向装有0.5gCu的烧杯中加入20mL30%H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:
[继续探究]
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2++4NH3
 [Cu(NH3)4]2+,[Cu(NH3)4]2+为深蓝色;
[Cu(NH3)4]2+,[Cu(NH3)4]2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
| 装置 | 序号 | 试剂a | 现象 |
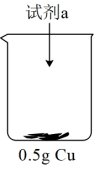 | ii | 20mL30%H2O2与4mL5mol/LH2SO4混合液 | Cu表面很快产生少量气泡,溶液逐渐变蓝,产生较多气泡 |
| iii | 20mL30%H2O2与4mL5mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。

已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:
利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)实验iii有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因可能是
(5)基于以上实验,影响Cu与H2O2反应速率的因素有
您最近半年使用:0次
名校
解题方法
2 . 某小组探究 和
和 的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
【实验探究】
实验i:向装有0.5g 的烧杯中加入20mL30%
的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊, 片表面附着少量蓝色固体。
片表面附着少量蓝色固体。
(1)写出该反应的化学方程式:_______ 。
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验ii中:溶液变蓝的原因是_______ (用离子反应方程式表示);经检验产生的气体为氧气,产生氧气的原因是_______ 。
(3)对比实验i和iii,为探究氨水对 的还原性或
的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
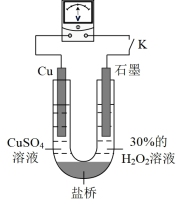
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:_______ 。
②利用该方法也可证明酸性增强可提高 的氧化性,与上述实验操作不同的是
的氧化性,与上述实验操作不同的是_______ 。
(4)总结:物质氧化性和还原性变化的一般规律是_______ 。
(5)应用: 分别与
分别与 的盐酸、氢溴酸、氢碘酸混合,
的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
只与氢碘酸发生置换反应,试解释原因_______ 。
 和
和 的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。【实验探究】
实验i:向装有0.5g
 的烧杯中加入20mL30%
的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊, 片表面附着少量蓝色固体。
片表面附着少量蓝色固体。(1)写出该反应的化学方程式:
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
| 装置 | 序号 | 试剂a | 现象 |
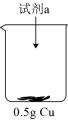 | ii | 20mL30% 与4mL 与4mL5mol/L  混合液 混合液 |  表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| iii | 20mL30% 与4mL 与4mL5mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡, 表面有少量蓝色不溶物 表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究氨水对
 的还原性或
的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:
②利用该方法也可证明酸性增强可提高
 的氧化性,与上述实验操作不同的是
的氧化性,与上述实验操作不同的是(4)总结:物质氧化性和还原性变化的一般规律是
(5)应用:
 分别与
分别与 的盐酸、氢溴酸、氢碘酸混合,
的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
只与氢碘酸发生置换反应,试解释原因
您最近半年使用:0次
2022-06-03更新
|
527次组卷
|
4卷引用:北京市和平街第一中学2021-2022学年高三下学期保温化学试题
北京市和平街第一中学2021-2022学年高三下学期保温化学试题(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题(已下线)微专题 物质性质综合实验探究北京市东直门中学2023-2024学年高三上学期12月阶段测试化学试题
3 . 某小组同学探究Cu和H2O2的反应,进行如下实验。
实验ⅰ:向装有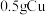 的烧杯中加入
的烧杯中加入 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)蓝色固体是_______ (填化学式)。
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料: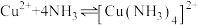 (深蓝色)
(深蓝色)
(2)实验中ⅱ:溶液变蓝的原因是_______ (用化学用语解释)。
(3)实验ⅲ中:
①深蓝色溶液含有 ,其中提供空轨道的微粒是
,其中提供空轨道的微粒是_______ ,提供孤电子对的原子是_______ 。
②对比实验ⅰ和ⅲ,为探究氨水对 的还原性或
的还原性或 氧化性的影响,利用下图装置继续实验。
氧化性的影响,利用下图装置继续实验。
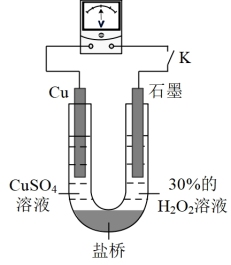
已知:电压大小反映了物质氧化性与还原性强弱的差异;差异越大,电压越大
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论是_______ ,结合化学用语解释c中电压增大的原因_______ 。利用该方法也可证明酸性增强可提高 的氧化性,导致
的氧化性,导致 溶解速率加快。
溶解速率加快。
(4)对比实验ii和iii,实验iii中产生氧气速率明显更快,可能的原因是_______ 。
(5)基于以上实验,影响Cu与 反应速率的因素有
反应速率的因素有_______ 。
实验ⅰ:向装有
 的烧杯中加入
的烧杯中加入 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。(1)蓝色固体是
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:
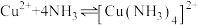 (深蓝色)
(深蓝色)| 装置 | 序号 | 试剂a | 现象 |
 | ⅱ |  与 与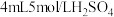 混合液 混合液 |  表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| ⅲ |  与 与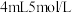 氨水混合液 氨水混合液 | 溶液立即变为深蓝色,产生大量气泡, 表面有少量蓝色不溶物 表面有少量蓝色不溶物 |
(3)实验ⅲ中:
①深蓝色溶液含有
 ,其中提供空轨道的微粒是
,其中提供空轨道的微粒是②对比实验ⅰ和ⅲ,为探究氨水对
 的还原性或
的还原性或 氧化性的影响,利用下图装置继续实验。
氧化性的影响,利用下图装置继续实验。
已知:电压大小反映了物质氧化性与还原性强弱的差异;差异越大,电压越大
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论是
 的氧化性,导致
的氧化性,导致 溶解速率加快。
溶解速率加快。(4)对比实验ii和iii,实验iii中产生氧气速率明显更快,可能的原因是
(5)基于以上实验,影响Cu与
 反应速率的因素有
反应速率的因素有
您最近半年使用:0次
名校
解题方法
4 . 草酸(H2C2O4)用途广泛,是一种易溶于水的二元有机弱酸,具有还原性,为探究草酸被氧化的速率问题,高二化学小组进行如下实验:
Ⅰ.探究H2C2O4与KMnO4溶液反应
(1)在酸性条件下反应,写出H2C2O4与KMnO4溶液反应的离子方程式:___________
(2)为探究外界条件对反应速率的影响,阳阳进行了如下实验:
对比实验___________ (填实验编号),可探究草酸浓度对反应速率的影响;实验测得t3< t2,由此得出的结论是____________
Ⅱ.探究H2C2O4与 溶液反应
溶液反应
查阅资料:H2C2O4与 溶液反应很慢,需数月时间才能完成,但加入
溶液反应很慢,需数月时间才能完成,但加入 可促进H2C2O4与
可促进H2C2O4与 的反应。依据此资料,阳阳设计如下实验证实了这一点。
的反应。依据此资料,阳阳设计如下实验证实了这一点。
(3)实验Ⅳ的目的是:___________ 。
(4)对实验Ⅱ继续进行探究,发现溶液中 浓度变化如图:
浓度变化如图:
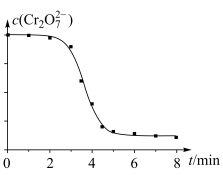
小宇认为此变化是通过两个过程实现的。
过程ⅰ: 与H2C2O4反应生成了
与H2C2O4反应生成了 。
。
过程ⅱ: 可加快草酸与重铬酸钾的反应
可加快草酸与重铬酸钾的反应
①查阅资料:溶液中 能被
能被 氧化为
氧化为 。针对过程ⅰ,小宇设计如下方法证实:
。针对过程ⅰ,小宇设计如下方法证实:
将 加入到
加入到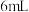
___________ 中,固体完全溶解;从中取出少量溶液,加入过量 固体,充分反应后静置,观察到
固体,充分反应后静置,观察到___________ 。
②小宇继续设计实验方案证实了过程ⅱ成立,他的实验方案如下:将2mL0.3moL/L H2C2O4溶液与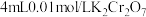 溶液混合,调至pH=2,加入
溶液混合,调至pH=2,加入 固体,6分钟后现象为:
固体,6分钟后现象为:___________ 。综合以上实验可知,草酸发生氧化反应的速率与___________ 有关。
Ⅰ.探究H2C2O4与KMnO4溶液反应
(1)在酸性条件下反应,写出H2C2O4与KMnO4溶液反应的离子方程式:
(2)为探究外界条件对反应速率的影响,阳阳进行了如下实验:
| 实验编号 | 所加试剂及用量/mL | 条件 | 溶液颜色褪至无色所需时间/min | |||
| 0.01mol/L H2C2O4溶液 | 0.01mol/L KMnO4溶液 | 3.0mol/L稀硫酸 | 水 | 温度/℃ | ||
| 1 | 8.0 | 2.0 | 2.0 | 3.0 | 20 | t1 |
| 2 | 6.0 | 2.0 | 2.0 | 5.0 | 20 | t2 |
| 3 | 6.0 | 2.0 | 2.0 | 5.0 | 30 | t3 |
| 4 | 5.0 | 2.0 | 2.0 | 5.0 | 30 | t4 |
Ⅱ.探究H2C2O4与
 溶液反应
溶液反应查阅资料:H2C2O4与
 溶液反应很慢,需数月时间才能完成,但加入
溶液反应很慢,需数月时间才能完成,但加入 可促进H2C2O4与
可促进H2C2O4与 的反应。依据此资料,阳阳设计如下实验证实了这一点。
的反应。依据此资料,阳阳设计如下实验证实了这一点。| 实验Ⅱ | 实验Ⅲ | 实验Ⅳ | |
| 实验操作 | 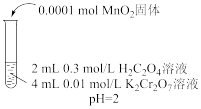 |  | 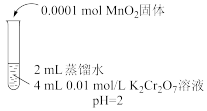 |
| 实验现象 | 6min后固体完全溶解,溶液橙色变浅,温度不变 | 6min后固体未溶解,溶液颜色无明显变化 | 6min后固体未溶解,溶液颜色无明显变化 |
(4)对实验Ⅱ继续进行探究,发现溶液中
 浓度变化如图:
浓度变化如图:
小宇认为此变化是通过两个过程实现的。
过程ⅰ:
 与H2C2O4反应生成了
与H2C2O4反应生成了 。
。过程ⅱ:
 可加快草酸与重铬酸钾的反应
可加快草酸与重铬酸钾的反应①查阅资料:溶液中
 能被
能被 氧化为
氧化为 。针对过程ⅰ,小宇设计如下方法证实:
。针对过程ⅰ,小宇设计如下方法证实:将
 加入到
加入到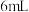
 固体,充分反应后静置,观察到
固体,充分反应后静置,观察到②小宇继续设计实验方案证实了过程ⅱ成立,他的实验方案如下:将2mL0.3moL/L H2C2O4溶液与
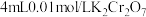 溶液混合,调至pH=2,加入
溶液混合,调至pH=2,加入 固体,6分钟后现象为:
固体,6分钟后现象为:
您最近半年使用:0次
2021-11-20更新
|
504次组卷
|
2卷引用:安徽省合肥市第六中学2021-2022学年高二上学期期中教学检测化学试题
名校
5 . 铁元素的“价—类”二维图如图所示:
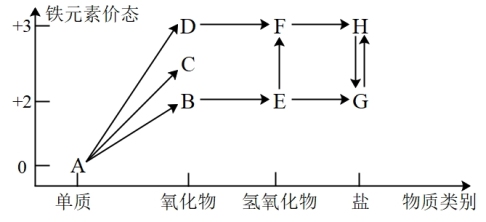
(1)C的化学式是_______ , 反应的化学方程式是
反应的化学方程式是_______ ,反应过程的现象为_______ 。
(2)维生素C可将H转化为G,维生素C具有_______ (填“酸性”、“氧化性”或“还原性”)。
(3)在指定条件下,下列铁及其化合物之间的转化不能实现的是_______ 。
A. B.
B.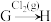 C.
C.
(4)某小组同学设计如下实验,研究亚铁盐与 溶液的反应。
溶液的反应。
试剂:酸化的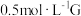 溶液,
溶液,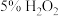 溶液
溶液
①上述实验中 溶液与G溶液反应的离子方程式是
溶液与G溶液反应的离子方程式是_______ 。
②产生气泡的原因是_______ 。

(1)C的化学式是
 反应的化学方程式是
反应的化学方程式是(2)维生素C可将H转化为G,维生素C具有
(3)在指定条件下,下列铁及其化合物之间的转化不能实现的是
A.
 B.
B.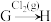 C.
C.
(4)某小组同学设计如下实验,研究亚铁盐与
 溶液的反应。
溶液的反应。试剂:酸化的
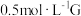 溶液,
溶液,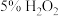 溶液
溶液| 操作 | 现象 |
取 酸化的G溶液于试管中,加入5滴 酸化的G溶液于试管中,加入5滴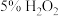 溶液 溶液 | 溶液立即变为棕黄色,稍后,产生气泡。 |
向反应后的溶液中加入 溶液 溶液 | 溶液变红 |
 溶液与G溶液反应的离子方程式是
溶液与G溶液反应的离子方程式是②产生气泡的原因是
您最近半年使用:0次
2022-01-23更新
|
798次组卷
|
8卷引用:安徽省安庆市2021-2022学年高一上学期期末考试化学试题
名校
6 . Ⅰ.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
(1)催化剂能增大化学反应速率的原因是___________ 。
(2)实验①和②的目的是探究___________ 对反应速率的影响。实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是___________ 。
(3)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图。
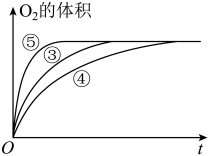
分析下图能够得出的实验结论:
①___________ 环境能增大H2O2分解的速率;
②___________ 环境能减小H2O2分解的速率。
(4)设计实验进一步探究Fe3+和Cu2+对H2O2分解的催化效果:在两支试管中各加入2mL5%的H2O2溶液,再向其中分别滴入1mL浓度均为0.1mol/L的FeCl3溶液和CuSO4溶液。有同学建议将CuSO4改为CuCl2溶液,理由是___________ ;还有同学认为即使改用了CuCl2溶液,仍不严谨,建议补做对比实验:向2mL5%的H2O2溶液中滴入的试剂及其用量是___________ 。
Ⅱ.为进一步研究浓度对反应速率的影响,该实验小组又涉及了如下实验方案:混合试剂1和试剂2,记录溶液褪色所需的时间。
(5)写出上述反应的离子方程式:___________ 。
(6)实验1中tmin时溶液褪色,用草酸表示的反应速率v(H2C2O4)=___________ mol·L-1·min-1。联系实验1、2,预期结论是___________ 。
(7)n(CO2)随时间的变化如下图1所示,其变化的原因是___________ 。
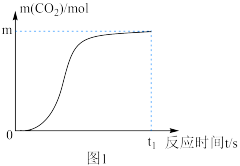
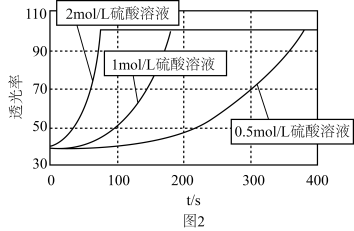
(8)研究发现KMnO4溶液的酸化程度对反应的速率也有较大影响,用不同浓度的硫酸进行酸化,其余条件均相同时,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图2所示,由此得出的结论是___________ 。
| 分组实验 | 催化剂 | |
| ① | 10mL5%H2O2溶液 | 无 |
| ② | 10mL2%H2O2溶液 | 无 |
| ③ | 10mL5%H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5%H2O2溶液+少量稀盐酸 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5%H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(2)实验①和②的目的是探究
(3)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图。

分析下图能够得出的实验结论:
①
②
(4)设计实验进一步探究Fe3+和Cu2+对H2O2分解的催化效果:在两支试管中各加入2mL5%的H2O2溶液,再向其中分别滴入1mL浓度均为0.1mol/L的FeCl3溶液和CuSO4溶液。有同学建议将CuSO4改为CuCl2溶液,理由是
Ⅱ.为进一步研究浓度对反应速率的影响,该实验小组又涉及了如下实验方案:混合试剂1和试剂2,记录溶液褪色所需的时间。
| 实验1 | 实验2 | |
| 试剂1 | 2mL0.1mol/L的草酸溶液 | 2mL0.2mol/L的草酸溶液 |
| 试剂2 | 4mL0.01mol/L的高锰酸钾酸性溶液 | 4mL0.01mol/L的高锰酸钾酸性溶液 |
(6)实验1中tmin时溶液褪色,用草酸表示的反应速率v(H2C2O4)=
(7)n(CO2)随时间的变化如下图1所示,其变化的原因是

(8)研究发现KMnO4溶液的酸化程度对反应的速率也有较大影响,用不同浓度的硫酸进行酸化,其余条件均相同时,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图2所示,由此得出的结论是

您最近半年使用:0次
名校
解题方法
7 . H2O2广泛应用于医疗卫生、化学合成等领域。
(1)已知2H2O2(l)=2H2O(l)+O2(g) △H=-196kJ•mol-1,趣味实验“大象牙膏”的实验原理是H2O2溶液在KI催化作用下分解,反应的机理可表示为:
i.H2O2(l)+I-(aq)=H2O(l)+IO-(aq) △H1=+akJ•mol-1(a>0)
ii.H2O2(l)+__________。
则ii中反应机理用热化学方程式表示为________ 。
(2)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如表方案完成实验。
I.实验①和②的目的是_______ 。实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2较稳定,不易分解,为达到实验目的,你对原方案的改进是_______ 。
II.实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图,结合图分析实验,能够得出什么实验结论?________ 。
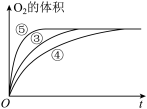
III.为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验。

①写出H2O2在FeCl3作用下发生反应的化学方程式:________ 。
②利用图1实验,可通过观察产生气泡的快慢定性比较得出结论·有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______ 。
③若利用图2实验可进行定量分析,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是_______ 。
(1)已知2H2O2(l)=2H2O(l)+O2(g) △H=-196kJ•mol-1,趣味实验“大象牙膏”的实验原理是H2O2溶液在KI催化作用下分解,反应的机理可表示为:
i.H2O2(l)+I-(aq)=H2O(l)+IO-(aq) △H1=+akJ•mol-1(a>0)
ii.H2O2(l)+__________。
则ii中反应机理用热化学方程式表示为
(2)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如表方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2%H2O2溶液 | 无 |
| ② | 10mL5%H2O2溶液 | 无 |
| ③ | 10mL5%H2O2溶液 | 1mL0.1mol/LFeCl3溶液 |
| ④ | 10mL5%H2O2溶液+少量HCl溶液 | 1mL0.1mol/LFeCl3溶液 |
| ⑤ | 10mL5%H2O2溶液+少量NaOH溶液 | 1mL0.1mol/LFeCl3溶液 |
II.实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图,结合图分析实验,能够得出什么实验结论?

III.为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验。

①写出H2O2在FeCl3作用下发生反应的化学方程式:
②利用图1实验,可通过观察产生气泡的快慢定性比较得出结论·有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
③若利用图2实验可进行定量分析,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
您最近半年使用:0次
名校
解题方法
8 . 某兴趣小组同学将 的酸性
的酸性 溶液和
溶液和 溶液按如下比例混合,探究浓度对反应速率的影响。
溶液按如下比例混合,探究浓度对反应速率的影响。
现象:实验①溶液很快由紫色变为青绿色,而实验②慢一点;变为青绿色后,实验②溶液很快褪至无色,而实验①褪色慢一点。
资料: 与
与 很难形成配合物;
很难形成配合物;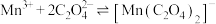 (青绿色),
(青绿色), 有强氧化性,而
有强氧化性,而 氧化性极弱。
氧化性极弱。
下列说法错误的是
 的酸性
的酸性 溶液和
溶液和 溶液按如下比例混合,探究浓度对反应速率的影响。
溶液按如下比例混合,探究浓度对反应速率的影响。序号 | 温度 |
|
|
|
|
|
① | 20℃ |
|
|
|
|
|
② | 20℃ |
|
|
|
|
|
资料:
 与
与 很难形成配合物;
很难形成配合物;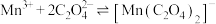 (青绿色),
(青绿色), 有强氧化性,而
有强氧化性,而 氧化性极弱。
氧化性极弱。下列说法错误的是
A. |
B. 溶液中能通过加盐酸酸化调 溶液中能通过加盐酸酸化调 |
C.溶液由青绿色褪至无色过程中,实验①中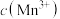 较小,导致褪色速率较慢 较小,导致褪色速率较慢 |
D.由实验可知,加入 越多, 越多, 溶液由紫色褪至无色的速率越快 溶液由紫色褪至无色的速率越快 |
您最近半年使用:0次
2023-06-02更新
|
228次组卷
|
2卷引用:河北省2022-2023学年高三下学期1月大联考化学试题
9 . 氧化剂H2O2在反应时不产生污染物被称为“绿色氧化剂”,因而受到人们越来越多的关注。
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
(1)实验①和②的目的是___________ 。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是__________ (填一种方法即可)。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图1所示。分析该图能够得出的实验结论是_______________ 。
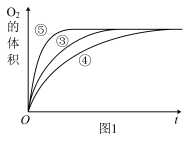
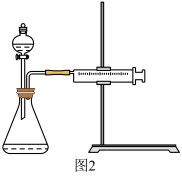
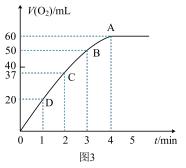
Ⅱ.资料显示,某些金属离子或金属氧化物对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如图2所示的实验装置进行实验。
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量_________ 或________ 来比较。
(2)0.1 g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示。请解释化学反应速率变化的原因:_______ 。请计算H2O2的初始物质的量浓度为__________ (保留两位有效数字)。为探究MnO2在此实验中对H2O2的分解起催化作用,需补做下列实验(无需写出具体操作):a._______ ;b._______ 。
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2% H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 10mL 5% H2O2溶液 | 1mL 0.1mol/LFeCl3溶液 |
| ④ | 10mL 5% H2O2溶液+少量HCl溶液 | 1mL 0.1mol/LFeCl3溶液 |
| ⑤ | 10mL 5% H2O2溶液+少量NaOH溶液 | 1mL 0.1mol/LFeCl3溶液 |
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图1所示。分析该图能够得出的实验结论是


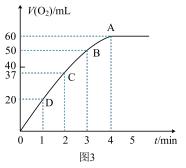
Ⅱ.资料显示,某些金属离子或金属氧化物对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如图2所示的实验装置进行实验。
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量
(2)0.1 g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示。请解释化学反应速率变化的原因:
您最近半年使用:0次
名校
解题方法
10 . 生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关四环素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应)
相关资料
①氰化物主要以CN-和[Fe(CN)6]3-两种形式存在
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂,Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计。
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH值越大,越稳定,越难被氧化。
实验过程
(1)请完成以下实验设计表(表中不要留空格)
实验测得含氰废水中的总氰浓度(以CN-表示)随时间变化关系如图所示。
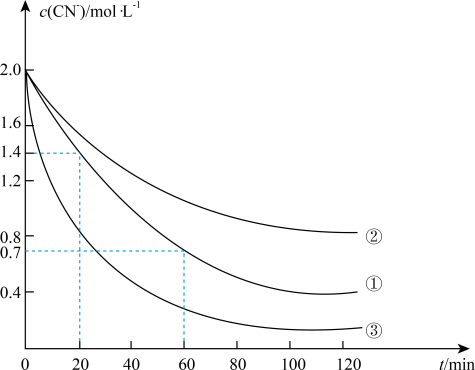
(2)实验①中20~60min时间段反应速率:υ(CN-)=___ mol•L-1•min-1。
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是__ (填一点即可),在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO3-,同时放出NH3,试写出该反应的离子方程式___ 。
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实验并验证上述结论,完成表2中内容。(已知:废水中的CN-浓度可用离子色谱仪测定)___
相关资料
①氰化物主要以CN-和[Fe(CN)6]3-两种形式存在
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂,Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计。
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH值越大,越稳定,越难被氧化。
实验过程
(1)请完成以下实验设计表(表中不要留空格)
| 实验 序号 | 实验目的 | 初始pH | 废水样品体积/mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积/mL |
| 1 | 为以下实验操作参考 | 7 | 60 | 10 | 10 | 20 |
| 2 | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
| 3 | 7 | 60 | 10 |

(2)实验①中20~60min时间段反应速率:υ(CN-)=
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实验并验证上述结论,完成表2中内容。(已知:废水中的CN-浓度可用离子色谱仪测定)
| 实验步骤(不要写出具体操作过程) | 预期实验现象和结论 |
您最近半年使用:0次