15. 六氨合氯化镁(MgCl
2•6NH
3)具有极好的可逆吸、放氨特性,是一种优良的储氨材料。某研究小组以MgCl
2•6H
2O为原料在实验室制备MgCl
2•6NH
3,并测定所得产品中氯的含量
(一)制备MgCl
2•6NH
3I.首先制备无水MgCl
2实验装置如下图(加热及夹持装置略去):

已知:SOCl
2:熔点

105℃、沸点76℃;遇水剧烈水解生成两种酸性气体。
(1)滴液漏斗中支管的作用为
___________。
(2)三颈瓶中发生反应的化学方程式为
___________。
(3)该实验装置中的不足之处为
___________。
II.将NH
3通入无水MgCl
2的乙二醇溶液中,充分反应(
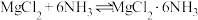
)后,过滤、洗涤并自然风干,制得粗品。相关物质的性质如表:

| NH3 | MgCl2 | MgCl2•NH3 |
| 水 | 易溶 | 易溶 | 易溶 |
| 甲醇(沸点65℃) | 易溶 | 易溶 | 难溶 |
| 乙二醇(沸点197℃) | 易溶 | 易溶 | 难溶 |
(4)生成MgCl
2•6NH
3的反应需在冰水浴中进行,其可能原因有___________(填字母)。
| A.反应吸热,促进反应正向进行 | B.加快反应速率 |
| C.防止氨气挥发,提高氨气利用率 | D.降低产物的溶解度 |
(5)洗涤产品时,应选择的洗涤剂为___________(填字母)。
| A.冰浓氨水 | B.乙二醇和水的混合液 |
| C.氨气饱和的甲醇溶液 | D.氨气饱和的乙二醇溶液 |
(二)测定产品中氯的含量,步骤如下:
步骤1:称取1.80g样品,加入足量稀硝酸溶解,配成250mL溶液;
步骤2:取25.00mL待测液于锥形瓶中,以K
2CrO
4为指示剂,用0.20

的AgNO
3标准液滴定溶液中

,记录消耗标准液的体积;
步骤3:重复步骤2操作2~3次,平均消耗标准液10.00 mL。
(6)步骒1中,用稀硝酸溶解样品的目的为
___________。
(7)该品中氯的质量分数为
___________(保留小数点后2位);该实验值与理论值(36.04%)有偏差,造成该偏差的可能原因是(已知滴定操作均正确)
___________。