名校
1 . 氯、氮、硫等及其化合物性质研究。如图是氮、硫元素的各种价态与物质类别的对应关系:

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的化学方程式为____ 。
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,写出化学方程式____ 。
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl b.NO+NO2+H2O 2HNO2 c.HClO+HNO2=HNO3+HCl
2HNO2 c.HClO+HNO2=HNO3+HCl
下列分析正确的是___ 。
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:
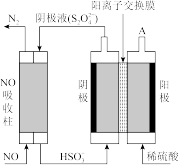
从A口中出来的物质的是____ 。写出电解池阴极的电极反应式____ 。
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
①上述实验中a=____ ,b=____ 。
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是____ (填实验编号)。

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的化学方程式为
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,写出化学方程式
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl b.NO+NO2+H2O
 2HNO2 c.HClO+HNO2=HNO3+HCl
2HNO2 c.HClO+HNO2=HNO3+HCl下列分析正确的是
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:

从A口中出来的物质的是
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO
 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | b | 124 |
| III | 350 | a | 5.80×10-3 | 82 |
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是
您最近一年使用:0次
解题方法
2 . 放热反应在生产、生活中用途广泛。
(1)已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则1mol甲烷不完全燃烧的热化学方程式为_______ 。
(2)甲烷可以消除氮氧化物污染,发生的反应为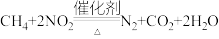 ,在体积固定的密闭容器中,每次实验均加入
,在体积固定的密闭容器中,每次实验均加入 和
和 ,使
,使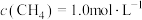 、
、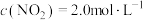 ,在不同条件下进行反应,测得
,在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:
①实验1中,在10~20min内,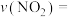
_______ ,40min时v(正)_______ v(逆)(填:“大于”、“小于”、“等于”)。
②0~20min内,实验2比实验1反应速率快的原因可能是_______ 。
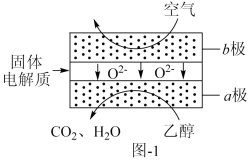
(3)乙醇应用于燃料电池,该电池采用可传导 的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为_______ 。
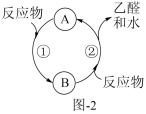
(4)乙醇在Cu作催化剂时与氧气反应的关系如图2,反应②的化学方程式:_______ 。
(5)硝酸铵在高温或猛烈撞击时易爆炸,放出大量的热。 高温分解不可能生成
高温分解不可能生成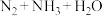 。理由是
。理由是_______ 。
(1)已知25℃、101kPa时,1g甲烷不完全燃烧生成CO和液态水时放出37.96kJ热量,则1mol甲烷不完全燃烧的热化学方程式为
(2)甲烷可以消除氮氧化物污染,发生的反应为
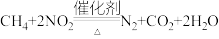 ,在体积固定的密闭容器中,每次实验均加入
,在体积固定的密闭容器中,每次实验均加入 和
和 ,使
,使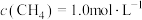 、
、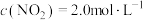 ,在不同条件下进行反应,测得
,在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:| 实验 序号 | 时间/min 浓度  温度/℃ | 10 | 20 | 30 | 40 | 50 |
| 1 | 800 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
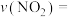
②0~20min内,实验2比实验1反应速率快的原因可能是
(3)乙醇应用于燃料电池,该电池采用可传导
 的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
(4)乙醇在Cu作催化剂时与氧气反应的关系如图2,反应②的化学方程式:

(5)硝酸铵在高温或猛烈撞击时易爆炸,放出大量的热。
 高温分解不可能生成
高温分解不可能生成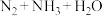 。理由是
。理由是
您最近一年使用:0次
名校
解题方法
3 . 草酸(H2C2O4)用途广泛,是一种易溶于水的二元有机弱酸,具有还原性,为探究草酸被氧化的速率问题,高二化学小组进行如下实验:
Ⅰ.探究H2C2O4与KMnO4溶液反应
(1)在酸性条件下反应,写出H2C2O4与KMnO4溶液反应的离子方程式:___________
(2)为探究外界条件对反应速率的影响,阳阳进行了如下实验:
对比实验___________ (填实验编号),可探究草酸浓度对反应速率的影响;实验测得t3< t2,由此得出的结论是____________
Ⅱ.探究H2C2O4与 溶液反应
溶液反应
查阅资料:H2C2O4与 溶液反应很慢,需数月时间才能完成,但加入
溶液反应很慢,需数月时间才能完成,但加入 可促进H2C2O4与
可促进H2C2O4与 的反应。依据此资料,阳阳设计如下实验证实了这一点。
的反应。依据此资料,阳阳设计如下实验证实了这一点。
(3)实验Ⅳ的目的是:___________ 。
(4)对实验Ⅱ继续进行探究,发现溶液中 浓度变化如图:
浓度变化如图:
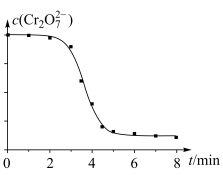
小宇认为此变化是通过两个过程实现的。
过程ⅰ: 与H2C2O4反应生成了
与H2C2O4反应生成了 。
。
过程ⅱ: 可加快草酸与重铬酸钾的反应
可加快草酸与重铬酸钾的反应
①查阅资料:溶液中 能被
能被 氧化为
氧化为 。针对过程ⅰ,小宇设计如下方法证实:
。针对过程ⅰ,小宇设计如下方法证实:
将 加入到
加入到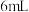
___________ 中,固体完全溶解;从中取出少量溶液,加入过量 固体,充分反应后静置,观察到
固体,充分反应后静置,观察到___________ 。
②小宇继续设计实验方案证实了过程ⅱ成立,他的实验方案如下:将2mL0.3moL/L H2C2O4溶液与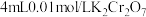 溶液混合,调至pH=2,加入
溶液混合,调至pH=2,加入 固体,6分钟后现象为:
固体,6分钟后现象为:___________ 。综合以上实验可知,草酸发生氧化反应的速率与___________ 有关。
Ⅰ.探究H2C2O4与KMnO4溶液反应
(1)在酸性条件下反应,写出H2C2O4与KMnO4溶液反应的离子方程式:
(2)为探究外界条件对反应速率的影响,阳阳进行了如下实验:
| 实验编号 | 所加试剂及用量/mL | 条件 | 溶液颜色褪至无色所需时间/min | |||
| 0.01mol/L H2C2O4溶液 | 0.01mol/L KMnO4溶液 | 3.0mol/L稀硫酸 | 水 | 温度/℃ | ||
| 1 | 8.0 | 2.0 | 2.0 | 3.0 | 20 | t1 |
| 2 | 6.0 | 2.0 | 2.0 | 5.0 | 20 | t2 |
| 3 | 6.0 | 2.0 | 2.0 | 5.0 | 30 | t3 |
| 4 | 5.0 | 2.0 | 2.0 | 5.0 | 30 | t4 |
Ⅱ.探究H2C2O4与
 溶液反应
溶液反应查阅资料:H2C2O4与
 溶液反应很慢,需数月时间才能完成,但加入
溶液反应很慢,需数月时间才能完成,但加入 可促进H2C2O4与
可促进H2C2O4与 的反应。依据此资料,阳阳设计如下实验证实了这一点。
的反应。依据此资料,阳阳设计如下实验证实了这一点。| 实验Ⅱ | 实验Ⅲ | 实验Ⅳ | |
| 实验操作 | 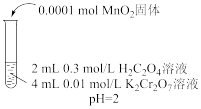 |  | 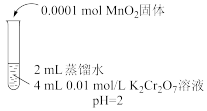 |
| 实验现象 | 6min后固体完全溶解,溶液橙色变浅,温度不变 | 6min后固体未溶解,溶液颜色无明显变化 | 6min后固体未溶解,溶液颜色无明显变化 |
(4)对实验Ⅱ继续进行探究,发现溶液中
 浓度变化如图:
浓度变化如图:
小宇认为此变化是通过两个过程实现的。
过程ⅰ:
 与H2C2O4反应生成了
与H2C2O4反应生成了 。
。过程ⅱ:
 可加快草酸与重铬酸钾的反应
可加快草酸与重铬酸钾的反应①查阅资料:溶液中
 能被
能被 氧化为
氧化为 。针对过程ⅰ,小宇设计如下方法证实:
。针对过程ⅰ,小宇设计如下方法证实:将
 加入到
加入到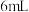
 固体,充分反应后静置,观察到
固体,充分反应后静置,观察到②小宇继续设计实验方案证实了过程ⅱ成立,他的实验方案如下:将2mL0.3moL/L H2C2O4溶液与
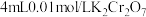 溶液混合,调至pH=2,加入
溶液混合,调至pH=2,加入 固体,6分钟后现象为:
固体,6分钟后现象为:
您最近一年使用:0次
2021-11-20更新
|
513次组卷
|
2卷引用:福建省永春华侨中学2022-2023学年高二上学期期中考试化学试题



