名校
解题方法
1 . 铱(Ir)的配合物催化氢化 得到甲酸盐的反应机理如图所示,下列说法错误的是
得到甲酸盐的反应机理如图所示,下列说法错误的是
 得到甲酸盐的反应机理如图所示,下列说法错误的是
得到甲酸盐的反应机理如图所示,下列说法错误的是
| A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
| B.反应过程中Ir的成键数目发生了变化 |
C.转化过程总反应的化学方程式为 |
| D.反应涉及极性键和非极性键的断裂与形成 |
您最近一年使用:0次
名校
解题方法
2 . 用某复合金属作电极电解催化还原 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是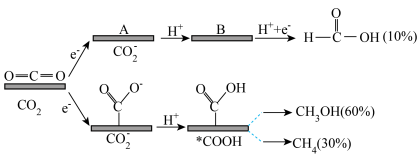
| A.过程中有极性键和非极性的断裂和形成 |
B.中间体B的结构简式为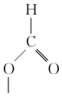 |
C. |
D.若有 完全转化,反应中转移的电子数为3.8mol 完全转化,反应中转移的电子数为3.8mol |
您最近一年使用:0次
名校
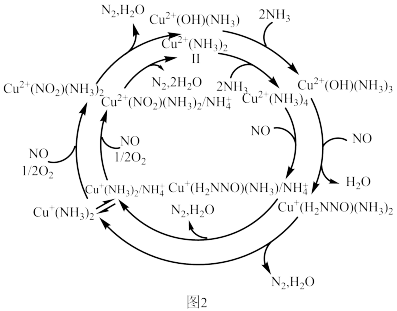
3 . 科学研究发现负载在Cu-SSZ-13分子筛表面的Cu2+有两种存在形式,其结构如图1所示,其催化NH3还原NO的机理如图2所示。下列说法错误的是
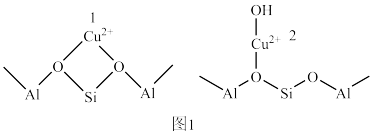
| A.图1中,1号Cu2+与O原子形成的配位键中,O提供孤电子对 |
| B.图2中,在Cu2+表面进行NH3还原NO的反应路径有2种,但可以相互转化 |
C.NH3还原NO的总化学方程式为4NH3+4N0+O2 4N2+6H2O 4N2+6H2O |
| D.该反应机理中涉及氧化还原反应,且Cu+形成配合物的配位数均相同 |
您最近一年使用:0次
名校
4 . 含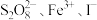 的溶液中发生反应的反应机理如图所示。下列说法正确的是
的溶液中发生反应的反应机理如图所示。下列说法正确的是
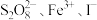 的溶液中发生反应的反应机理如图所示。下列说法正确的是
的溶液中发生反应的反应机理如图所示。下列说法正确的是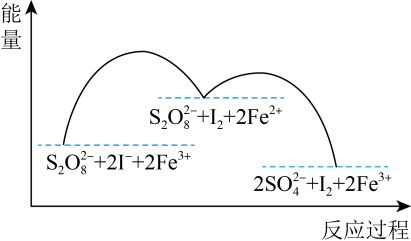
A.由图可知 不能氧化 不能氧化 |
| B.反应过程中包含三个基元反应 |
C.若不加 ,该反应的化学反应速率更大 ,该反应的化学反应速率更大 |
D. 和 和 不能大量共存 不能大量共存 |
您最近一年使用:0次
名校
5 . 一定条件下,一氧化二氮被镍配合物催化形成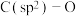 的活化机理如图所示(ii、iii、ⅳ中右上角“—”代表1个负电荷,i的右上角“0”代表不带电荷,
的活化机理如图所示(ii、iii、ⅳ中右上角“—”代表1个负电荷,i的右上角“0”代表不带电荷, 右上角“Ⅱ”代表+2价)。下列说法错误的是
右上角“Ⅱ”代表+2价)。下列说法错误的是
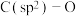 的活化机理如图所示(ii、iii、ⅳ中右上角“—”代表1个负电荷,i的右上角“0”代表不带电荷,
的活化机理如图所示(ii、iii、ⅳ中右上角“—”代表1个负电荷,i的右上角“0”代表不带电荷, 右上角“Ⅱ”代表+2价)。下列说法错误的是
右上角“Ⅱ”代表+2价)。下列说法错误的是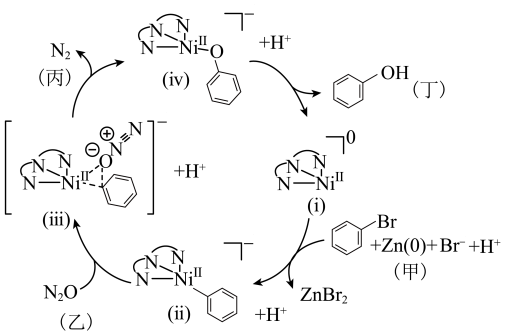
| A.ⅰ是催化剂,ⅰ、ⅱ、ⅲ是中间产物 | B.利用上述原理可实现溴苯制备苯酚 |
C. 的配合物(ⅳ)中配体只有N 的配合物(ⅳ)中配体只有N | D.ⅲ→ⅳ断裂了氮氧键和镍碳键 |
您最近一年使用:0次
6 . 烯丙醇制备丙醛的反应机理如图所示,此过程中Co的配位数不变.下列说法错误的是

A. 作催化剂 作催化剂 | B.反应过程中涉及 键的断裂与形成 键的断裂与形成 |
C.反应过程中 的化合价发生了变化 的化合价发生了变化 | D.该反应的原子利用率为 |
您最近一年使用:0次
名校
7 . 硅铝酸盐沸石离子交换分子筛M-ZSM-5(M为Fe、Co、Ni、Cu)催化N2O氧化CH4制甲醇的反应机理如图所示,下列说法错误的是
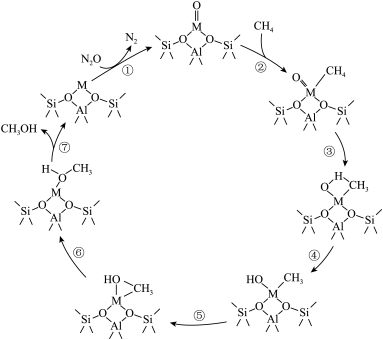
A.反应②的原子利用率为 |
B.反应①、②、③、⑥、⑦中, 的化合价发生了改变 的化合价发生了改变 |
C.M-ZSM-5能降低 氧化 氧化 制甲醇反应的活化能,改变反应的 制甲醇反应的活化能,改变反应的 |
D.总反应为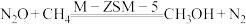 |
您最近一年使用:0次
8 . 对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。反应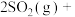
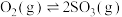
 在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
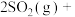
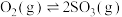
 在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是A.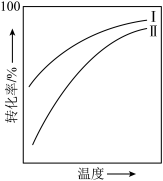 | B.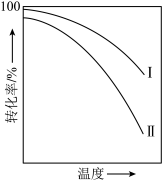 |
C.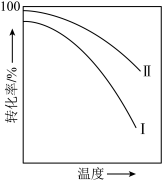 | D.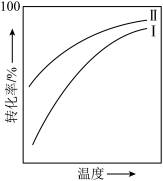 |
您最近一年使用:0次
名校
9 . 有机反应中经常采用实验和量子学手段进行反应的微观探究。一种铜催化某有机反应历程如下,下列说法错误的是

| A.碘元素位于周期表p区 |
| B.催化剂可降低该反应的活化能,加快反应速率 |
| C.Tpy-[CuⅡ]CN-是中间产物 |
D.总反应方程式是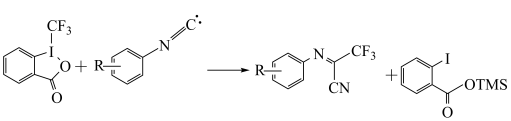 |
您最近一年使用:0次
名校
解题方法
10 . 研究表明, 催化
催化 分解的微观机制是复杂的,可以形成以下基本观点:
分解的微观机制是复杂的,可以形成以下基本观点: 与
与 循环反应;且
循环反应;且 与
与 反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
 催化
催化 分解的微观机制是复杂的,可以形成以下基本观点:
分解的微观机制是复杂的,可以形成以下基本观点: 与
与 循环反应;且
循环反应;且 与
与 反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是
反应产生的强氧化性羟基自由基(·OH)起到了关键作用,该过程被称为类-Fenton反应,如图所示,下列说法正确的是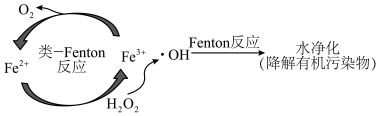
A.0.1mol羟基自由基(·OH)所含电子的数目为 |
B. 可以改变反应历程,降低 可以改变反应历程,降低 分解反应的反应热 分解反应的反应热 |
C. 与 与 反应产生羟基自由基的反应为 反应产生羟基自由基的反应为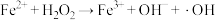 |
| D.去除废水中难降解的有机污染物,主要利用了羟基自由基的还原性 |
您最近一年使用:0次
2024-04-13更新
|
142次组卷
|
2卷引用:2024届河北省雄安新区雄安部分高中高三下学期一模化学试题



