名校
解题方法
1 . 二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害。某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示。下列判断正确的是
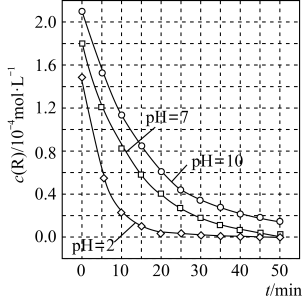

| A.在0~20min之间,pH=7时R的降解速率为0.07mol·L-1·min-1 |
| B.R的起始浓度不同,无法判断溶液的酸碱性对R的降解速率的影响 |
| C.二氧化钛对pH=2的R溶液催化效率好 |
| D.在0~50 min之间,R的降解百分率pH=2大于pH=7 |
您最近一年使用:0次
2019-03-22更新
|
1911次组卷
|
9卷引用:第二章化学反应速率与化学平衡
第二章化学反应速率与化学平衡浙江省临海市白云高级中学2019届高三3月月考化学试题黑龙江省黑河市嫩江县高级中学2019-2020学年高二下学期第一次月考化学试题(已下线)第17讲 化学平衡计算与图像-2021年高考化学一轮复习名师精讲练(已下线)【省级联考】金丽衢十二校2018学年高三第三次联考化学试题(已下线)练习5 化学反应的方向与调控-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)广东省广大附中、铁一、广外三校2020-2021学年高一下学期期中联考化学试题河北省任丘一中2021-2022学年高二上学期阶段考试(一)化学试题广东省江门市蓬江区三校2020-2021学年高一下学期期中联考化学试题
2 . 士兵在野外加热食物时通常采用“无焰食物加热器”,其主要化学成分为镁粉、铁粉、氯化钠粉末。使用时加入水与其中的镁反应放出热量。下面是在室温下对本产品的两个探究实验。
实验1:向加有等量水的三个相同隔热容器中分别加入下列各组物质,结果见图1。
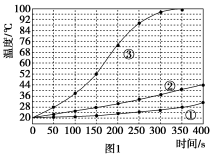
①1.0 mol镁条、0.10 mol铁粉、0.10 mol氯化钠粉末;
②将1.0 mol镁条剪成100份、0.10 mol铁粉、0.10 mol氯化钠粉末;
③1.0 mol镁粉、0.10 mol铁粉、0.10 mol氯化钠粉末。
实验2:向加有100 mL水的多个相同的隔热容器中分别加入由0.10 mol镁粉、0.50 mol铁粉及不同量的氯化钠粉末组成的混合物,不断搅拌,第15 min 时记录温度升高的幅度,结果见图2。
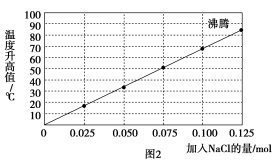
请回答下列问题:
(1)实验1证实了该反应的反应速率与________ 有关。
(2)实验2中当NaCl的用量大于0.125 mol时,实验就无需再做的原因是________ (填选项字母)。
A.加入更多的NaCl不再增加反应速率
B.加入NaCl反而会降低反应速率
C.已达到沸点不再有温度变化
D.需要加入更多的铁粉来提高温度
(3)如果在实验2中加入0.060 mol的NaCl,则第15 min 时混合物的温度最接近于________ (填字母)。
A.34 ℃ B.42 ℃ C.50 ℃ D.62 ℃
(4)加入铁粉和NaCl能使反应速率加快的原因是_______________ 。
实验1:向加有等量水的三个相同隔热容器中分别加入下列各组物质,结果见图1。

①1.0 mol镁条、0.10 mol铁粉、0.10 mol氯化钠粉末;
②将1.0 mol镁条剪成100份、0.10 mol铁粉、0.10 mol氯化钠粉末;
③1.0 mol镁粉、0.10 mol铁粉、0.10 mol氯化钠粉末。
实验2:向加有100 mL水的多个相同的隔热容器中分别加入由0.10 mol镁粉、0.50 mol铁粉及不同量的氯化钠粉末组成的混合物,不断搅拌,第15 min 时记录温度升高的幅度,结果见图2。

请回答下列问题:
(1)实验1证实了该反应的反应速率与
(2)实验2中当NaCl的用量大于0.125 mol时,实验就无需再做的原因是
A.加入更多的NaCl不再增加反应速率
B.加入NaCl反而会降低反应速率
C.已达到沸点不再有温度变化
D.需要加入更多的铁粉来提高温度
(3)如果在实验2中加入0.060 mol的NaCl,则第15 min 时混合物的温度最接近于
A.34 ℃ B.42 ℃ C.50 ℃ D.62 ℃
(4)加入铁粉和NaCl能使反应速率加快的原因是
您最近一年使用:0次



